
【題目】為了除去粗鹽中的少量泥沙和Ca2+、Mg2+、SO![]() 等雜質(zhì)離子,先將粗鹽溶于水,過濾,然后對濾液進行4項操作①過濾②加適量鹽酸③加過量的NaOH和Na2CO3混合溶液④加入過量BaCl2溶液。上述4項操作的正確順序為( )
等雜質(zhì)離子,先將粗鹽溶于水,過濾,然后對濾液進行4項操作①過濾②加適量鹽酸③加過量的NaOH和Na2CO3混合溶液④加入過量BaCl2溶液。上述4項操作的正確順序為( )
A.②①③④B.④②③①
C.④③①②D.②③④①
科目:高中化學 來源: 題型:
【題目】已知25℃時,H2SO3 的電離常數(shù)Ka1=1.23![]() 10-2,Ka2=5.6
10-2,Ka2=5.6![]() 10-8,HClO的電離常數(shù)Ka=2.98
10-8,HClO的電離常數(shù)Ka=2.98![]() 10-8,下列說法錯誤的是
10-8,下列說法錯誤的是
A. 常溫下,相同濃度的H2SO3 比HClO酸性強
B. 常溫下,將NaHSO3溶液滴入到NaClO溶液中發(fā)生反應:HSO3-+ClO-=SO32-+HClO
C. 常溫下,NaHSO3溶液中HSO3-的電離程度大于其水解程度,NaHSO3溶液呈酸性
D. 將pH=5的HClO溶液加水稀釋到pH=6時,溶液中部分離子濃度會升高
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以A為原料,經(jīng)過以下途徑可以合成一種重要的制藥原料有機物F。
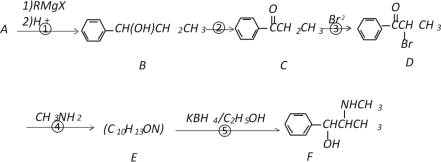
已知:
I.
II.A蒸氣的密度是相同條件下氫氣密度的53倍。
請回答下列問題:
(1)寫出A的結構簡式_____________;E中含氧官能團的名稱為__________________。
(2)D→E的反應類型是_____________,E→F的反應類型是_________________。
(3)寫出反應④的化學反應方程式___________________________________________。
(4)符合下列條件的C的同分異構體有________種(不考慮順反異構)。
a.苯環(huán)上有兩個取代基 b.能與NaOH溶液反應 c.分子中含有兩種官能團
(5)C的所有同分異構體在下列一種表征儀器中顯示的信號(或數(shù)據(jù))完全相同的是(_______)(填字母序號)
A.核磁共振儀 B.元素分析儀 C.質(zhì)譜儀 D.紅外光譜儀
(6)以A為原料可以合成高分子化合物G(  ),請設計出合理的合成路線(無機試劑任選)。________________________________________________________________
),請設計出合理的合成路線(無機試劑任選)。________________________________________________________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組探究酸化條件對0.1mol/LKI溶液氧化反應的影響。
序號 | 操作及現(xiàn)象 |
實驗1 | 取放置一段時間后依然無色的0.1mol/LKI溶液,加入淀粉溶液,溶液不變藍;向溶液中繼續(xù)加入2滴6mol/L的稀硫酸,溶液立即變藍 |
實驗2 | 取新制的0.1mol/LKI溶液,加入淀粉溶液,溶液不變藍;向溶液中繼續(xù)加入2滴6mol/L的稀硫酸,溶液10s后微弱變藍 |
(1)溶液變藍,說明溶液中含有____________ 。結合實驗1和實驗2,該小組同學認為酸化能夠加快I-氧化反應的速率。
(2)同學甲對滴加稀硫酸后溶液變藍速率不同的原因提出猜想:放置一段時間后的0.1mol/LKI溶液成分與新制0.1mol/LKI溶液可能存在差異,并繼續(xù)進行探究。
實驗3:取新制0.1mol/LKI溶液在空氣中放置,測得pH如下:
時間 | 5分鐘 | 1天 | 3天 | 10天 |
pH | 7.2 | 7.4 | 7.8 | 8.7 |
資料:
ⅰ.pH<11.7時,I-能被O2氧化為I。
ⅱ.一定堿性條件下,I2容易發(fā)生歧化,產(chǎn)物中氧化產(chǎn)物與還原產(chǎn)物的物質(zhì)的量之比為1∶5。
①用化學用語,解釋0.1mol/LKI溶液放置初期pH升高的原因:_________________________________________________________。
②對比實驗1和實驗2,結合化學用語和必要的文字,分析實驗1中加稀硫酸后“溶液立即變藍”的主要原因可能是_____________________________________________________________________________________。
(3)同學甲進一步設計實驗驗證分析的合理性。
序號 | 操作 | 現(xiàn)象 |
實驗4 | 重復實驗2操作后,繼續(xù)向溶液中加入 ________________。 | 溶液立即變藍 |
(4)該組同學想進一步探究pH對I2發(fā)生歧化反應的影響,進行了如下實驗。
實驗5:用20mL 4種不同濃度的KOH溶液與2mL淀粉溶液進行混合,測量混合液的pH后,向其中加入2滴飽和碘水,觀察現(xiàn)象。記錄如下:
實驗組 | A | B | C | D |
pH | 11.4 | 10.6 | 9.5 | 8.4 |
現(xiàn)象 | 無顏色變化 | 產(chǎn)生藍色后瞬間消失 | 產(chǎn)生藍色,30s后藍色消失 | |
從實驗5可以看出pH越大,歧化反應速率越_______________(填“快”或“慢”)。
解釋pH=8.4時,“產(chǎn)生藍色,30s后藍色消失”的原因:_________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碘在科研與生活中有重要作用,某興趣小組用0.50molL-1 KI、0.2%淀粉溶液、0.20molL-1 K2S2O8、0.10molL-1 Na2S2O3等試劑,探究反應條件對化學反應速率的影響。
已知:S2O82-+2I-=2SO42-+I2(慢) I2+2S2O32-=2I-+S4O62-(快)
(1)向KI、Na2S2O3與淀粉的混合溶液中加入一定量的K2S2O8溶液,當溶液中的 耗盡后,溶液顏色將由無色變?yōu)樗{色,為確保能觀察到藍色,S2O32-與S2O82-初始的物質(zhì)的量需滿足的關系為:n(S2O32-):n(S2O82-) 。
(2)為探究反應物濃度對化學反應速率的影響,設計的實驗方案如下表:
實驗 | 體積V/mL | ||||
K2S2O8溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
表中Vx= mL,理由是 。
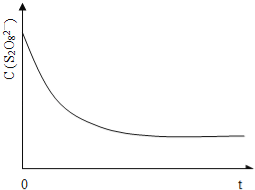
(3)已知某條件下,濃度c(S2O82-)~反應時間t的變化曲線如圖13,若保持其它條件不變,請在答題卡坐標圖中,分別畫出降低反應溫度和加入催化劑時c(S2O82-)~反應時間t的變化曲線示意圖(進行相應的標注)。
(4)碘也可用作心臟起捕器電源﹣鋰碘電池的材料,該電池反應為:2Li(s)+I2(s)=2LiI(s) △H
已知:4Li(s)+O2(g)=2Li2O(s) △H1
4LiI(s)+O2(g)=2I2(s)+2Li2O(s) △H2
則電池反應的△H= ;碘電極作為該電池的 極。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物HIn在水溶液中因存在以下電離平衡HIn(aq,紅色) ![]() H+(aq)+ In-(aq,黃色)故可作酸堿指示劑。濃度為0.02mol/L的下列溶液:① 鹽酸 ② 石灰水 ③ NaCl溶液 ④ NaHSO4溶液 ⑤ NaHCO3溶液 ⑥ 氨水,其中能使指示劑顯紅色的是
H+(aq)+ In-(aq,黃色)故可作酸堿指示劑。濃度為0.02mol/L的下列溶液:① 鹽酸 ② 石灰水 ③ NaCl溶液 ④ NaHSO4溶液 ⑤ NaHCO3溶液 ⑥ 氨水,其中能使指示劑顯紅色的是
A. ④⑤B. ③⑤C. ①④D. ②⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:H2O(g)=H2O(l) ΔH=Q1 kJ·mol-1
C2H5OH(g)=C2H5OH(l)ΔH=Q2 kJ·mol-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)ΔH=Q3 kJ·mol-1
若使46 g液體酒精完全燃燒,最后恢復到室溫,則放出的熱量為
A. -(3Q1-Q2+Q3) kJB. -0.5(Q1+Q2+Q3) kJ
C. -(0.5Q1-1.5Q2+0.5Q3) kJD. -(Q1+Q2+Q3) kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氧燃料電池是符合綠色化學理念的新型發(fā)電裝置。下圖為電池示意圖,該電池電極表面鍍一層細小的鉑粉,鉑吸附氣體的能力強,性質(zhì)穩(wěn)定。請回答:

(1)氫氧燃料電池的在導線中電流的方向為由______(用a、b表示)。
(2)負極反應式為______,正極反應式為___________。
(3)該電池工作時,H2和O2連續(xù)由外部供給,電池可連續(xù)不斷提供電能。因此,大量安全儲氫是關鍵技術之一。金屬鋰是一種重要的儲氫材料,吸氫和放氫原理如下:
Ⅰ 2Li+H2![]() 2LiH Ⅱ LiH+H2O=LiOH+H2↑
2LiH Ⅱ LiH+H2O=LiOH+H2↑
①反應Ⅰ中的還原劑是_________,反應Ⅱ中的氧化劑是_____。
②已知LiH固體密度為0.82g·cm-3,用鋰吸收224 L(標準狀況)H2,生成的LiH體積與被吸收的H2體積比為______。
③由②生成的LiH與H2O作用,放出的H2用作電池燃料,若能量轉化率為80%,則導線中通過電子的物質(zhì)的量為___mol。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com