
【題目】治理SO2、CO、NOx污染是化學工作者研究的重要課題。
Ⅰ.硫酸廠大量排放含SO2的尾氣會對環境造成嚴重危害。
(1)工業上可利用廢堿液(主要成分為Na2CO3)處理硫酸廠尾氣中的SO2,得到Na2SO3溶液,該反應的離子方程式為______。
Ⅱ.瀝青混凝土可作為反應;2CO(g)+O2(g)2CO2(g)的催化劑。如圖表示在相同的恒容密閉容器、相同起始濃度、相同反應時間段下,使用同質量的不同瀝青混凝土(α型、β型)催化時,CO的轉化率與溫度的關系。
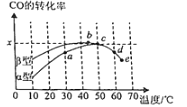
(2)a、b、c、d四點中,達到平衡狀態的是______。
(3)已知c點時容器中O2濃度為0.02molL-1,則50℃時,在α型瀝青混凝土中CO轉化反應的平衡常數K=______(用含x的代數式表示)。
(4)觀察分析圖,回答下列問題:

①CO轉化反應的平衡常數K(a)______K(c)。
②在均未達到平衡狀態時,同溫下β型瀝青混凝土中CO轉化速率比α型要______(填“大”、“小”)。
③______點時CO與O2分子之間發生有效碰撞的幾率在整個實驗過程中最高。
【答案】CO32-+SO2=SO32-+CO2 bcd ![]() > 大 e
> 大 e
【解析】
(1)工業上可利用廢堿液(主要成分為Na2CO3)處理硫酸廠尾氣中的SO2,得到Na2SO3溶液,結合原子守恒、電荷守恒書寫離子方程式;
(2)圖象分析可知b點反應達到平衡狀態,升溫平衡逆向進行;
(3)一氧化碳降解反應2CO(g)+O2(g)2CO2(g),K=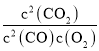 進行計算;
進行計算;
(4)①平衡常數是溫度的函數,溫度升高向吸熱方向進行,即向逆反應方向進行,K=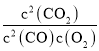 ,故K減小;
,故K減小;
②相同溫度下β型瀝青混凝土中CO降解速率比α型要大;
③溫度越高,有效碰撞的幾率越大;
(1)工業上可利用廢堿液(主要成分為Na2CO3)處理硫酸廠尾氣中的SO2,得到Na2SO3溶液,結合原子守恒、電荷守恒書寫離子方程式為:CO32-+SO2=SO32-+CO2;
(2)圖象分析可知b點反應達到平衡狀態,升溫平衡逆向進行,a、b、c、d四點中,達到平衡狀態的是bcd;
(3)CO的降解率為x,設起始CO濃度為1mol/L,
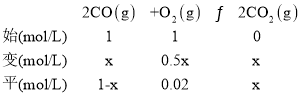
平衡常數K=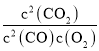 =
=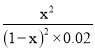 =
=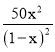 ;
;
(4)①平衡常數是溫度的函數,溫度升高向吸熱方向進行,即向逆反應方向進行,K=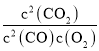 ,故K減小,即Ka>Kc;
,故K減小,即Ka>Kc;
②由圖得,相同溫度下β型瀝青混凝土中CO降解速率比α型要大;
③溫度越高,有效碰撞的幾率越大,故e點的有效碰撞的幾率是最大的;


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案 期末好成績系列答案
期末好成績系列答案科目:高中化學 來源: 題型:
【題目】在![]() 時,碳酸鈣在水中的沉淀溶解平衡曲線如圖所示,已知
時,碳酸鈣在水中的沉淀溶解平衡曲線如圖所示,已知![]() 時硫酸鈣的Ksp=9.1×10-6,下列說法正確的是( )
時硫酸鈣的Ksp=9.1×10-6,下列說法正確的是( )
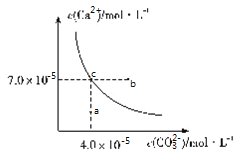
A.除去鍋爐水垢中硫酸鈣的辦法是將其轉化為碳酸鈣,然后用酸去除
B.圖中b點碳酸鈣的結晶速率小于其溶解速率
C.通過蒸發,可使溶液由a點變化到c點
D.在25℃時,反應![]() 的平衡常數K=3500
的平衡常數K=3500
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】分析下列反應在任何溫度下均能自發進行的是( )
A.2N2(g)+O2(g)═2N2O(g)△H=+163kJmol-1
B.Ag(s)+![]() Cl2(g)═AgCl(s)△H=-127kJmol-1
Cl2(g)═AgCl(s)△H=-127kJmol-1
C.HgO(s)═Hg(l)+![]() O2(g)△H=+91kJmol-1
O2(g)△H=+91kJmol-1
D.H2O2(l)═![]() O2(g)+H2O(l)△H=-98kJmol-1
O2(g)+H2O(l)△H=-98kJmol-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二氧化鈰(CeO2)是一種重要的稀土氧化物。以氟碳鈰礦(主要含 CeFCO3)為原料制備 CeO2 的一種工藝流程如下:
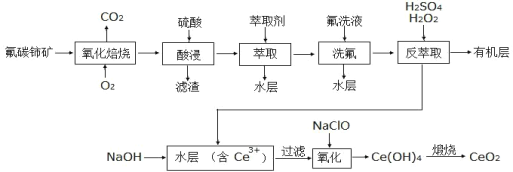
已知:①CeO2具有較強的氧化性,難溶于一般的酸或堿。
②F—能和很多金屬離子形成較為穩定的配合物,如Ce4+能與 F—結合成CeF3+,Al3+也能與 F—結合成 AlF63-;它的這種性質有利于酸浸步驟,卻不利于后續的沉淀步驟。
③Ce4+能被萃取劑 TBP 萃取,而 Ce3+不能。回答下列問題:
(1)“氧化焙燒”前需將礦石粉碎成細顆粒,其目的是_____。
(2)氧化焙燒后的固體產物中含有 CeO2 和 CeF4 物質的量之比為 3:1,“酸浸”時發生反應的離子方程式為_____________。傳統工藝中用鹽酸替代硫酸,其缺點為________________。
(3)TBP是一種有機萃取劑,“萃取”時存在反應CeF3++TBP![]() CeTBP4++F-,氟洗液中添加 Al3+的作用是________________。
CeTBP4++F-,氟洗液中添加 Al3+的作用是________________。
(4)“反萃取”步驟中發生反應的離子方程式為________________。
(5)反萃取后的水層溶液中 c(Ce3+)=1mol/L,c(Al3+)= 0.01mol/L,應先加入 NaOH 溶液調節溶液的___<pH<_______ ,除去 Al3+后,再加入 NaOH 調節溶液的 pH 大于_____(保留一位小數),即可確保 Ce3+已完全沉淀。(已知:常溫下,當溶液中的某離子濃度小于 1.0×10-5mol·L-1時,可認為該離子沉淀完全。Ksp[Al(OH)3]=1.0×10-32,Ksp[Ce(OH)3]=1.0×10-21)。
(6)CeO2是汽車尾氣凈化催化劑的關鍵成分,在尾氣消除過程中發生著 CeO2 與 CeO2(1-x) (0≤x≤0.25)的相互轉化。寫出 CeO2 消除 CO尾氣的化學方程式:______________。
(7)CeO2(1-x)中的 Ce為+3、+4 價,測定 x的值可判斷它們的比例。現取 CeO2(1-x)固體 0.8280 g,加入足量硫酸和 0.0110 molFeSO4·7H2O充分溶解,使 Ce4+全部被還原成 Ce3+,再用 0.1000 mol·L-1的酸性KMnO4標準溶液滴定至終點時,消耗 20.00 mL 標準溶液。(已知氧化性:Ce4+>KMnO4)
①x的值為_____。
②若加入的 FeSO4·7H2O 部分變質,會導致測定的 x 值_____(填“偏高”“偏低”或“不變”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖所示實驗裝置,能達到對應實驗目的或現象描述正確的是( )
A. 所示裝置用于 Cu 和濃 H2SO4 制取少量的 SO2 氣體
所示裝置用于 Cu 和濃 H2SO4 制取少量的 SO2 氣體
B.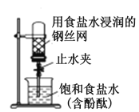 打開圖中的止水夾,一段時間后,可觀察到燒杯內溶液上升到試管中
打開圖中的止水夾,一段時間后,可觀察到燒杯內溶液上升到試管中
C.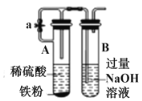 利用圖所示裝置制取 Fe(OH)2
利用圖所示裝置制取 Fe(OH)2
D. 利用圖測定中和反應反應熱
利用圖測定中和反應反應熱
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳酸亞鐵(白色固體,難溶于水)是一種重要的工業原料,可用于制備補血劑乳酸亞鐵,也可用作可充電電池的電極。某研究小組通過下列實驗,尋找利用復分解反應制備FeCO3的最佳方案:
實驗 | 試劑 | 現象 | |
滴管 | 試管 | ||
| 0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L Na2CO3溶液 (pH=11.9) | 實驗Ⅰ:立即產生灰綠色沉淀,5min后出現明顯的紅褐色 |
0.8 mol/L FeSO4溶液 (pH=4.5) | 1 mol/L NaHCO3溶液 (pH=8.6) | 實驗Ⅱ:產生白色沉淀及少量無色氣泡,2min后出現明顯的灰綠色 | |
0.8 mol/L (NH4)2Fe(SO4)2 溶液(pH=4.0) | 1 mol/L NaHCO3溶液 (pH=8.6) | 實驗Ⅲ:產生白色沉淀及無色氣泡,較長時間保持白色 | |
(1)實驗I中紅褐色沉淀產生的原因可用如下反應表示,請補全反應:_____________
![]() Fe2++
Fe2++ ![]() +
+ ![]() +
+ ![]() H2O
H2O ![]()
![]() Fe(OH)3 +
Fe(OH)3 + ![]() HCO3
HCO3
(2)實驗II中產生FeCO3的離子方程式為__________________。
(3)為了探究實驗III中NH4+所起的作用,甲同學設計了實驗IV進行探究:
操作 | 現象 | |
實驗IV | 向0.8 mol/L FeSO4溶液中加入________,再加入一定量Na2SO4固體配制成混合溶液(已知Na+對實驗無影響,忽略混合后溶液體積變化)。再取該溶液一滴管,與2mL 1mol/L NaHCO3溶液混合 | 與實驗III現象相同 |
實驗IV中加入Na2SO4固體的目的是_________。
對比實驗II、III、IV,甲同學得出結論:NH4+水解產生H+,降低溶液pH,減少了副產物Fe(OH)2的產生。
乙同學認為該實驗方案不夠嚴謹,應補充的對比實驗操作是:_________,再取該溶液一滴管,與2mL 1mol/L NaHCO3溶液混合。
(4)小組同學進一步討論認為,定性實驗現象并不能直接證明實驗III中FeCO3的純度最高,需要利用如圖所示的裝置進行定量測定。分別將實驗I、II、III中的沉淀進行過濾、洗滌、干燥后稱量,然后轉移至A處的廣口瓶中。

① 補全A中裝置并標明所用試劑。____________
② 為測定FeCO3的純度,除樣品總質量外,還需測定的物理量是____________。
(5)實驗反思:經測定,實驗III中的FeCO3純度高于實驗I和實驗II。通過以上實驗分析,制備FeCO3實驗成功的關鍵因素是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于有機物的說法正確的是
A.分子式為C5H10O2,且屬于酯的同分異構體共有9種(不考慮立體異構)
B.環己烯(![]() )分子中的所有碳原子共面
)分子中的所有碳原子共面
C.乙醇和丙三醇互為同系物
D.二環己烷( ![]() )的一氯代物有3種結構(不考慮立體異構)
)的一氯代物有3種結構(不考慮立體異構)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二甲醚作為燃料電池的原料,可通過以下途徑制取:
I.2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g) ΔH
CH3OCH3(g)+H2O(g) ΔH
II.2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ΔH
CH3OCH3(g)+3H2O(g) ΔH
(1)已知:①CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH1=-41.0kJ·mol-1
CO2(g)+H2(g) ΔH1=-41.0kJ·mol-1
②CO2(g)+3H2(g)![]() CH3OH(g)+ H2O(g) ΔH2=-49.0kJ·mol-1
CH3OH(g)+ H2O(g) ΔH2=-49.0kJ·mol-1
③CH3OCH3(g)+ H2O(g)![]() 2CH3OH(g) ΔH3=+23.5kJ·mol-1
2CH3OH(g) ΔH3=+23.5kJ·mol-1
則反應I的ΔH=_______kJ·mol-1
(2)在恒容密閉容器里按體積比為1:2充入一氧化碳和氫氣發生反應2CO(g)+4H2(g)![]() CH3OCH3(g)+H2O(g),一定條件下反應達到平衡狀態。當改變反應的某一個條件后,下列變化能說明平衡一定向正反應方向移動的是________。
CH3OCH3(g)+H2O(g),一定條件下反應達到平衡狀態。當改變反應的某一個條件后,下列變化能說明平衡一定向正反應方向移動的是________。
A.新平衡后c(CH3OCH3)增大
B.正反應速率先增大后減小
C.反應物的體積百分含量減小
D.化學平衡常數K值增大
(3)在10L恒容密閉容器中,均充入4molCO2和7molH2,分別以銥(Ir)和鈰(Ce)作催化劑,通過反應II:2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g)制二甲醚,反應進行相同的時間后測得的CO2的轉化率α(CO2)隨反應溫度的變化情況如圖所示。
CH3OCH3(g)+3H2O(g)制二甲醚,反應進行相同的時間后測得的CO2的轉化率α(CO2)隨反應溫度的變化情況如圖所示。
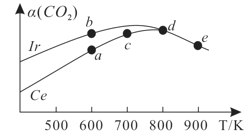
①根據圖1,下列說法不正確的是________。
A.反應II的ΔH<0,ΔS>0
B.600K時,H2的速率:v(b)正>v(a)逆
C.分別用Ir、Ce作催化劑時,Ce使反應II的活化能降低更多
D.從狀態d到e,α(CO2)減小的原因可能是溫度升高平衡逆向移動
②狀態e(900K)時,α(CO2)=50%,則此時的平衡常數K=______(保留3位有效數字)。
(4)寫出二甲醚堿性(電解質溶液為KOH溶液)燃料電池的負極電極反應式__________。該電池工作時,溶液中的OH-向______極移動,該電池工作一段時間后,測得溶液的pH減小。
(5)己知參與電極反應的電極材料單位質量放出電能的大小稱為該電池的比能量.關于二甲醚堿性燃料電池與乙醇堿性燃料電池,下列說法正確的是________。
A.兩種燃料互為同分異構體,分子式和摩爾質量相同,比能量相同
B.兩種燃料所含共價鍵數目相同,斷鍵時所需能量相同,比能量相同
C.兩種燃料所含共價鍵類型不同,斷鍵時所需能量不同,比能量不同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】1799年,英國化學家漢弗萊·戴維發現了N2O氣體。在食品行業中,N2O可用作發泡 劑和密封劑。
(l) N2是硝酸生產中氨催化氧化的副產物,NH3與O2在加熱和催化劑的作用下生成N2O的化學方程式為________。
(2)N2O在金粉表面發生熱分解反應:2N2O(g)=2N2(g)+O2(g)△H。
已知:2NH3(g)+3N2O(g)=4N2(g)+3H2O(l) △H1=-1010KJ/mol
4NH3(g)+3O2(g) =2N2(g)+6H2O(l) △H2=-1531KJ/mol
△H=__________。
(3)N2O和CO是環境污染性氣體,研究表明,CO與N2O在Fe+作用下發生反應:N2O(g)+CO(g)![]() CO2(g)十N2(g)的能量變化及反應歷程如下圖所示,兩步反應分別為:反應①Fe++N2O
CO2(g)十N2(g)的能量變化及反應歷程如下圖所示,兩步反應分別為:反應①Fe++N2O![]() FeO+N2;反應②______________
FeO+N2;反應②______________
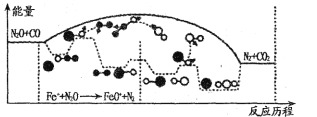
由圖可知兩步反應均為____(填“放熱”或“吸熱”)反應,由______(填“反應①或反應②”)決定反應達到平衡所用時間。
(4)在固定體積的密閉容器中,發生反應:N2O(g)+CO(g)![]() CO2(g)+N2(g),改變原料氣配比進行多組實驗(各次實驗的溫度可能相同,也可能不同),測定N2O的平衡轉化率。部分實驗結果如圖所示:
CO2(g)+N2(g),改變原料氣配比進行多組實驗(各次實驗的溫度可能相同,也可能不同),測定N2O的平衡轉化率。部分實驗結果如圖所示:
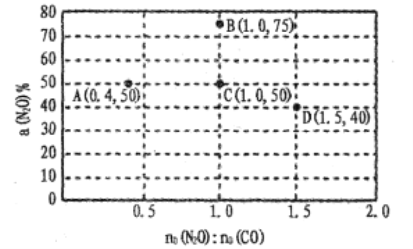
①如果要將圖中C點的平衡狀態改變為B點的平衡狀態,應采取的措施是:____ ;
②圖中C、D兩點對應的實驗溫度分別為TC和TD,,通過計算判斷TC____TD(填“>”“=”或“<”)。
(5)在某溫度下,向1L密閉容器中充入CO與N2O,發生反應:N2O(g)+CO(g)![]() CO2(g)十N2(g),隨著反應的進行,容器內CO的物質的量分數變化如下表所示:
CO2(g)十N2(g),隨著反應的進行,容器內CO的物質的量分數變化如下表所示:
時間/min | 0 | 2 | 4 | 6 | 8 | 10 |
物質的量分數 | 50.0% | 40.25% | 32.0% | 26.2% | 24.0% | 24.0% |
則該溫度下反應的平衡常數K=____。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com