
【題目】目前生物質能研究的方向之一是替代化石能源制備有機化工產品。
(1)化石原料合成丙烯腈(CH2=CH—CN):
已知:![]()
CH2=CH-CH3(g)+NH3(g)+![]() O2(g)→CH2=CH-CN(g)+3H2O(g) △H=-514.6kJ·mol-1
O2(g)→CH2=CH-CN(g)+3H2O(g) △H=-514.6kJ·mol-1
i:CH2=CH-CH3(g)+O2(g)→CH2=CH-CHO(g)+H2O(g) △H=-353.1kJ·mol-1
寫出反應ii的熱化學方程式:______。
(2)生物質原料合成丙烯腈:
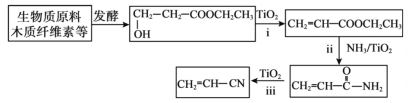
①寫出ii的化學方程式:_______。
②丙烯腈與1,3-丁二烯共聚生產的丁腈橡膠是現代工業重要的橡膠。寫出合成丁腈橡膠的化學方程式:______。
(3)生物質脂肪酸脫羧制備長鏈烷烴:H2氣氛,TiO2/Pt為催化劑,光催化長鏈脂肪酸轉化為長鏈烷烴機理示意圖如下:
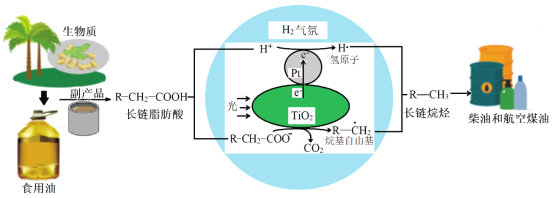
①油脂酸性水解可得高級脂肪酸和______(寫結構簡式)。
②TiO2界面發生的電極反應式為______。
【答案】![]()
![]()
![]() n
n![]() +n
+n![]()
![]()
![]()
![]()
【解析】
(1)反應ⅱ的化學方程式為:![]() ;通過分析可知該反應的焓變
;通過分析可知該反應的焓變![]() ;因此該反應的熱化學方程式為:
;因此該反應的熱化學方程式為:![]()
![]() ;
;
(2)①通過分析可知,CH2=CH-COOCH2CH3發生反應ⅱ后,酯基轉變為肽鍵,因此反應ⅱ實質是取代反應,方程式為:![]() ;
;
②丙烯腈與1,3-丁二烯發生共聚反應生成丁腈橡膠的方程式為:
n![]() +n
+n![]()
![]()
![]() ;
;
(3)①油脂是高級脂肪酸與甘油形成的酯,因此酸性條件下水解可得到高級脂肪酸和甘油即![]() ;
;
②由機理示意圖可知,長鏈脂肪酸首先解離成R-CH2-COO-和H+,其中H+在Pt的表面得電子變為氫原子,R-CH2-COO-則在TiO2的表面失電子生成一分子CO2的同時,產生烷基自由基,烷基自由基可與Pt表面產生的H原子結合形成長鏈烷烴,因此TiO2界面的電極反應式為:![]() 。
。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】砷(As)是第四周期ⅤA族元素,可以形成As2O3、As2O5、H3AsO3、H3AsO4等化合物,有著廣泛的用途。回答下列問題:
(1)畫出砷的原子結構示意圖____________。
(2)工業上常將含砷廢渣(主要成分為As2S3)制成漿狀,通入O2氧化,生成H3AsO4和單質硫。寫出發生反應的化學方程式________。該反應需要在加壓下進行,原因是________。
(3)已知:As(s)+![]() H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+2O2(g)=H3AsO4(s) ΔH1
H2(g)+![]() O2(g)=H2O(l) ΔH2
O2(g)=H2O(l) ΔH2
2As(s)+![]() O2(g) =As2O5(s) ΔH3
O2(g) =As2O5(s) ΔH3
則反應As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。
(4)298 K時,將20 mL 3x mol·L1 Na3AsO3、20 mL 3x mol·L1 I2和20 mL NaOH溶液混合,發生反應:AsO33(aq)+I2(aq)+2OH![]() AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)與反應時間(t)的關系如圖所示。
AsO43(aq)+2I(aq)+ H2O(l)。溶液中c(AsO43)與反應時間(t)的關系如圖所示。

①下列可判斷反應達到平衡的是__________(填標號)。
a.溶液的pH不再變化
b.v(I)=2v(AsO33)
c. c (AsO43)/c (AsO33)不再變化
d. c(I)=y mol·L1
②tm時,v正_____ v逆(填“大于”“小于”或“等于”)。
③tm時v逆_____ tn時v逆(填“大于”“小于”或“等于”),理由是_____________。
④若平衡時溶液的pH=14,則該反應的平衡常數K為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某菱鎂礦主要成分是MgCO3,還含有Al2O3、FeCO3、Fe2O3、SiO2等雜質,由該菱鎂礦制備高純MgO的流程如圖。回答下列問題:
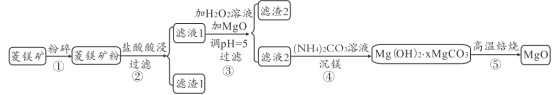
(1)將礦石粉碎的目的是_____,濾渣1的成分是_____
(2)步驟③先加入足量H2O2溶液,再加MgO調節溶液pH=5,加入足量的H2O2溶液后發生的所有氧化還原反應的方程式為_____
(3)濾渣2的成分是_____,1mol該濾渣用3mol/L硫酸溶解,需消耗硫酸_____mL
(4)列舉沉鎂之后的濾液的一種用途_____,稱取14.2g的![]() 在_____(填儀器名稱)中進行高溫焙燒得到的MgO質量為8.0g,則x=_____。
在_____(填儀器名稱)中進行高溫焙燒得到的MgO質量為8.0g,則x=_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列物質的實驗室制取、檢驗及分離方法不合理的是(夾持裝置已略去,氣密性已檢驗)。
A.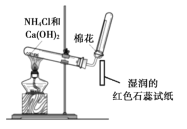 制取并檢驗氨氣
制取并檢驗氨氣
B.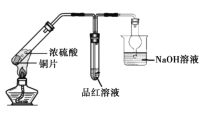 制取并檢驗SO2氣體
制取并檢驗SO2氣體
C. 制取并提純乙酸乙酯
制取并提純乙酸乙酯
D. 制取并檢驗乙炔
制取并檢驗乙炔
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聚乙烯胺可用于合成染料 Y,增加纖維著色度,乙烯胺(CH2=CHNH2)不穩定,所以 聚乙烯胺常用聚合物 X 水解法制備。下列說法不正確的是
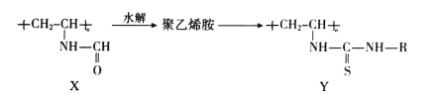
A. 聚合物 X 在酸性或堿性條件下發生水解反應后的產物相同
B. 測定聚乙烯胺的平均相對分子質量,可得其聚合度
C. 乙烯胺與 CH3CH=NH 互為同分異構體
D. 聚乙烯胺和 R-N=C=S 合成聚合物 Y 的反應類型是加成反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為檢驗某加碘食鹽中是否含有KIO3,取相同食鹽樣品進行下表所示實驗:
(已知:KIO3+5KI+3H2SO4=3I2+3K2SO4+3H2O)
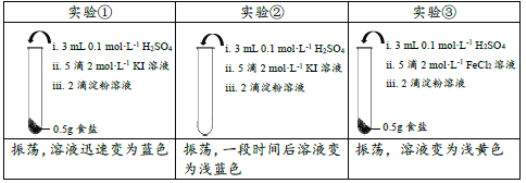
下列說法中不正確的是( )
A.僅由實驗①不能證明食鹽樣品中存在KIO3
B.實驗②中發生反應的離子方程式為4I-+O2+4H+=2I2+2H2O
C.實驗③溶液變黃色是生成了Fe3+,證明食鹽樣品中存在KIO3
D.結合實驗①和②的現象差異,可以推斷實驗樣品中存在KIO3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物甲的結構簡式為:![]() ,它可以通過下列路線合成(分離方法和其他產物已經略去)
,它可以通過下列路線合成(分離方法和其他產物已經略去)

(1)寫出 反應銀氨溶液反應的化學方程式_____。
反應銀氨溶液反應的化學方程式_____。
(2)寫出甲發生聚合反應的化學方程式_____。
(3)步驟 I 和 IV 在合成甲過程中的目的是_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,向20.00 mL 0.1000mol·L1HA中滴加0.1000mol·L1 NaOH溶液,溶液的pH隨NaOH溶液體積的變化如圖。已知Ka(HA)=5×10-4。

下列說法不正確的是( )
A.b點時,HA的電離大于A- 的水解,溶液呈酸性
B.從題給數據中無法計算a點時溶液的pH
C.忽略溶液混合體積變化,c點時pH近似為8
D.該滴定宜選擇酚酞作為終點判斷的指示劑
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究小組利用如圖裝置探究SO2和Fe(NO3)3溶液的反應原理。下列說法錯誤的是( )
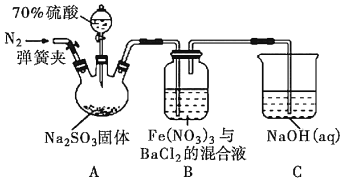
A.裝置B中若產生白色沉淀,說明Fe3+能將SO2氧化成SO![]()
B.實驗室中配制加70%的硫酸需要的玻璃儀器有量筒、燒杯、玻璃棒
C.三頸燒瓶中通入N2的操作應在滴加濃硫酸之前,目的是排盡裝置內的空氣
D.裝置C可能發生倒吸,同時還不能完全吸收反應產生的尾氣
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com