
常溫下,下列各組離子在指定溶液中能大量共存的是
A.在加入鋁粉能產生氫氣的溶液中:Fe2+、K+、NO3-、Cl-
B.澄清透明的溶液:Cu2+、SO42-、Mg2+、Cl-
C.含有大量Al3+的溶液中:K+、Ba2+、AlO2-、Cl-
D.pH=1的溶液:Na+、ClO-、K+、CH3COO-
科目:高中化學 來源: 題型:多選題
| A. | 碳酸鈉與稀鹽酸反應:CO32-+2H+═CO2↑+H2O | |
| B. | Fe與稀鹽酸反應:Fe+2H+═Fe2++H2↑ | |
| C. | Cl2與H2O反應:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 銅與濃硝酸反應:Cu+H++NO3-═Cu2++NO2↑+H2O |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北石家莊辛集中學高二上階段考一化學卷(解析版) 題型:選擇題
下列關于有機物的說法正確的是( )
A.有機物只能存在于動植物體內,不能通過人工的方法合成
B.有機物只含有碳、氫兩種元素
C.含碳元素的化合物不一定屬于有機物
D.烴是指燃燒后只生成CO2和H2O的有機物
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北石家莊辛集中學高二上階段考一化學卷(解析版) 題型:選擇題
下列說法正確的是( )
A.配制FeCl3溶液時,將FeCl3固體溶于適量鹽酸中,然后再用水稀釋到所需的濃度
B.為繪制中和滴定曲線,在滴定過程中,每隔相同時間用pH計測定一次錐形瓶中溶液的pH
C.測定溶液的pH時,應先將pH試紙潤濕,然后進行檢測
D.為準確測定鹽酸與NaOH溶液反應的中和熱,所用酸和堿的物質的量應相等
查看答案和解析>>
科目:高中化學 來源:2017屆江西省鷹潭市高三上學期第四次月考化學試卷 題型:選擇題
下列有關實驗原理、裝置、操作或結論的描述中,正確的(或實驗能達到預期目的)有(有關裝置中的夾持儀器略去未畫)( )項
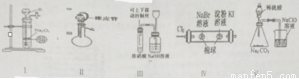
Ⅰ.仿啟普發生器制少量氧氣Ⅱ.該裝置檢查氣密性(止水夾已關)一打開分液漏斗活塞,液體順利流下Ⅲ.進行銅與濃硝酸反應的實驗Ⅳ.證明氧化性Cl2>Br2>I2Ⅴ.驗證酸性的強弱,H2SO4>H2CO3>HClO
A.1項
B.2項
C.3項
D.4項
查看答案和解析>>
科目:高中化學 來源:2017屆江西省鷹潭市高三上學期第四次月考化學試卷 題型:選擇題
某澄清透明溶液中只可能含有:①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥C032-⑦NO3-中的幾種,向該溶液中逐滴加入NaOH溶液至過量,生成沉淀的質量與NaOH的物質的量的關系如圖所示。則該溶液中一定含有的離子是
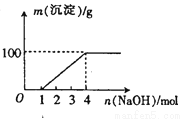
A.②⑤⑦
B.②③⑤⑦
C.③⑤⑦
D.①②③⑤⑦
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:實驗題
實驗題:
請從下圖中選用必要的裝置進行電解飽和食鹽水的實驗,要求測定產生的氫氣的體積(大于25mL),并檢驗氯氣的氧化性。
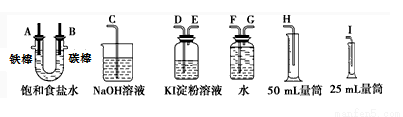
(1)A極發生的電極反應式是,B極發生的電極反應式是。
(2)設計上述氣體實驗裝置時,各接口的正確連接順序為:A接、接;B接、接。
(3)在實驗中,盛有KI淀粉溶液的容器中發生反應的離子方程式為。
(4)已知飽和食鹽水50mL(假設NaCl足量且忽略溶液體積變化),某時刻測得H2體積為16.8mL(標準狀況)。此時溶液pH約為。(lg2=0.3,lg3=0.5,lg5=0.7)
(5)已知甲烷燃料電池采用鉑為電極材料,兩電極上分別通入CH4和O2,電解質為KOH溶液。某研究小組將甲烷燃料電池作為電源,進行上述飽和食鹽水電解實驗。若甲烷通入量為1L(標準狀況),且反應完全,則理論上通過電解池的 電量為(已知NA=6.02×1023mol-1,電子電荷為1.60×10-19C,列式表示即可)。
電量為(已知NA=6.02×1023mol-1,電子電荷為1.60×10-19C,列式表示即可)。
查看答案和解析>>
科目:高中化學 來源:2017屆吉林省長春市高三上學期期中考試化學試卷(解析版) 題型:選擇題
O2F2可以發生反應:H2S+4O2F2=SF6+2HF+4O2,下列說法正確的是
A.氧氣是氧化產物
B.O2F2既是氧化劑又是還原劑
C.若生成4.48LHF,則轉移0.8mol電子
D.還原劑與氧化劑的物質的量之比為1:4
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com