
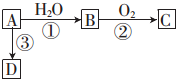
 已知A 是一種相對分子質量為28 的氣態烴,它可轉化為其他常見有機物.轉化關系如圖所示.
已知A 是一種相對分子質量為28 的氣態烴,它可轉化為其他常見有機物.轉化關系如圖所示.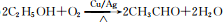 .
.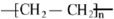 .
. 分析 A是一種相對分子質量為28的氣態烴,則A為CH2=CH2,CH2=CH2與水發生加成反應生成B為CH3CH2OH,CH3CH2OH發生氧化反應生成C為CH3CHO,D是一種聚合物,常用于塑料產品,則CH2=CH2發生加聚反應生成高聚物D為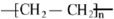 ,據此解答.
,據此解答.
解答 解:A是一種相對分子質量為28的氣態烴,則A為CH2=CH2,CH2=CH2與水發生加成反應生成B為CH3CH2OH,CH3CH2OH發生氧化反應生成C為CH3CHO,D是一種聚合物,常用于塑料產品,則CH2=CH2發生加聚反應生成高聚物D為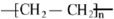 ,
,
(1)根據上面的分析可知,A為CH2=CH2,
故答案為:CH2=CH2;
(2)反應①為乙烯與水的加成,所以反應類型為加成反應,
故答案為:加成反應;
(3)B→C是乙醇在Cu或Ag作催化劑條件下發生氧化反應CH3CHO,反應方程式為: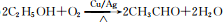 ,
,
故答案為: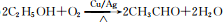 ;
;
(3)乙醇別直接氧化為乙酸,需要加入的試劑是:酸性高錳酸鉀溶液等,故答案為:酸性高錳酸鉀溶液;
(4)根據上面的分析可知,D為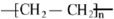 ,故答案為:
,故答案為: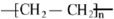 .
.
點評 本題考查有機物推斷,涉及烯與醇、醛、羧酸之間的轉化關系等,難度不大,注意基礎知識的理解掌握.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 配合物中中心原子的電荷數和配位數均為6 | |
| B. | 該配合物可能是平面正方形結構 | |
| C. | 4個Cl-和2個NH3分子均與Pt4+配位 | |
| D. | 配合物中4個Cl-與Pt4+配位,而2個NH3分子與Pt4+不配位 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鈉在空氣中露置會立刻被空氣氧化成過氧化鈉 | |
| B. | 鈉單質具有強還原性,可將銅從其鹽溶液中置換出來 | |
| C. | 鈉與鈉離子都具有強的還原性 | |
| D. | 鈉與稀鹽酸反應的實質是與氫離子的反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
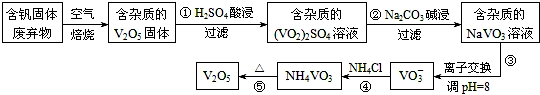
| 物質 | V2O5 | NH4VO3 | VOSO4 | (VO2)2SO4 |
| 溶解性 | 難溶 | 難溶 | 可溶 | 易溶 |
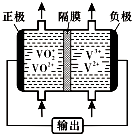
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
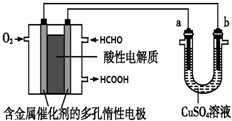
| A. | 當a、b都是銅做電極時,電解的總反應方程式為:2CuSO4+2H2O $\frac{\underline{\;通電\;}}{\;}$2H2SO4+2Cu+O2↑ | |
| B. | 燃料電池工作時,正極反應為:O2+2H2O+4e-═4 OH- | |
| C. | 當燃料電池消耗2.24L 甲醛氣體時,電路中理論上轉移2mol e- | |
| D. | 燃料電池工作時,負極反應為:HCHO+H2O-2e-═HCOOH+2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
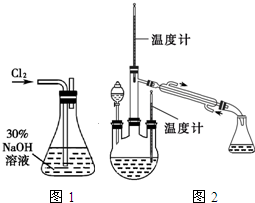 肼是重要的化工原料.某探究小組利用下列反應制取水合肼(N2H4•H2O).
肼是重要的化工原料.某探究小組利用下列反應制取水合肼(N2H4•H2O).查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
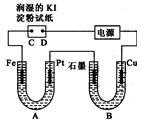 電解裝置如圖所示.圖中B裝置盛1000mL 3mol•L-1Na2SO4溶液,A裝置中盛1000mL 3mol•L-1AgNO3溶液.通電一段時間后,潤濕的淀粉KI試紙的C端變藍色.室溫下,若從電解開始到時間為t時,A、B裝置中共收集到16.8mL(標準狀況)氣體.若電解過程中無其他副反應發生,且溶液體積變化忽略不計,下列判斷正確的是( )
電解裝置如圖所示.圖中B裝置盛1000mL 3mol•L-1Na2SO4溶液,A裝置中盛1000mL 3mol•L-1AgNO3溶液.通電一段時間后,潤濕的淀粉KI試紙的C端變藍色.室溫下,若從電解開始到時間為t時,A、B裝置中共收集到16.8mL(標準狀況)氣體.若電解過程中無其他副反應發生,且溶液體積變化忽略不計,下列判斷正確的是( )| A. | 電子流動的方向:Fe→Pt→石墨→Cu | |
| B. | B中石墨上可能有紅色物質析出 | |
| C. | 若把Fe電極改成Ag電極,可向Pt上鍍銀 | |
| D. | t時A溶液的pH為3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 推測 | 操作和現象 | 結論 |
| 雜質中的正鹽成分可能有: A,、Na2S B,、Na2CO3 C,、Na2SO4 D,、Na2SO3 | ①取Wg產品配成稀溶液; ②向溶液中滴加過量BaCl2溶液,有白色沉淀生成,過濾,得沉淀和濾液; ③向沉淀中加入過量鹽酸,沉淀完全溶解,并有刺激性氣味的氣體產生. ④向濾液滴加2滴淀粉溶液,再逐滴加0.1000mol•L-1碘的標準溶液,消耗碘的標準溶液體積為18.10mL. | 產品雜質中: 一定含有Na2SO3, 可能含有Na2CO3Na2S, 一定不含有Na2SO4. 操作④發生的反應是: 2S2O32-+I2═S4O${\;}_{6}^{2-}$+2I- Ⅰ、判斷達到滴定終點的現象是溶液由無色變藍色,且半分鐘不褪色 Ⅱ、產品純度:(9/W)×100%. |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 制取氨氣并完成噴泉實驗(圖中夾持裝置均已略去).
制取氨氣并完成噴泉實驗(圖中夾持裝置均已略去).查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com