
【題目】從廢鈷酸鋰電池正極片(LiCoO2、乙炔炭黑、Al箔)中回收鈷和鋰的流程如圖:下列說法錯誤的是( )
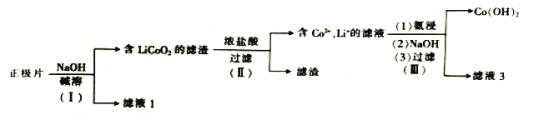
A.步驟(Ⅰ)中的濾液1中含有AlO2-
B.步驟(Ⅱ)中的濃鹽酸可用濃硝酸代替
C.步驟(Ⅲ)中的濾液3可用于回收鋰
D.合理處理廢舊電池有利于保護環境和資源再利用
【答案】B
【解析】
廢鈷酸鋰電池正極片(LiCoO2、乙炔炭黑、Al箔)中加入NaOH溶液堿溶,此時只有Al轉化為NaAlO2進入濾液1中,濾渣為LiCoO2、乙炔炭黑;加入濃鹽酸,乙炔炭黑不反應,進入濾渣,LiCoO2被濃鹽酸還原,Co由+3價轉化為Co2+,同時生成Li+和Cl2;經過氨浸、NaOH處理后,Co2+生成Co(OH)2沉淀,Li+進入濾液中。
A.由以上分析可知,步驟(Ⅰ)的濾液1中含有AlO2-,A正確;
B.步驟(Ⅱ)中的濃鹽酸若用濃硝酸代替,則無法將鈷由+3價還原為Co2+,B錯誤;
C.步驟(Ⅲ)中的濾液3中含有Li+,可用于回收鋰,C正確;
D.廢舊電池中含有鋰、鈷等可回收利用的資源,有利于保護環境和資源再利用,D正確;
故選B。


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】下列說法正確的是
A. ![]() 的一溴代物和
的一溴代物和![]() 的一溴代物都有4種(不考慮立體異構)
的一溴代物都有4種(不考慮立體異構)
B. CH3CH=CHCH3分子中的四個碳原子在同一直線上
C. 按系統命名法,化合物 的名稱是2,3,4-三甲基-2-乙基戊烷
的名稱是2,3,4-三甲基-2-乙基戊烷
D. ![]() 與
與![]() 都是α-氨基酸且互為同系物
都是α-氨基酸且互為同系物
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知A、B、C、D、E、F為元素周期表中原子序數依次增大的前20號元素,A與B,C、D與E分別位于同一周期。A原子L層上有2對成對電子,B、C、D的核外電子排布相同的簡單離子可形成一種C3DB6型離子晶體X,CE、FA為電子數相同的離子晶體。
(1)請寫出F離子的電子排布式_________。
(2)寫出X的化學式________,X的化學名稱為______。
(3)寫出X涉及化工生產中的一個化學方程式:__________。
(4)試解釋工業冶煉D不以DE3而是以D2A3為原料的原因:____________。
(5)F與B可形成離子化合物,其晶胞結構如圖所示。F與B形成的離子化合物的化學式為__________;該離子化合物晶體的密度為a g·cm-3,則晶胞的體積是________(只要求列出算式)。
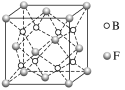
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一種制備草酸鐵銨晶體[(NH4)3Fe(C2O4)3]的工藝流程如下:
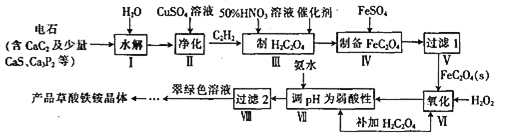
回答下列問題:
(1)CaC2的電子式為__________
(2)步驟Ⅱ主要是除去H2S、PH3等雜質氣體。在除PH3時,PH3被氧化為H3PO4,CuSO4被還原為Cu,該反應中氧化劑與還原劑的物質的量之比為____________
(3)步驟Ⅲ制H2C2O4時需要加熱硝酸的還原產物為NO,該反應的化學方程式為______________,硝酸的濃度及反應溫度都不宜過高,是因為____________.
(4)“過濾1”需對沉淀進行洗滌檢驗其是否洗滌干凈的依據是____________________
(5)步驟Ⅵ、VII補加草酸的目的是______________________.
(6)步驟VIII由濾液制得產品的操作為____________、____________、過濾、洗滌、干燥。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列難溶鹽的飽和溶液中,Ag+濃度最大的是( )
A.AgCl(Ksp=1.8×10-10 molL﹣1)
B.Ag2CO3(Ksp=8.1×10-12 molL﹣1)
C.Ag2CrO4(Ksp=9.0×10-12 molL﹣1)
D.AgBr(Ksp=5.0×10-13 molL﹣1)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】聯氨(N2H4)和次磷酸鈉(NaH2PO2)都具有強還原性,都有著廣泛的用途。
(1)已知:①N2H4(1)+O2(g)=N2(g)+2H2O(g) △H1=-621.5kJmol-1
②N2O4(1)=N2(g)+2O2(g) △H2=+204.3kJmol-1
則火箭燃料的燃燒反應為2N2H4(1)+N2O4(1)=3N2(g)+4H2O(g) △H=__。
(2)已知反應N2H4(g)+2Cl2(g)![]() N2(g)+4HCl(g),T℃時,向2L恒容密閉容器中加入2molN2H4(g)和4molCl2(g),測得Cl2和HCl的濃度隨時間的關系如圖所示。
N2(g)+4HCl(g),T℃時,向2L恒容密閉容器中加入2molN2H4(g)和4molCl2(g),測得Cl2和HCl的濃度隨時間的關系如圖所示。

①0~10min內,用N2(g)表示的平均反應速率v(N2)=__。
②M點時,N2H4的轉化率為__(精確到0.1)%。
③T℃時,達到平衡后再向該容器中加入1.2molN2H4(g)、0.4molCl2(g)、0.8molN2(g)、1.2molHCl(g),此時平衡__(填“正向移動”“逆向移動”或“不移動”)。
(3)①次磷酸(H3PO2)是一元酸,常溫下,1.0molL-1的NaH2PO2溶液pH為8,則次磷酸的Ka=__。
②用次磷酸鈉通過電滲析法制備次磷酸,裝置如圖所示。交換膜A屬于__(“陽離子”或“陰離子”)交換膜,電極N的電極反應式為___。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】電解原理在化學工業中有廣泛應用。如圖表示一個電解池,裝有電解液a;X、Y是兩塊電極板,通過導線與直流電源相連。請回答以下問題:
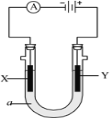
(1)若X、Y都是惰性電極,a是飽和NaCl溶液,實驗開始時,同時在兩邊各滴入幾滴酚酞試液,則
①電解池中X極上的電極反應式是___。在X極附近觀察到的現象是___。
②Y電極上的電極反應式是___,檢驗該電極反應產物的方法是___。
(2)如要用電解方法精煉粗銅,電解液a選用CuSO4溶液,則
①X電極的電極反應式是___。
②Y電極的材料是___。
③假若電路中有0.04摩爾電子通過時,陰極增重___克。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用燃燒法測定某種氨基酸(CxHyOzNm)的分子組成。取Wg該種氨基酸放在純氧中充分燃燒,生成二氧化碳、水和氮氣。按下圖所示裝置進行實驗。

回答下列問題:
(1)實驗開始時,首先通入一段時間的氧氣,其理由是__________________。
(2)以上裝置中需要加熱的儀器有_______ (填寫字母),操作時應先點燃_____處的酒精燈。
(3)A裝置中發生反應的化學方程式是____________________________。
(4)D裝置的作用是____________________________。
(5)讀取氮氣的體積時,應注意①_________________;②_________________。
(6)實驗中測得氮氣的體積為VmL(標準狀況),為確定此氨基酸的分子式,還需要的有關數據有____________________。
A.生成二氧化碳氣體的質量
B.生成水的質量
C.通人氧氣的體積
D.氨基酸的相對分子質量
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定溫度下,容器內某一反應中M、N的物質的量隨反應時間變化的曲線如下圖,
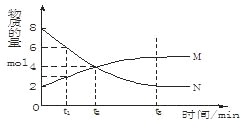
下列表述中正確的是
A.反應的化學方程式為: M![]() NB.t2時,正逆反應速率相等,達到平衡
NB.t2時,正逆反應速率相等,達到平衡
C.t3時,正反應速率大于逆反應速率D.t1時,N的濃度是M濃度的2倍
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com