
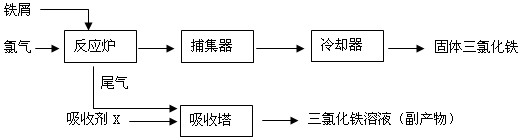
氯化鐵是常見的水處理劑,利用廢鐵屑可制備無水氯化鐵。實驗室制備裝置和工業制備流程圖如下:
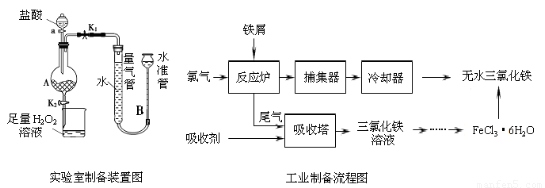
已知:(1)無水FeCl3的熔點為555 K、沸點為588 K。
(2) 廢鐵屑中的雜質不與鹽酸反應
(3)不同溫度下六水合氯化鐵在水中的溶解度如下:
溫度/℃ | 0 | 20 | 80 | 100 |
溶解度(g/100 g H2O) | 74.4 | 91.8 | 525.8 | 535.7 |
實驗室制備操作步驟如下:
Ⅰ.打開彈簧夾K1,關閉彈簧夾K2,并打開活塞a,緩慢滴加鹽酸。
Ⅱ.當??????? 時,關閉彈簧夾K1,打開彈簧夾K2,當A中溶液完全進入燒杯后關閉活塞a。
Ⅲ.將燒杯中溶液經過一系列操作后得到FeCl3·6H2O晶體。
請回答:
(1)燒杯中足量的H2O2溶液的作用是??????? 。
(2)為了測定廢鐵屑中鐵的質量分數,操作Ⅱ中“……”的內容是__________。
(3)從FeCl3溶液制得FeCl3?6H2O晶體的操作步驟是:加入? _??? 后、?? _?? 、過濾、洗滌、干燥.
(4)試寫出吸收塔中反應的離子方程式:????????????? 。
(5)捕集器溫度超過673 K時,存在相對分子質量為325的鐵的氯化物,該物質的分子式為???????????? 。
(6)FeCl3的質量分數通常可用碘量法測定:稱取m g無水氯化鐵樣品,溶于稀鹽酸,配制成100mL溶液;取出10.00mL,加入稍過量的KI溶液,充分反應后,滴入幾滴淀粉溶液,并用c mol?L-1 Na2S2O3溶液滴定,消耗V mL(已知:I2+2S2O32-═2I-+S4O62-)。
①滴定終點的現象是:??????????? _????????????
②樣品中氯化鐵的質量分數?????????????? _???????????
(1)把亞鐵離子全部氧化成三價鐵離子???? (2分)
(2)裝置A中不產生氣泡或量氣管和水準管液面不變(其他合理答案也給分)(2分)
(3)鹽酸(1分)???? 蒸發濃縮、冷卻結晶(1分)
(4)2Fe2+ + Cl2 = 2Fe3+? (2分)
(5)Fe2Cl6(2分)
(6)① 溶液由藍色變無色,且半分鐘內不變色(2分)
② (2分)
(2分)
【解析】
試題分析:(1)根據實驗裝置和操作步驟可知,實驗室制備無水FeCl3,是利用鐵與鹽酸反應生成FeCl2,然后把FeCl2氧化成FeCl3,先制得FeCl3·6H2O晶體,再脫結晶水制得無水FeCl3。燒杯中足量的H2O2溶液是作氧化劑,把亞鐵離子全部氧化成三價鐵離子;
(2)鐵與鹽酸反應完全時,不再產生氫氣,所以裝置A中不產生氣泡或量氣管和水準管的液面不再變化,此時,可將A中FeCl2溶液放入燒杯中進行氧化。
(3)從FeCl3溶液制得FeCl3?6H2O晶體的操作步驟是:蒸發濃縮、冷卻結晶、過濾、洗滌、干燥.
(4)從工業制備流程圖分析可知,反應爐中進行的反應是 2Fe + 3Cl2 = 2FeCl3 ,因此,進入吸收塔中的尾氣是沒有參加反應的氯氣,在吸收塔中氯氣被吸收劑吸收,反應后生成2FeCl3溶液,所以吸收劑應是2FeCl2溶液,反應的離子方程式為:2Fe2+ + Cl2 = 2Fe3+。
(5)捕集器收集的是氣態FeCl3,FeCl3的相對分子質量是162.5,由相對分子質量為325的鐵的氯化物可以推出,當溫度超過673 K時,二分子氣態FeCl3可以聚合生成雙聚體Fe2Cl6。(備注:FeCl3屬共價型化合物,能溶于乙醚、丙酮等有機溶劑,在673K蒸氣中有雙聚體,1023K以上分解為單分子)。
(6)① 稱取m g無水氯化鐵樣品,溶于稀鹽酸,配制成100mL溶液;取出10.00mL,加入稍過量的KI溶液,充分反應后,滴入幾滴淀粉溶液,此時溶液呈藍色,用 Na2S2O3溶液滴定,滴入最后一滴Na2S2O3溶液,錐形瓶內的溶液由藍色變為無色,且半分鐘內不變色。所以滴定終點的現象是:溶液由藍色變為無色,且半分鐘內不變色。
② 求樣品中氯化鐵的質量分數
由反應:2Fe3+ + 2I - = 2Fe2+ + I2 ;? I2+2S2O32-═2I-+S4O62- ;可得關系式:
?????????????? 2Fe3+? —? I2 —? 2S2O32-
???????????????? 1??????????????? 1
???????????????? n????????????? cV×10-3??
求得n(Fe3+) = cV×10-3 mol,? 則樣品中氯化鐵的質量分數為:
ω(Fe3+) = cV×10-3 mol×10×162.5g/mol×100% = 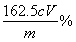
考點:化學實驗設計與評價


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
| ||
| ||
| 溫度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度/g | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
| 162.5cV |
| m |
| 162.5cV |
| m |
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
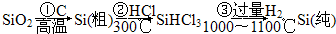
查看答案和解析>>
科目:高中化學 來源:山東省棗莊市2010屆高三年級調研考試理綜(化學部分)試題 題型:填空題
(11分)
“材料”的發現和使用往往會極大地推動生產、生活的發展,一些材料的出現甚至具有里程碑式劃時代的意義。請你回答以下問題:
(1)無機非金屬材料。高純度單晶硅是典型的無機非金屬材料,又稱“半導體”材料,它的發現和使用曾引起計算機的一場“革命”。這種材料可以按下列方法制備: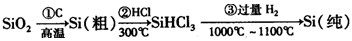
①寫出步驟①的化學方程式 。
②步驟②經過冷凝得到的SiHCl3(沸點33.0℃)中含有少量的SiCl4(沸點57.6℃)和HCl(沸點—84.7℃),提純SiHCl3的主要化學操作的名稱是 ;SiHCl3和SiCl4一樣遇水可發生劇烈水解,已知SiHCl3水解會生成兩種氣態產物,請寫出其水解的化學方程式 。
③請寫出二氧化硅與氫氟酸反應的化學方程式 。
(2)磁性材料。這種材料一般含有鐵元素,鐵是用途最為廣泛的金屬,也較為活潑,所以從它的使用開始就不斷實施著對它的防護。最常見的鐵制品腐蝕就是電化學腐蝕,請出最為普遍的電化學腐蝕的負極反應式 。
(3)激光材料。我國是激光技術先進的國家,紅寶石(Al2O3)是最早用于產生激光的材料,它是一種兩性氧化物,請用離子方程式加以說明:
, 。
(4)納米材料。膠體是一種物質以“納米”顆粒的形式分散到另一種物質里形成的分散系,膠體粒子的直經大約是 ,三氯化鐵溶液可以加速傷口止血,請簡述原因 。
(5)高分子材料。可以分成無機高分子材料和有機高分子材料。一種新型高效凈水劑
[AlFe(OH)nCl6—n]m就屬于無機高分子材料,廣泛應用于生活用水和工業污水處理,其中鐵元素的化合價為 。
一種合成纖維腈綸,又稱“人造羊毛”,由丙烯腈(CH2=CH—CN)為原料聚合生成,請寫出生成該有機高分子材料的化學方程式 。
查看答案和解析>>
科目:高中化學 來源:山東省棗莊市2010屆高三年級調研考試理綜(化學部分)試題 題型:填空題
(11分)
“材料”的發現和使用往往會極大地推動生產、生活的發展,一些材料的出現甚至具有里程碑式劃時代的意義。請你回答以下問題:
(1)無機非金屬材料。高純度單晶硅是典型的無機非金屬材料,又稱“半導體”材料,它的發現和使用曾引起計算機的一場“革命”。這種材料可以按下列方法制備:

①寫出步驟①的化學方程式 。
②步驟②經過冷凝得到的SiHCl3(沸點33.0℃)中含有少量的SiCl4(沸點57.6℃)和HCl(沸點—84.7℃),提純SiHCl3的主要化學操作的名稱是 ;SiHCl3和SiCl4一樣遇水可發生劇烈水解,已知SiHCl3水解會生成兩種氣態產物,請寫出其水解的化學方程式 。
③請寫出二氧化硅與氫氟酸反應的化學方程式 。
(2)磁性材料。這種材料一般含有鐵元素,鐵是用途最為廣泛的金屬,也較為活潑,所以從它的使用開始就不斷實施著對它的防護。最常見的鐵制品腐蝕就是電化學腐蝕,請出最為普遍的電化學腐蝕的負極反應式 。
(3)激光材料。我國是激光技術先進的國家,紅寶石(Al2O3)是最早用于產生激光的材料,它是一種兩性氧化物,請用離子方程式加以說明:
, 。
(4)納米材料。膠體是一種物質以“納米”顆粒的形式分散到另一種物質里形成的分散系,膠體粒子的直經大約是 ,三氯化鐵溶液可以加速傷口止血,請簡述原因 。
(5)高分子材料。可以分成無機高分子材料和有機高分子材料。一種新型高效凈水劑
[AlFe(OH)nCl6—n]m就屬于無機高分子材料,廣泛應用于生活用水和工業污水處理,其中鐵元素的化合價為 。
一種合成纖維腈綸,又稱“人造羊毛”,由丙烯腈(CH2=CH—CN)為原料聚合生成,請寫出生成該有機高分子材料的化學方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 溫度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度/g | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com