
【題目】如圖所示是用石墨和鐵作電極電解飽和食鹽水的裝置,請填空:
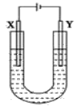
(1)X的電極名稱是________極,發生的電極反應式為:_______________________。Y極的電極材料是__________,檢驗X極產物的方法是___________________________________________。
(2)寫出該電極總反應的離子方程式:___________________________________。
(3)若食鹽水為100mL 兩極共放出2.24L氣體(標準狀況),則電路中通過電子的物質的量為___________。(假定電解后仍為100mL)
【答案】 陽 2Cl--2e-=Cl2↑ Fe 用濕潤的淀粉-碘化鉀試紙放在X極附近,若試紙變藍,說明Cl2產生 2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑ 0.1mol
2OH-+H2↑+Cl2↑ 0.1mol
【解析】(1)用石墨和鐵作電極電解飽和食鹽水,根據反應,則鐵作陰極,溶液中的氫離子在鐵電極上得電子生成氫氣,石墨作陽極,溶液中的氯離子在石墨上失電子生成氯氣,根據氯氣能使濕潤的淀粉碘化鉀試紙變藍來檢驗;
(2)電解飽和食鹽水生成氫氧化鈉、氫氣和氧氣;
(3)根據反應2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑計算轉移電子數。
2OH-+H2↑+Cl2↑計算轉移電子數。
(1)用石墨和鐵作電極電解飽和食鹽水,根據反應,則鐵作陰極,應為Y,溶液中的氫離子在鐵電極上得電子生成氫氣,石墨作陽極,應為X,溶液中的氯離子在石墨上失電子生成氯氣,電極反應為2Cl--2e-=Cl2↑;由于氯氣能使濕潤的淀粉碘化鉀試紙變藍來檢驗,所以檢驗X極的產物方法是用濕潤的淀粉-碘化鉀試紙放在X極附近,若試紙變藍,說明有Cl2產生;
(2)電解飽和食鹽水生成氫氧化鈉、氫氣和氧氣,方程式為2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑;
2OH-+H2↑+Cl2↑;
(3)電解飽和食鹽水生成氫氧化鈉、氫氣和氧氣,即2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑,兩極放出2.24L即0.1mol氣體(標準狀況),由方程式可知產生2mol氣體轉移2mol電子,則電路中通過電子的物質的量為0.1mol。
2OH-+H2↑+Cl2↑,兩極放出2.24L即0.1mol氣體(標準狀況),由方程式可知產生2mol氣體轉移2mol電子,則電路中通過電子的物質的量為0.1mol。


 學練快車道快樂假期寒假作業系列答案
學練快車道快樂假期寒假作業系列答案 新思維寒假作業系列答案
新思維寒假作業系列答案科目:高中化學 來源: 題型:
【題目】A、B、C是由周期表中短周期元素組成的三種常見化合物,甲、乙、丙是三種單質,這些單質和化合物之間存在如圖所示的關系,完成下列空白:
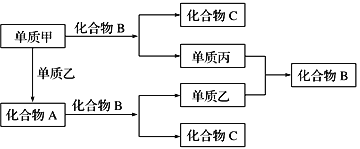
(1)向酚酞試液中加入化合物A的粉末,現象為________。
(2)單質甲與化合物B反應的離子方程式為__________。5.05g單質甲—鉀合金溶于200mL水生成0.075mol氫氣,確定該合金的化學式為______ 。
(3)向一定體積某濃度的化合物C的溶液中通人CO2氣體后得溶液M,因CO2通入量的不同,溶液M的組成也不同。若向M中逐滴加入0.1mol/L鹽酸,產生的氣體體積V(CO2)與加入鹽酸的體積V(HCl)的關系有下列圖示兩種情況。
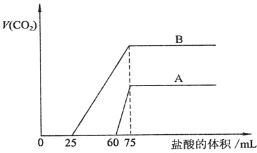
①由A確定滴加前60mL的鹽酸時,發生反應的離子方程式為_____________________
②B對應的溶液M低溫蒸干后得到固體a克,將a克固體充分加熱至恒重后,固體質量減少 _____ 克。
③由A、B可知,兩次實驗通入的CO2的體積比為___________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知:①能量越低的物質就越穩定;②白磷轉化成紅磷是放熱反應。據此判斷下列說法中正確的是( )
A.在相同的條件下,紅磷比白磷穩定
B.在相同的條件下,白磷比紅磷穩定
C.紅磷和白磷的結構相同
D.紅磷容易發生自燃而白磷則不會自燃
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有機物A的結構簡式為:![]()
(1)A的分子式為_____.
(2)A在NaOH水溶液中加熱,經酸化得到有機物B和D,D是芳香族化合物.當有1mol A發生反應時,最多消耗_____mol NaOH.
(3)B在一定條件下發生酯化反應可生成某五元環酯,該五元環酯的結構簡式為_____.
(4)寫出苯環上只有一個取代基且屬于酯類的D的所有同分異構體._____.
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】短周期主族元素X、Y、Z、W的原子序數依次增大。在下圖所示物質轉化關系中,e是由該四種元素組成的離子化合物,m是Y的單質,n是Z的單質,m、n均為空氣的主要成分,p是W的單質,其余為由上述的兩種或三種元素組成的化合物;u的水溶液具有漂白性;t和v均為一元強酸。下列說法正確的是
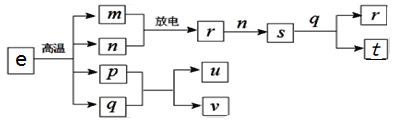
A. 物質u中既含共價鍵又含離子鍵
B. 常溫常壓下,r與s均為無色氣體
C. 簡單氣態氫化物的熱穩定性:Z<Y
D. X、Y、Z三種元素形成化合物的水溶液可能呈酸性,也可能呈堿性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式中正確的是( )
A. 鈉與水反應: Na +2H2O![]() Na++2OH– + H2↑
Na++2OH– + H2↑
B. 向氫氧化鋇溶液中加入稀硫酸: Ba2++OH–+ H++ ![]()
![]() BaSO4↓+H2O
BaSO4↓+H2O
C. 向Al2(SO4)3溶液中加入過量氨水:Al3++3NH3﹒H2O=Al(OH)3↓+3NH4+
D. 向碳酸氫銨溶液中加入足量石灰水: Ca2++![]() +OH–
+OH–![]() CaCO3↓+H2O
CaCO3↓+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下表是元素周期表的一部分, 針對表中的①~⑨種元素,填寫下列空白:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ |
(1)在這些元素中,化學性質最不活潑的是:_______(填具體元素符號或化學式,下同)。
(2) 在最高價氧化物的水化物中,酸性最強的化合物的子式是_________,第三周期中堿性最強的化合物的化學式是____________________。
(3)最高價氧化物是兩性氧化物的元素是____________;寫出它最高價氧化物對應水化物與氫氧化鈉反應的化學方程式_______________________________________。
(4)用電子式表示元素④與⑥形成化合物的形成過程:________________________,該化合物屬于__________________(填 “共價”或“離子”)化合物。
(5)表示③與①最高價態形成的化合物電子式___________________,該化合物分子由___________(填“極性”“非極性”)鍵形成。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下圖是氧氣氧化某濃度Fe2+為Fe3+過程的實驗結果,下列有關說法正確的是
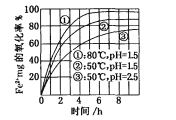
A. pH=1.5時氧化率一定比pH=2.5時大
B. 其他條件相同時,80℃的氧化率比50℃大
C. Fe2+的氧化率僅與溶液的pH和溫度有關
D. 該氧化過程的離子方程式為:Fe2++O2+4H+=Fe3++2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com