
有機物F是一種新型涂料固化劑,可由下列路線合成(部分反應條件略去):
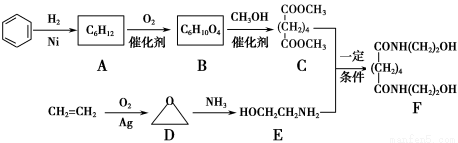
(1)B的結構簡式是____________;E中含有的官能團名稱是________。
(2)由C和E合成F的化學方程式是___________________________________________
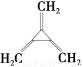
(3)同時滿足下列條件的苯的同分異構體的結構簡式是________________。
①含有3個雙鍵 ②核磁共振氫譜只顯示1個吸收峰 ③不存在甲基
(4)乙烯在實驗室可由______(填有機物名稱)通過________(填反應類型)制備。
(5)下列說法正確的是________(填字母序號)。
a.A屬于飽和烴 b.D與乙醛的分子式相同 c.E不能與鹽酸反應 d.F可以發生酯化反應
(1)HOOC(CH2)4COOH 羥基、氨基
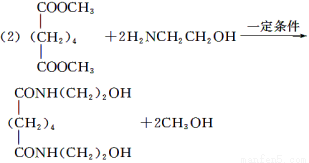
(3)
(4)乙醇 消去反應(其他合理答案均可)
(5)abd
【解析】根據合成路線圖中已知物質的結構簡式,推斷出其他物質的結構簡式,按照題目要求解答相關問題即可。(1)B和甲醇反應生成C,根據C的結構簡式可以判斷B為二元羧酸;E分子中有兩種官能團:氨基和羥基。(2)觀察C、E、F三者的結構簡式,可知C和E反應即為E中的HOCH2CH2NH—取代了C中的—OCH3,同時生成兩分子的甲醇。(3)苯的分子式為C6H6,離飽和烴還差8個氫原子,條件①該分子中存在3個雙鍵,要滿足碳、氫比,分子中還應存在一個環狀結構;條件②說明該分子呈對稱結構,分子中氫的位置是相同的;再結合條件③即可寫出該物質的結構簡式。(4)實驗室中是利用濃硫酸和乙醇反應制取乙烯的,該反應類型為消去反應。(5)A是環己烷,屬于飽和烴,所以a項正確;D的分子式為C2H4O,其分子式和乙醛的相同,所以b項正確;E分子中含有氨基,可以和鹽酸反應,所以c項錯誤;F分子中含有羥基,可以和羧酸發生酯化反應,所以d項正確。


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源:2014高考化學二輪專題突破 專題四氧化還原反應練習卷(解析版) 題型:選擇題
工業廢水中常含有一定量的Cr2O72-和CrO42-,它們會對生態系統造成很大的損害,其中還原沉淀法是常用的一種處理方法。流程如下:
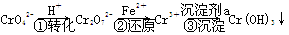
其中第①步中存在平衡:2CrO42- (黃色)+2H+??Cr2O72- (橙色)+H2O。下列有關說法正確的是( )
A.第①步當2v(Cr2O72-)=v(CrO42-)時,達到了平衡狀態
B.對于上述平衡,加入適量稀硫酸后,溶液顏色變黃色,則有利于CrO42-的生成
C.第②步中,還原0.1 mol Cr2O72-需要45.6 g FeSO4
D.第③步沉淀劑a可以使用NaOH等堿性物質
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題十五綜合實驗探究練習卷(解析版) 題型:實驗題
3,5?二甲氧基苯酚是重要的有機合成中間體,可用于天然物質白檸檬素的合成。一種以間苯三酚為原料的合成反應如下:

甲醇、乙醚和3,5?二甲氧基苯酚的部分物理性質見下表:
物質 | 沸點/℃ | 熔點/℃ | 密度(20 ℃) /g·cm-3 | 溶解性 |
甲醇 | 64.7 | — | 0.791 5 | 易溶于水 |
乙醚 | 34.5 | — | 0.713 8 | 微溶于水 |
3,5?二甲氧基苯酚 | — | 33~36 | — | 易溶于甲醇、乙醚,微溶于水 |
(1)反應結束后,先分離出甲醇,再加入乙醚進行萃取。①分離出甲醇的操作是________________。②萃取用到的分液漏斗使用前需________并洗凈,分液時有機層在分液漏斗的________(填“上”或“下”)層。
(2)分離得到的有機層依次用飽和NaHCO3溶液、飽和食鹽水、少量蒸餾水進行洗滌。用飽和NaHCO3溶液洗滌的目的是________;用飽和食鹽水洗滌的目的是________________________。
(3)洗滌完成后,通過以下操作分離、提純產物,正確的操作順序是________(填字母)。
a.蒸餾除去乙醚 b.重結晶
c.過濾除去干燥劑 d.加入無水CaCl2干燥
(4)固液分離常采用減壓過濾。為了防止倒吸,減壓過濾完成后應先________,再________。
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題十三無機化學綜合應用練習卷(解析版) 題型:填空題
工業上以碳酸錳礦為主要原料生產MnO2的工藝流程如下:
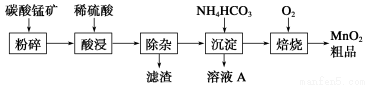
有關氫氧化物開始沉淀和沉淀完全的pH如下表:
氫氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
開始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
請回答下列問題:
(1)酸浸前將碳酸錳礦粉碎的作用是__________________。
(2)酸浸后的溶液中含有Mn2+、SO42—,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除雜過程如下:
①加入MnO2將Fe2+氧化,其離子反應方程式為__________________________。
②加入CaO將溶液的pH調到5.2~6.0,其主要目的是
_____________________________________________________________。
③加入BaS,除去Cu2+、Pb2+后,再加入NaF溶液,除去______________________。
(3)從溶液A中回收的主要物質是________________,該物質常用作化肥。
(4)MnO2粗品中含有少量Mn3O4,可以用稀硫酸處理,將其轉化為MnSO4和MnO2,然后再用氧化劑將Mn2+轉化為MnO2,制得優質MnO2。寫出Mn3O4與稀硫酸反應的化學方程式:______________________________。
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題十七有機化學基礎練習卷(解析版) 題型:推斷題
二甲氧芐胺嘧啶是一種用于家禽細菌感染防治藥。其合成路線如下:
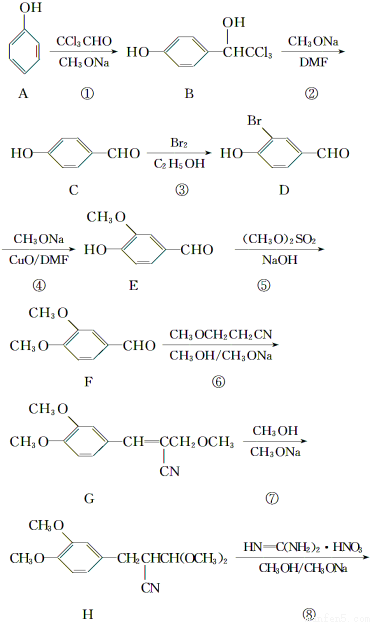
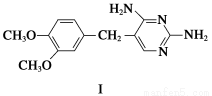
(1)化合物F的含氧官能團名稱為________、__________;合成路線中,步驟①、④的反應類型分別為______________、____________。
(2)化合物B的核磁共振氫譜中有________個峰。
(3)寫出F與新制氫氧化銅反應的化學方程式_______________________________。
(4)寫出同時滿足下列條件的E的同分異構體的結構簡式:__________________________。
Ⅰ.分子中苯環上有兩個取代基;
Ⅱ.能發生銀鏡反應;
Ⅲ.不能與FeCl3溶液發生顯色反應,但水解產物之一能發生此反應;
Ⅳ.核磁共振氫譜顯示有4個峰。
(5)實驗生產的產品中存在一種結構為 的副產物,為了使該產物的含量降到最低,需要合成路線中第________步反應的工藝最優化。
的副產物,為了使該產物的含量降到最低,需要合成路線中第________步反應的工藝最優化。
(6)已知 。化合物
。化合物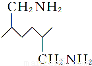 是合成染料的中間體,請寫出以氯乙烷為原料制備該化合物的合成路線流程圖(無機試劑任用)。合成路線流程圖示例如下:
是合成染料的中間體,請寫出以氯乙烷為原料制備該化合物的合成路線流程圖(無機試劑任用)。合成路線流程圖示例如下:
CH3CH2OH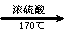 CH2=CH2
CH2=CH2 ?CH2—CH2?
?CH2—CH2?
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題十一常見金屬元素練習卷(解析版) 題型:選擇題
常溫常壓下過氧化鈉可與CO2反應,與CO不反應。現將CO2、CO的混合氣體在一定條件下和足量過氧化鈉充分反應后,若固體質量增加了28 g,下列說法正確的是( )
A.反應過程中,電子轉移數為2NA
B.固體生成物的質量為106 g
C.CO可能有剩余
D.反應后一定生成11.2 L氧氣
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題十一常見金屬元素練習卷(解析版) 題型:選擇題
實驗室中使用鋁鹽制備氫氧化鋁,為了使其中的鋁元素完全轉化為目標產物,應該選用的試劑是( )
A.碳酸 B.稀硫酸 C.氫氧化鈉溶液 D.氨水
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題八電化學練習卷(解析版) 題型:填空題
以黃銅礦精礦為原料,制取硫酸銅及金屬銅的工藝如下所示:
Ⅰ.將黃銅礦精礦(主要成分為CuFeS2,含有少量CaO、MgO、Al2O3)粉碎。
Ⅱ.采用如下裝置進行電化學浸出實驗
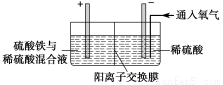
將精選黃銅礦粉加入電解槽陽極區,恒速攪拌,使礦粉溶解。在陰極區通入氧氣,并加入少量催化劑。
Ⅲ.一段時間后,抽取陰極區溶液,向其中加入有機萃取劑(RH)發生反應:2RH(有機相)+Cu2+(水相)  R2Cu(有機相)+2H+(水相)
R2Cu(有機相)+2H+(水相)
分離出有機相,向其中加入一定濃度的硫酸,使Cu2+得以再生。
Ⅳ.電解硫酸銅溶液制得金屬銅。
(1)黃銅礦粉加入陽極區與硫酸及硫酸鐵主要發生以下反應:
CuFeS2+4H+=Cu2++Fe2++2H2S
2Fe3++H2S=2Fe2++S↓+2H+
①陽極區硫酸鐵的主要作用是____________。
②電解過程中,陽極區Fe3+的濃度基本保持不變,原因是______________________。
(2)陰極區,電極上開始時有大量氣泡產生,后有固體析出,一段時間后固體溶解。寫出上述現象對應的反應式____________________。
(3)若在實驗室進行步驟Ⅲ,分離有機相和水相的主要實驗儀器是__________;加入有機萃取劑的目的是__________。
(4)步驟Ⅲ,向有機相中加入一定濃度的硫酸,Cu2+得以再生的原理是____________。
(5)步驟Ⅳ,若電解200 mL 0.5 mol·L-1的CuSO4溶液,生成銅3.2 g,此時溶液中離子濃度由大到小的順序是__________。
查看答案和解析>>
科目:高中化學 來源:2014高考化學二輪專題突破 專題九化學反應速率化學平衡練習卷(解析版) 題型:填空題
工業上合成氨的反應:N2(g)+3H2(g)  2NH3(g)ΔH=-92.60 kJ·mol-1。
2NH3(g)ΔH=-92.60 kJ·mol-1。
(1)在絕熱、容積固定的密閉容器中發生反應:N2(g)+3H2(g)  2NH3(g),下列說法能說明上述反應向正反應方向進行的是________(填序號)。
2NH3(g),下列說法能說明上述反應向正反應方向進行的是________(填序號)。
①單位時間內生成2n mol NH3的同時生成3n mol H2
②單位時間內生成6n mol N—H鍵的同時生成2n mol H—H鍵
③用N2、H2、NH3的物質的量濃度變化表示的反應速率之比為1∶3∶2
④混合氣體的平均摩爾質量增大
⑤容器內的氣體密度不變
(2)已知合成氨反應在某溫度下2 L的密閉容器中進行,測得如下數據:
時間(h) 物質的量(mol) | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0 | 0.20 |
| 1.00 | 1.00 |
根據表中數據計算:
①反應進行到2 h時放出的熱量為________ kJ。
②0~1 h內N2的平均反應速率為________ mol·L-1·h-1。
③此溫度下該反應的化學平衡常數K=________(保留兩位小數)。
④反應達到平衡后,若往平衡體系中再加入N2、H2和NH3各1.00 mol,化學平衡將向________方向移動(填“正反應”或“逆反應”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com