
右圖中每條折線表示周期表ⅣA~ⅦA中的某一族元素氫化物的沸點變化。每個小黑點代表一種氫化物,其中a點代表的是
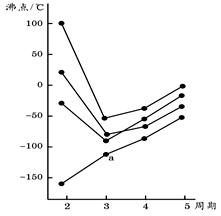
A.H2SB.HClC.PH3D.SiH4
 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源:2016-2017學年寧夏高一上第一次月考化學試卷(解析版) 題型:選擇題
將5 mol/L鹽酸10 mL稀釋到200 mL,再取出5 mL,這5 mL溶液的物質的量濃度是
A.0.05 mol/L B.0.25 mol/L
C.0.1 mol/L D.0.5 mol/L
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省高二上10月月考化學試卷(解析版) 題型:填空題
據《參考消息》報道,有科學家提出硅是“21世紀的能源”“未來的石油”的觀點。
(1)晶體硅在氧氣中燃燒的熱化學方程式為Si(s)+O2(g)=SiO2(s) ΔH=-989.2 kJ·mol-1,有關鍵能數據如下表:
化學鍵 | Si—O | O=O | Si—Si |
鍵能(kJ/mol) | x | 498.8 | 176 |
已知1 mol Si中含2 mol Si—Si鍵,1 mol SiO2中含4 mol Si—O鍵,則x的值為____________。
(2)假如硅作為一種普遍使用的新型能源被開發利用,關于其有利因素的下列說法中,你認為不妥當的是________________。
A.硅便于運輸、貯存,從安全角度考慮,硅是最佳的燃料
B.硅的來源豐富,易于開采,且可再生
C.硅燃燒放出的熱量大,且燃燒產物對環境污染程度低,容易有效控制
D.尋找高效新催化劑,使硅的生產耗能很低,是硅能源開發利用的關鍵技術
(3)工業制備純硅的反應為2H2(g)+SiCl4(g)=Si(s)+4HCl(g) ΔH=+240.4 kJ·mol-1,
生成的HCl通入100 mL 1 mol·L-1的NaOH溶液恰好反應,則反應過程中__________(填“吸收”或“釋放”)的熱量為________kJ。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省高二上10月月考化學試卷(解析版) 題型:選擇題
下列敘述正確的是
A.在某反應中,當反應物具有的總能量大于生成物具有的總能量時,該反應吸熱
B.同溫同壓下,4Al(s)+3O2(g)=2Al2O3(s)在常溫和點燃條件下的ΔH不同
C.稀溶液中:H+(aq)+OH- (aq)= H2O(l);ΔH=-53.7KJ/mol ,若將含0.5 mol H2SO4的濃溶液與含1 mol NaOH的溶液混合,放出的熱量大于53.7kJ
D.由C(石墨)= C(金剛石)△H= +1.90 kJ·mol-1 可知,金剛石比石墨穩定
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省校高二上月考化學試卷(解析版) 題型:填空題
新型儲氫材料是開發利用氫能的重要研究方向。
(1)Ti(BH4)3是一種儲氫材料,可由TiCl4和LiBH4反應制得。
①基態Cl原子中,電子占據的最高能層符號為,該能層具有的原子軌道數為_________。
②LiBH4由Li+和BH4-構成,BH4-的立體結構是,Li、B、H元素的電負性由大到小排列順序為_________。
(2)金屬氫化物是具有良好發展前景的儲氫材料。
①LiH中,離子半徑:Li+_________H-(填“>”、“=”或“<”)。
②某儲氫材料是短周期金屬元素M的氫化物。M的部分電離能如下表所示:
I1/KJ·mol-1 | I2/KJ·mol-1 | I3/KJ·mol-1 | I4/KJ·mol-1 | I5/KJ·mol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是_________(填元素符號)。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省校高二上月考化學試卷(解析版) 題型:選擇題
已知X、Y元素同周期,且電負性X<Y,下列說法錯誤的是
A. 第一電離能X可能大于Y
B. 氣態氫化物的穩定性:HmY小于HmX
C. 最高價含氧酸的酸性:X對應的酸性弱于Y對應的酸性
D. X和Y形成化合物時,X顯正價,Y顯負價
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省校高二上月考化學試卷(解析版) 題型:選擇題
下列粒子互為等電子體的是
A.NO和O2B.CH4和NH4+C.NH2?和H2O2D.HCl和H2O
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省高二上10月月考化學卷(解析版) 題型:選擇題
在體積、溫度都相同的條件下,反應2A(g)+2B(g)  C(g)+3D(g)分別從下列兩條途徑建立平衡:
C(g)+3D(g)分別從下列兩條途徑建立平衡:
Ⅰ.A、B的起始物質的量均為2 mol;
Ⅱ.C、D的起始物質的量分別為2 mol和6 mol。
以下敘述中不正確的是
A.Ⅰ、Ⅱ兩途徑最終達到平衡時,體系內混合氣體的百分組成相同
B.Ⅰ、Ⅱ兩途徑最終達到平衡時,體系內混合氣體的平均相對分子質量相同
C.達平衡時,Ⅰ途徑的反應速率vA等于Ⅱ途徑的反應速率vA
D.達平衡時,Ⅰ途徑所得混合氣體的密度為Ⅱ途徑所得混合氣體密度的
查看答案和解析>>
科目:高中化學 來源:2016-2017學年黑龍江省高一上9月月考化學卷(解析版) 題型:選擇題
自來水中因含少量的Fe3+而無法用于溶液的配制,實驗室為了除去Fe3+而獲得純凈水,可采用的方法是( )
A.蒸發 B.過濾 C.蒸餾 D.分液
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com