
【題目】(1)A、B、C是中學化學常見的三種物質,它們之間的相互轉化關系如圖所示(部分反應條件及產物略去)

(1)若A是一種黃色單質固體,則B→C的化學方程式為_______________。濃的D溶液使紙張變黑體現了它的___________性。
(2)若C是紅棕色氣體,則A化學式可能_________;寫出稀的D溶液與銅反應的離于方程式___________________________________________。
(II)工業上治煉鋁的原料是鋁土(主要成分是A12O3,雜質為Fe2O3、FeO、SiO2等)。某研究小阻設計的提純A12O3的方案如下

(3)濾液2中含有的溶質有NaOH、______和______(填化學式)。
(4)加入過量NaOH溶液過濾后,若濾渣中Fe(OH)2被空氣氧化,寫出其被氧化的化學方程式___________________________。
(5)寫出通入過量CO2生成沉淀A時反應的離子方程式為__________________。
【答案】2SO2+O2![]() 2SO3 脫水 N2或NH3 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O NaAlO2 NaCl 4Fe(OH)2+O2+2H2O=4Fe(OH)3 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
2SO3 脫水 N2或NH3 3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O NaAlO2 NaCl 4Fe(OH)2+O2+2H2O=4Fe(OH)3 AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
【解析】
(Ⅰ)A、B、C是中學化學常見的三種物質,A物質能連續氧化生成C,結合物質的性質分析判斷;
(II)氧化鋁、氧化鐵以及氧化亞鐵與鹽酸反應,二氧化硅不反應,過濾得到的濾液1中含有氯化鐵、氯化鋁、氯化亞鐵和鹽酸,加入過量的氫氧化鈉溶液,得到氫氧化亞鐵、氫氧化鐵、氯化鈉和偏鋁酸鈉,氫氧化亞鐵不穩定最終變為氫氧化鐵,過濾得到偏鋁酸鈉和氫氧化鈉以及氯化鈉的混合溶液,通入過量二氧化碳生成氫氧化鋁沉淀,氫氧化鋁灼燒得到氧化鋁,據此解答。
(Ⅰ)(1)若A是一種黃色單質固體,則A是單質硫,硫與氧氣反應生成B是二氧化硫,二氧化硫氧化生成C為三氧化硫,三氧化硫溶于水生成D是硫酸。其中B→C的化學方程式為2SO2+O2![]() 2SO3。濃硫酸能使紙張變黑體現了它的脫水性。
2SO3。濃硫酸能使紙張變黑體現了它的脫水性。
(2)若C是紅棕色氣體,C是二氧化氮,則B是NO,因此A可能是氮氣或氨氣,其化學式分別是N2、NH3;稀硝酸具有強氧化性,與銅反應的離于方程式為3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O。
(II)(3)反應中鹽酸過量,因此濾液1中含有氯化鐵、氯化鋁、氯化亞鐵和鹽酸,加入過量的氫氧化鈉溶液,得到氫氧化亞鐵、氫氧化鐵、氯化鈉和偏鋁酸鈉,氫氧化亞鐵不穩定最終變為氫氧化鐵,過濾得到偏鋁酸鈉和氫氧化鈉以及氯化鈉的混合溶液,因此濾液2中含有的溶質有NaOH、NaAlO2、NaCl。
(4)Fe(OH)2易被空氣氧化生成氫氧化鐵,反應的化學方程式為4Fe(OH)2+O2+2H2O=4Fe(OH)3。
(5)偏鋁酸鈉溶液和二氧化碳反應生成氫氧化鋁沉淀和碳酸氫鈉,則通入過量CO2生成沉淀A時反應的離子方程式為AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。


科目:高中化學 來源: 題型:
【題目】400 ℃時,某密閉容器中有X、Y、Z三種氣體,從反應開始到達到平衡時各物質濃度的變化如圖甲所示(假定反應向正反應方向進行)。圖乙為相應時刻僅改變反應體系中某一條件后正、逆反應速率隨時間變化的情況。

(1)反應從開始至平衡時v(X)=________________;A、B、C三點的逆反應速率由大到小的順序為_______________________________________________。
(2)若t3 s時改變的條件是降低壓強,則Z物質的起始濃度是________;400 ℃時該反應的平衡常數為________。
(3)t4 s時改變的條件是________,若該反應具有自發性,則此時平衡向________________(填“正反應方向”或“逆反應方向”)移動。
(4)在圖乙中繪制出t6 s時向容器中加入一定量X后建立新平衡的過程中(壓強保持不變)正、逆反應速率的變化曲線并注明速率類型。____________________
(5)研究表明,該反應經過如下幾個階段:
3X(g)![]() 2Q(s)+P(g) ΔH1 Q(s)===Y(g)+W(g) ΔH2 P(g)+2W(g)
2Q(s)+P(g) ΔH1 Q(s)===Y(g)+W(g) ΔH2 P(g)+2W(g)![]() Z(g) ΔH3
Z(g) ΔH3
試寫出X、Y、Z間反應的熱化學方程式________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈷(Co)及其化合物在工業上有廣泛應用。利用水鈷礦(主要成分為Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO等)制取CoC12·6H2O粗品的工藝流程圖如下:

已知:①浸出液含有的陽離子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、A13+等;
②部分陽離子以氫氧化物形式開始沉淀和完全沉淀時的pH如下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
請回答下列問題:
(1)上述工藝流程圖中操作a的名稱:_______________。
(2)寫出“浸出”時Co2O3發生反應的離子方程式:____________________。
(3)加入NaC1O3的作用是________________ 。
(4)萃取劑對金屬離子的萃取率與pH的關系如圖。使用萃取劑最適宜的pH范圍是_________(填字母序號)。
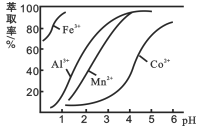
A.2.0~2.5 B. 3.0~3.5 C. 5.0~5.5 D. 9.5~9.8
(5)“除鈣”“鎂”是將溶液中Ca2+與Mg2+轉化為MgF2、CaF2沉淀。已知某溫度下,Ksp(MgF2)=7.35×10-11, Ksp(CaF2)=1.50×10-10。當加入過量NaF,所得濾液中c(Mg2+)/c(Ca2+)=_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,下列溶液中水的電離程度最小的是
A. pH=11的氨水 B. 0.01 mol/L的Na2CO3溶液
C. 0.01 mol/L的鹽酸 D. pH=4的NaHSO3溶液
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】我國化工專家侯德榜的“侯氏制堿法”曾為世界制堿工業做出了突出貢獻,他以飽和食鹽水、NH3、CO2為原料先制得NaHCO3,進而生產出純堿。回答下列問題:
某探究活動小組根據上述制堿原理,進行碳酸氫鈉的制備實驗,同學們按各自設計方案實驗。一位同學將二氧化碳氣體通入含氨的飽和食鹽水中制備碳酸氫鈉,實驗裝置如下圖所示(圖中夾持、固定用的儀器未畫出)。

(1)裝置甲中用稀鹽酸與CaCO3反應制備CO2,發現CaCO3與試管內的稀鹽酸不能接觸,在加稀鹽酸時,發現試劑瓶中的稀鹽酸已用完,為使反應能順利進行,可向長頸漏斗中加入的試劑是______________。
A.H2SO4溶液 B.CCl4 C.苯 D.稀硝酸
(2)乙裝置中的試劑是______________;丁裝置中稀硫酸的作用是______________。
(3)另一位同學用圖中戊裝置(其他裝置未畫出)進行實驗。實驗時,須先從______________管通入 __________氣體。
(4)有同學建議在戊裝置的b管下端連接己裝置,理由是______________ 。
(5)下表中所列出的是相關物質在不同溫度下的溶解度數據(g/100 g水):
0 ℃ | 10 ℃ | 20 ℃ | 30 ℃ | 40 ℃ | 50 ℃ | |
NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 |
NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
參照表中數據,請分析丙、戊裝置中使用冷卻水或者冰水的原因:______________。
(6)根據侯氏制堿原理制備少量NaHCO

(7)該小組同學為了測定丙中所得晶體的碳酸氫鈉的純度(假設晶體中不含碳酸鹽雜質),將晶體充分干燥后,稱量質量為w g。再將晶體加熱到質量不再變化時,稱量所得粉末質量為m g。然后進行下圖所示實驗:

①在操作Ⅱ中,為了判斷加入氯化鈣溶液是否過量,其中正確的是 ______________ (填字母)。
a.在加入氯化鈣溶液后,振蕩、靜置,向溶液中繼續加入少量氯化鈣溶液
b.在加入氯化鈣溶液后,振蕩、靜置,向溶液中再加入少量碳酸鈉溶液
c.在加入氯化鈣溶液后,振蕩、靜置,取上層清液再加入少量碳酸鈉溶液
②所得晶體中碳酸氫鈉的純度為______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列各種儀器:①漏斗②容量瓶③表面皿④分液漏斗⑤天平⑥量筒⑦膠頭滴管⑧蒸餾燒瓶。常用于物質分離的是( )
A.①③⑦B.②⑥⑦
C.①④⑧D.④⑥⑧
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】按要求回答問題。
(1)羰基硫的水解反應和氫解反應是兩種常用的脫硫方法:
水解反應: COS(g)+ H2O(g)![]() H2S(g)+CO2(g) △H=-34kJ/mol
H2S(g)+CO2(g) △H=-34kJ/mol
氫解反應:COS(g)+H2(g)![]() H2S(g)+CO(g) △H=+7kJ/mol
H2S(g)+CO(g) △H=+7kJ/mol
己知: 2H2(g)+O2(g)=2H2O(g) △H=-484 kJ/mol
寫出表示CO燃燒熱的熱化學方程式:_______________。
(2)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11;草酸H2C2O4,K1=5.9×10-2,K2=6.4×10-5; 0.1mol/LNa2CO3溶液的pH_____0.1mol/L Na2C2O4溶液的pH。(選填“大于”、“小于”或“等于”)。若將等分濃度的草酸溶液和碳酸溶液等體積混合,溶液中各種離子濃度大小的順序正確的是___________。(選填編號)
A.c(H+)>c(HC2O4-)> (HCO3-)>c (CO32-)
B.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C.c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-)
D.c(H2CO3) >c(HCO3-)>c(HC2O4-)>c(CO32-)
(3)已知:①難溶電解質的溶度積常數:Ksp(CaF2)=1.5×10-10;②25℃時2.0×10-3mol/L氫氟酸水溶液中,調節溶液pH(忽略體長變化),得到c(HF)、c(F-) 與溶液pH 的變化關系,如圖所示:
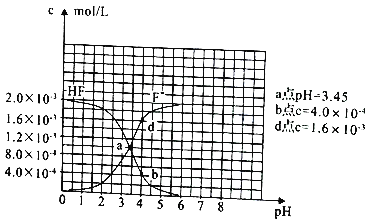
請根據信息回答下列問題:
①25℃時,HF電離平衡常數的數值Ka≈_______。
②4.0×10-3mol/LHF溶液與4.0×10-4mol/LCaCl2溶液等體積混合,調節混合液pH為4.0(忽略調節混合液體積的變化),通過列式計算說明是否有沉淀產生。____________。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com