
影響電離平衡的因素
外因
①溫度:由于電解質的電離是________的,故升高溫度,將使弱電解質的電離平衡向________方向移動.
②濃度:在一定溫度下,濃度的變化影響電離平衡移動.對于同一弱電解質來說,溶液越稀,離子相互碰撞結合成分子的機會越________,弱電解質的電離程度就越________.因此,稀釋溶液會使弱電解質的電離平衡向________方向移動.
③同離子效應:如果加入某種強電解質,其中含有弱電解質的組成離子,會使弱電解質的電離平衡向________方向移動,即加入具有與弱電解質相同離子的強電解質則抑制弱電解質的電離.如向CH3COOH溶液中加入CH3COONa固體,由于CH3COONa完全電離形成________和________,溶液中________濃度增大,使醋酸的電離平衡向________方向移動.
④化學反應:加入能與弱電解質電離出的離子發生反應的物質,則能________弱電解質的電離.如在CH3COOH溶液中加入金屬Mg,金屬Mg會與CH3COOH電離出的________發生反應而置換出________,使CH3COOH溶液中的________濃度減小,平衡會向________方向移動.
 導學教程高中新課標系列答案
導學教程高中新課標系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源:新課程同步學案專家伴讀 化學選修4(化學反應原理) 魯科版 魯科版 題型:022
影響電離平衡的因素
內因
與其他平衡一樣,弱電解質在水中達到電離平衡時,電離程度的大小主要是由________決定的.
查看答案和解析>>
科目:高中化學 來源:2011-2012年黑龍江哈三中高二上學期期中考試化學(理)試卷 題型:實驗題
(10分,每空2分)甲、乙兩個實驗小組利用KMnO4酸性溶液與H2C2O4溶液反應研究影響反應速率的因素。
(1)該反應的離子方程式為(提示:H2C2O4的一級電離平衡常數為5.4×10-2)
。
設計實驗方案如下(實驗中所用KMnO4溶液均已加入H2SO4):
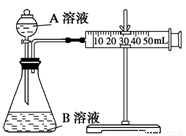
(2)甲組:通過測定單位時間內生成CO2氣體體積的大小來比較化學反應速率的大小。 實驗裝置如圖,實驗時分液漏斗中A溶液一次性放下,A、B的成分見下表:
|
序號 |
A溶液 |
B溶液 |
|
① |
2 mL 0.1 mol/L H2C2O4溶液 |
4 mL 0.01 mol/L KMnO4溶液 |
|
② |
2 mL 0.2 mol/L H2C2O4溶液 |
4 mL 0.01 mol/L KMnO4溶液 |
|
③ |
2 mL 0.2 mol/L H2C2O4溶液 |
4 mL 0.01 mol/L KMnO4溶液和少量MnSO4 |
該實驗探究的是 對化學反應速率的影響。在反應停止之前,相同時間內針管中所得CO2的體積由大到小的順序是 (用實驗序號填空)。
(3)乙組:通過測定KMnO4溶液褪色所需時間的多少來比較化學反應速率的大小。
取兩支試管各加入2 mL 0.1 mol/L H2C2O4溶液,另取兩支試管各加入4 mL 0.1 mol/L KMnO4溶液。將四支試管分成兩組(各有一支盛有H2C2O4溶液和KMnO4溶液的試管),一組放入冷水中,另一組放入熱水中,經過一段時間后,分別混合并振蕩,記錄溶液褪色所需時間。該實驗目的是研究 對化學反應速率的影響,但該組同學始終沒有看到溶液褪色,其原因是 。
查看答案和解析>>
科目:高中化學 來源:2011-2012年黑龍江哈三中高二上學期期中考試化學(理)試卷 題型:實驗題
(10分,每空2分)甲、乙兩個實驗小組利用KMnO4酸性溶液與H2C2O4溶液反應研究影響反應速率的因素。
(1)該反應的離子方程式為(提示:H2C2O4的一級電離平衡常數為5.4×10-2)

 。
。
設計實驗方案如下(實驗中所用KMnO4溶液均已加入H2SO4):
(2)甲組:通過測定單位時間內生成CO2氣體體積的大小來比較化學反應速率的大小。實驗裝置如圖,實驗時分液漏斗中A溶液一次性放下,A、B的成分見下表: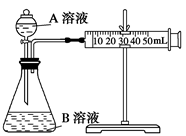
| 序號 | A溶液 | B溶液 |
| ① | 2 mL 0.1 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ② | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ③ | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液和少量MnSO4 |
 mol/L
mol/L H2C2O4溶液,另取兩支試管各加入4 mL 0.1 mol/L KMnO4溶液。將四支試管分成兩組(各有一支盛有H2C2O4溶液和KMnO4溶液的試管),一組放入冷水中,另一組放入熱水中,經過一段時間后,分別混合
H2C2O4溶液,另取兩支試管各加入4 mL 0.1 mol/L KMnO4溶液。將四支試管分成兩組(各有一支盛有H2C2O4溶液和KMnO4溶液的試管),一組放入冷水中,另一組放入熱水中,經過一段時間后,分別混合 并振蕩,記錄溶液褪色所需時間。該實驗目的是研究 對化學反應速率的影響,但該組同學始終沒有看到溶液褪色,其原因是 。
并振蕩,記錄溶液褪色所需時間。該實驗目的是研究 對化學反應速率的影響,但該組同學始終沒有看到溶液褪色,其原因是 。查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com