
【題目】已知H2O2是一種弱酸,在強堿溶液中主要以![]() 形式存在。現以AlH2O2燃料電池電解尿素[CO(NH2)2]的堿性溶液制備氫氣(電解池中隔膜僅阻止氣體通過,c、d均為惰性電極)。下列說法正確的是
形式存在。現以AlH2O2燃料電池電解尿素[CO(NH2)2]的堿性溶液制備氫氣(電解池中隔膜僅阻止氣體通過,c、d均為惰性電極)。下列說法正確的是
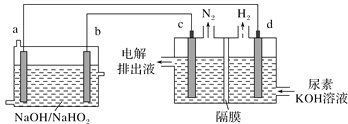
A. 燃料電池的總反應為:2Al+3![]() 2
2![]() +2H2O
+2H2O
B. 電解時,Al消耗2.7 g,則產生氮氣的體積為1.12 L
C. 電極b是負極,且反應后該電極區pH增大
D. 電解過程中,電子的流向:a→d,c→b
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數的數值,下列說法正確的是( )
A.1mol乙基中含有的電子數為16NA
B.8g CH4中含有10NA個電子
C.標準狀況下22.4L氯仿中共價鍵數目為4NA
D.28g乙烯、丙烯、丁烯的混合氣體,其碳原子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】等質量的鎂分別在足量的二氧化碳、氧氣中燃燒,有關敘述正確的是( )
A.在二氧化碳中燃燒產生的固體質量大
B.在氧氣中產生的氧化鎂質量大
C.氧化劑與還原劑物質的量之比都是2∶1
D.反應中都是氧元素被還原
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫代硫酸鈉(Na2S2O3)可用作分析試劑及鞣革還原劑。它受熱、遇酸易分解。工業上可用反應:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得。實驗室模擬該工業過程的裝置如圖所示。
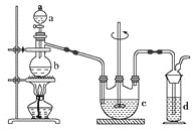
回答下列問題:
(1)a中試劑為__________,b中試劑為__________,c中試劑為____________________。
(2)反應開始后,c中先有渾濁產生,后又變澄清。此渾濁物是______________。
(3)d中的試劑為__________________。
(4)實驗中要控制SO2生成速率,可以采取的措施有________________(寫出兩條)。
(5)為了保證硫代硫酸鈉的產量,實驗中通入的SO2不能過量,原因是__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知乙烯能發生以下轉化:
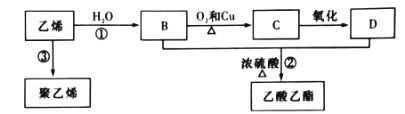
(1)乙烯是一種重要的化工原料,其產量是衡量一個國家_______的標志。
(2)反應①的反應類型是_______,D中含有的官能團的名稱為_____。
(3)寫出反應②的化學方程式:____________
(4)下列關于乙烯和聚乙烯的說法中,正確的是_______(填字母代號,下同)。
A.乙烯在常溫下是氣體,為純凈物 ;聚乙烯在常溫下是固體,為混合物
B.乙烯的化學性質比聚乙烯活潑
C.取等質量的乙烯和聚乙烯完全燃燒后,生成的 CO2和H2O的質量分別相等
D.乙烯和聚乙烯都能使溴水褪色
(5)乙醇的催化氧化過程如圖所示,下列對該反應過程的說法正確的是_____
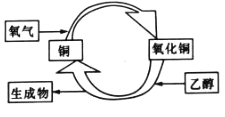
A.氧化劑是氧氣
B.生成物只有乙醛
C.銅是該反應的催化劑
D.銅絲出現紅、黑顏色交替變化的現象
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】綠色化學是指從技術、經濟上設計可行的化學反應,盡可能減少對環境的負作用。下列 化學反應不符合綠色化學概念的是( )
A. 消除硫酸廠尾氣排放:SO2+2NH3+H2O=(NH4)2SO3
B. 消除制硝酸廠的氮氧化物污染:NO2+NO+2NaOH=2NaNO2+H2O
C. 制 CuSO4:Cu+2H2SO4(濃) ![]() CuSO4+SO2↑+2H2O
CuSO4+SO2↑+2H2O
D. 制 CuSO4:2Cu+O2![]() 2CuO,CuO+H2SO4(稀)=CuSO4+H2O
2CuO,CuO+H2SO4(稀)=CuSO4+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】科學家一直致力于“人工固氮”的方法研究。
(1)目前合成氨的技術原理為:N2(g)+3H2(g) 2NH3(g) △H 該反應的能量變化如圖所示。
2NH3(g) △H 該反應的能量變化如圖所示。

①在反應體系中加入催化劑,反應速率增大,E2的變化是:______________。(填“增大”、“減小”或“不變”)。
②將一定量的N2(g)和H2(g)放入2L的密閉容器中,在500℃、2×107Pa下發生如下反應:![]()
5分鐘后達到平衡,測得N2為0.2 mol,H2為0.6 mol,NH3為0.2 mol。氮氣的平均反應速率v(N2)=_______________,H2的轉化率為_______________,該反應在此溫度下的化學平衡常數為_______________。(后兩空保留小數點后一位)
③欲提高②容器中H2的轉化率,下列措施可行的是____________。
A.向容器中按原比例再充入原料氣
B.向容器中再充入惰性氣體
C.改變反應的催化劑
D.液化生成物分離出氨
(2)1998年希臘亞里士多德大學的兩位科學家采用高質子導電性的SCY陶瓷(能傳導H+),從而實現了高轉化率的電解法合成氨。其實驗裝置如圖所示。陰極的電極反應式為_____________________。

(3)根據最新“人工固氮”的研究報道,在常溫、常壓、光照條件下,N2在催化劑(摻有少量Fe2O3和TiO2)表面與水發生下列反應:
2N2(g) +6H2O(l) ![]() 4NH3(g) +3O2(g) △H = a kJ/mol
4NH3(g) +3O2(g) △H = a kJ/mol
進一步研究NH3生成量與溫度關系,常壓下達到平衡時測得部分實驗數據如下:
T/K | 303 | 313 | 323 |
NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
此合成反應的a_________0。(填“大于”、“小于”或“等于”)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學實驗室產生的廢液中含有大量會污染環境的物質,為了保護環境,化學寶驗室產生的廢液必須經處理后才能排放。某化學實驗室產生的酸性廢液中含有Fe3+、Cu2+、Ba2+三種金屬陽離子和Cl-種陰離子,實驗室設計了下述方案對廢液進行處理,以回收金屬并測定含量,保護環境。
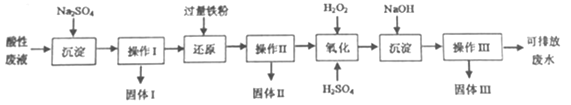
已知實驗中處理的酸性廢液的體積為IL,用pH計測定出其中H+物質的量濃度為0.10mol·L-1.
請回答下列問題:.
(1)實驗中操作I、II、III的方法相同,操作步驟依次為過濾、_________、干燥。
(2)“氧化”步驟所得溶液顏色為棕黃色,該反應的離子方程式為:_________
(3)檢驗可排放的廢水中不含Fe3+的方法是:_________
(4)實驗中稱量固體I的質量為4.66g,固體II的質量為15.2g,用足量的稀硝酸溶解固體II后產生了標準狀況下的無色氣體4.48L,則固體II中金屬銅的質量為_________
(5)實驗中將固體II進行充分灼燒,使用儀器除了酒精燈、三腳架、泥三角、玻璃棒外,還有_________(填名稱)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有機物命名正確的是( )
A.![]() 3-甲基-1,3-丁二烯
3-甲基-1,3-丁二烯
B.![]() 3-甲基丁酸
3-甲基丁酸
C.CH3CH(C2H5)CH2CH2CH32-乙基戊烷
D.![]() 2-羥基丁烷
2-羥基丁烷
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com