
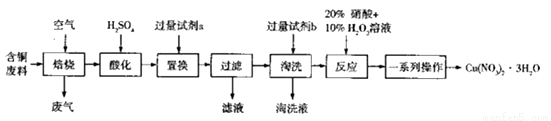
某工業含銅廢料含有Cu、CuO、CuS、CuSO4等成分,利用該含銅廢料可生產硝酸銅晶體[Cu(NO3)2 •3H2O],其生產工藝流程如圖所示:
回答下列問題:
(1)“焙燒”過程中生成SO2的化學方程式為___________________。
(2)“酸化”過程的離子方程式為__________________________。
(3)試劑a可以是__________________。
(4)“淘洗”的目的是___________,圖中的淘洗液與濾液溶質的陰離子相同,則試劑b是__________,淘洗液的溶質是__________。
(5)“反應”中使用20%硝酸和10% H2O2溶液,硝酸起酸的作用,則“反應”的化學方程式為______________。若該步驟只使用20%硝酸,隨著反應的進行,溫度升高,出現大量紅棕色氣體,則生成紅棕色氣體時反應中還原劑與氧化劑的物質的量之比為___________。
(6)“一系列操作”是指化學實驗操作,這些操作需要用到的玻璃儀器有_______________。
 孟建平小學滾動測試系列答案
孟建平小學滾動測試系列答案 黃岡天天練口算題卡系列答案
黃岡天天練口算題卡系列答案科目:高中化學 來源:2015-2016學年吉林省高二下學期基礎訓練(15)化學試卷(解析版) 題型:選擇題
在下列條件下,兩瓶氣體所含的原子數一定相等的是
A. 具有同質量、不同體積的N2O和CO2 B. 具有同溫度、同體積的CO和N2
C. 具有同體積、同密度的SO2和NO2 D. 具有同密度、不同質量的O2和O3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年陜西省西安市高一上學期期末考試化學試卷(解析版) 題型:選擇題
某國外化學教材中有一張關于氧化還原反應的插圖:由圖可知,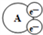 在該反應中是( )
在該反應中是( )
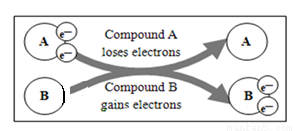
A. 還原劑 B. 氧化劑
C. 氧化產物 D. 還原產物
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省衡陽市高二理科實驗班下學期第一次月考理綜化學試卷(解析版) 題型:實驗題
2CH3CH2CH2CH2OH (CH3CH2CH2CH2)2O + H2O。反應物和產物的相關數據如下
(CH3CH2CH2CH2)2O + H2O。反應物和產物的相關數據如下
| 相對分子質量 | 沸點/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 74 | 117.2 | 0.8109 | 微溶 |
正丁醚 | 130 | 142.0 | 0.7704 | 幾乎不溶 |
合成反應:
①將6 mL濃硫酸和37 g正丁醇,按一定順序添加到A中,并加幾粒沸石。
②加熱A中反應液,迅速升溫至135℃,維持反應一段時間。
分離提純:
③待A中液體冷卻后將其緩慢倒入盛有70 mL水的分液漏斗中,振蕩后靜置,分液得粗產物。
④粗產物依次用40 mL水、20 mL NaOH溶液和40 mL水洗滌,分液后加入約3 g無水氯化鈣顆粒,靜置一段時間后棄去氯化鈣。
⑤將上述處理過的粗產物進行蒸餾,收集餾分,得純凈正丁醚11 g。
請回答:
(1)步驟①中濃硫酸和正丁醇的添加順序為 。
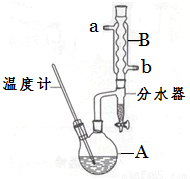
(2)加熱A前,需先從 (填“a”或“b”)口向B中通入水。
(3)步驟③的目的是初步洗去 ,振蕩后靜置,粗產物應從分液漏斗的 (填“上”或“下”)口分離出。
(4)步驟④中最后一次水洗的目的為 。
(5)步驟⑤中,加熱蒸餾時應收集 (填選項字母)左右的餾分。
a.100℃ b. 117℃ c. 135℃ d.142℃
(6)反應過程中會觀察到分水器中收集到液體物質,且分為上下兩層,隨著反應的進行,分水器中液體逐漸增多至充滿時,上層液體會從左側支管自動流回A。分水器中上層液體的主要成分為 ,下層液體的主要成分為 。
(7)本實驗中,正丁醚的產率為 。(保留兩位有效數字)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖南省衡陽市高二理科實驗班下學期第一次月考理綜化學試卷(解析版) 題型:選擇題
某溶液中含有大量的下列離子:Fe3+、SO42﹣、Al3+和M離子,經測定Fe3+、SO42﹣、Al3+和M離子的物質的量之比為1:4:1:2,則M離子可能是下列中的
A. Na+ B. OH﹣ C. S2﹣ D. Ag+
查看答案和解析>>
科目:高中化學 來源:2017屆河南省天一大聯考高三階段性測試(四)(b卷)理綜化學試卷(解析版) 題型:選擇題
用NA表示阿伏加德羅常數的值,下列說法正確的是
A. 標準狀況下,11g CO2含有的共用電子對數為0.5NA
B. 1mol Na分別與足量的O2反應生成Na2O或Na2O2,失去的電子數均為NA
C. 通常狀況下,39 g Na2O2固體中含有的離子總數為2NA
D. 滴加到沸水中的FeCl3溶液有5.6 g Fe3+發生水解,則生成的膠粒數為0.1NA
查看答案和解析>>
科目:高中化學 來源:浙江省衢州市2017屆高三1月教學質量檢測化學試卷 題型:實驗題
紙質一次性飯盒涂有石蠟(高級烷烴)和CaCO3,若它們在食物中溶出過量,食用后會影響身體健康。測定石蠟或CaCO3溶出量的實驗方法是:稱取飯盒質量(W1),剪碎,選用適當的浸泡劑浸泡一段時間,取殘渣洗滌、烘干、冷卻、稱重(W2)。W1-W2即物質溶出量。溶解浸泡試劑有NaCl溶液、稀醋酸、菜油可供選擇。
請回答:
(1)該實驗一定用不到的玻璃儀器是_______(填序號)。
①燒杯 ②坩堝鉗 ③酒精燈 ④集氣瓶 ⑤漏斗 ⑥天平 ⑦燃燒匙
(2)為了將石蠟和碳酸鈣分別溶出,選用的浸泡劑分別是______、_________。
(3)下列說法不正確的是______。
A.每種殘渣稱重操作至少要3次
B.測定CaCO3溶出量時,可用過濾法得到殘渣
C.殘渣不清洗會導致溶出量測定值偏大
D.分離菜油與石蠟油可用蒸餾的方法
查看答案和解析>>
科目:高中化學 來源:浙江省衢州市2017屆高三1月教學質量檢測化學試卷 題型:選擇題
下列說法不正確的是
A. 等物質的量的乙烯和乙醇完全燃燒消耗氧氣的量相等
B. 戊烷和2-甲基丁烷是同系物
C. 甲烷的二氯代物只有一種的事實,可證明甲烷為正四面體結構
D. 三硝酸甘油酯的分子式為C3H5N3O9
查看答案和解析>>
科目:高中化學 來源:2017屆山東省青島市高三第一次統一質量檢測理綜化學試卷(解析版) 題型:實驗題
氯化鐵可用作金屬蝕刻、有機合成的催化劑,研究其制備及性質是一個重要的課題。
(1)氯化鐵晶體的制備:
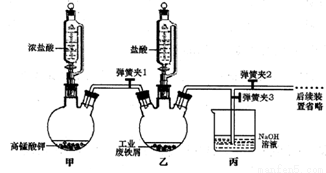
①實驗過程中裝置乙發生反應的離子方程式有________,儀器丙的作用為_________。
②為順利達成實驗目的,上述裝置中彈簧夾打開和關閉的順序為_______________。
③反應結束后,將乙中溶液邊加入_____________,邊進行加熱濃縮、______、過濾、洗滌、干燥即得到產品。
(2)氯化鐵的性質探究:
某興趣小組將飽和FeC13溶液進行加熱蒸發、蒸干灼燒,在試管底部得到固體。為進一步探究該固體的成分設計了如下實驗。(查閱文獻知:①FeC13溶液濃度越大,水解程度越小 ②氯化鐵的熔點為306℃、沸點為315℃ ,易升華,氣態FeCl3會分解成FeCl2和Cl2③ FeC12熔點670℃)
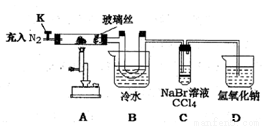
操作步驟 | 實驗現象 | 解釋原因 |
打開K , 充入氮氣 | D中有氣泡產生 | ①充入N2的原因________ |
關閉K, 加熱至600℃,充分灼燒固體 | B中出現棕黃色固體 | ②產生現象的原因__________ |
實驗結束,振蕩C靜置 | ③___________ | ④________________(用相關的方程式說明) |
⑤結合以上實驗和文獻資料,該固體可以確定的成分有______________________。 | ||
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com