
| AlT/(mol•L-1) | Ala/% | Alb/% | A1c/% |
| 0.208 | 1.4 | 86.6 | 12.0 |
| 0.489 | 2.3 | 86.2 | 11.5 |
| 0.884 | 2.3 | 88.1 | 9.6 |
| 1.613 | 3.1 | 87.0 | 9.9 |
| 2.520 | 4.5 | 88.2 | 7.3 |
分析 (1)結合原子守恒、電荷守恒書寫生成[AlO4Al12(OH)24(H2O)12]7+的離子方程式;
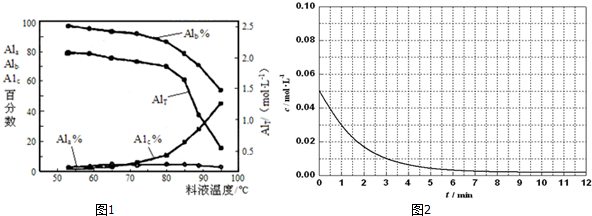
(2)①在一定溫度下,AlT越大,Ala%越大,Alc%越小,所以pH減小;
②如將AlT=2.520mol•L-1的聚合氯化鋁溶液加水稀釋,稀釋過程中主要鋁離子發生水解得到Al(OH)3(膠體);
③當T>80℃時,溫度升高鋁離子水解程度加大,產生氫氧化鋁沉淀增大;
(3)已知:①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ•mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ•mol-1
根據蓋斯定律,①+②可得:Al2O3(s)+3C(s)=2Al(l)+3CO(g);
反應①常壓下在1900℃的高溫下才能進行,△H-T△S<0反應自發進行;
(4)pH計測定溶液pH值,元素分析儀分析組成元素,原子吸收光譜儀分析組成元素,用于比色分析的儀器是分光光度計;
(5)隨反應進行Al3+濃度減小,則Al${\;}_{\frac{1}{2}}$X21.5+濃度增大,且△c(Al${\;}_{\frac{1}{2}}$X21.5+)=2△c(Al3+).
解答 解:(1)向1.0mol•L-1 AlCl3溶液中加入0.6mol•L-1的NaOH溶液,可制得Alb含量約為86%的聚合氯化鋁溶液,根據原子守恒、電荷守恒可得生成[AlO4Al12(OH)24(H2O)12]7+的離子方程式為:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+,
故答案為:13Al3++32OH-+8H2O=[AlO4Al12(OH)24(H2O)12]7+;
(2)①在一定溫度下,AlT越大,Ala%越大,Alc%越小,所以pH越小,故答案為:越小;
②如將AlT=2.520mol•L-1的聚合氯化鋁溶液加水稀釋,則稀釋過程中主要發生反應的離子方程式:Al3++3H2O?Al(OH)3(膠體)+3H+,
故答案為:Al3++3H2O?Al(OH)3(膠體)+3H+;
③膜蒸餾料液溫度對鋁聚合形態百分數及鋁的總濃度的影響如圖所示,當T>80℃時,AlT顯著下降的原因是:溫度升高,水解程度加大,產生氫氧化鋁沉淀,
故答案為:溫度升高,水解程度加大,產生氫氧化鋁沉淀;
(3)已知:①Al2O3(s)+AlCl3(g)+3C(s)=3AlCl(g)+3CO(g)△H1=a kJ•mol-1
②3AlCl(g)=2Al(l)+AlCl3(g)△H2=b kJ•mol-1
根據蓋斯定律,①+②可得:Al2O3(s)+3C(s)=2Al(l)+3CO(g),則△H=△H1+△H2=(a+b)kJ/mol;
該反應△S>0,反應①常壓下在1900℃的高溫下才能進行,△H-T△S<0反應自發進行,說明該反應△H>0,
故答案為:(a+b);>;
(4)pH計測定溶液pH值,元素分析儀分析組成元素,原子吸收光譜儀分析組成元素,用于比色分析的儀器是分光光度計,
故選:C;
(5)隨反應進行Al3+濃度減小,則Al${\;}_{\frac{1}{2}}$X21.5+濃度增大,且△c(Al${\;}_{\frac{1}{2}}$X21.5+)=2△c(Al3+),Al${\;}_{\frac{1}{2}}$X21.5+濃度隨時間的變化曲線為: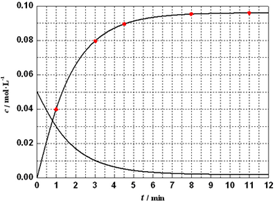 ,
,
故答案為: .
.
點評 本題考查學生對信息獲取與知識遷移應用、反應熱有關計算等,題目綜合性非常強,題目素材陌生,增大題目難度,很好的考查學生對化學反應原理的掌握程度,難度較大.


科目:高中化學 來源: 題型:多選題
| A. | 鐵做還原劑 | B. | Fe2O3做氧化劑 | ||
| C. | 鐵元素被還原 | D. | 鐵元素化合價升高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
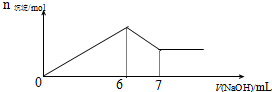 現有AlCl3和MgSO4混合溶液,向其中不斷加入0.1mol/L 的NaOH溶液,得到沉淀的量與加入NaOH溶液的體積如圖所示,原溶液中Cl-與SO42-的物質的量之比為( )
現有AlCl3和MgSO4混合溶液,向其中不斷加入0.1mol/L 的NaOH溶液,得到沉淀的量與加入NaOH溶液的體積如圖所示,原溶液中Cl-與SO42-的物質的量之比為( )| A. | 2:1 | B. | 2:3 | C. | 6:1 | D. | 3:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 鋅和稀硫酸反應時,加入少量的CuSO4溶液可使反應加快 | |
| B. | 紅熱的鐵絲與冷水接觸,表面表成藍黑色保護層 | |
| C. | 鍍鋅鐵表面鋅有劃損時,仍然能阻止鐵被氧化 | |
| D. | 在空氣中金屬鋁表面迅速氧化形成保護層 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 屬于金屬元素 | B. | 中子數與質子數之差為29 | ||
| C. | 原子的核外電子數為13 | D. | 27Al和42Al是兩種不同的核素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 體積 | B. | 質量 | C. | 原子數 | D. | 分子數 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| X | Y | Z | |
| R | W | ||
| T |
| A. | 簡單離子半徑大小關系為:W>R>Z>Y | |
| B. | X有多種同素異形體,而Z不存在同素異形體 | |
| C. | R2W3可用RCl3溶液與Na2W溶液混合制取 | |
| D. | T的單質既能與鹽酸反應又能與NaOH溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 銅片插入FeCl3溶液中:Cu+2Fe3+═Cu2++2 Fe2+ | |
| B. | 氯化鋁溶液中加入過量的氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 燒堿溶液中加鋁片:2Al+2OH-+2H2O═2 AlO2-+3H2↑ | |
| D. | 鐵粉與稀鹽酸的反應:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com