
碲(Te)為ⅥA族元素,是當今高新技術新材料的主要成分之一。工業上可從電解精煉銅的陽極泥中提取碲。
(1)粗銅中含有Cu和少量Zn、Ag、Au、TeO2及其他化合物,電解精煉后,陽極泥中主要含有TeO2、少量金屬單質及其他化合物。電解精煉粗銅時,陽極電極反應式為 。
(2)TeO2是兩性氧化物,微溶于水,可溶于強酸或強堿。從上述陽極泥中提取碲的一種工藝流程如下: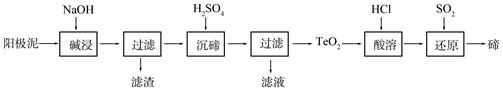
①“堿浸”時TeO2發生反應的化學方程式為 。
②“沉碲”時控制溶液的pH為4.5-5.0,生成TeO2沉淀。如果H2SO4過量,溶液酸度過大,將導致碲的沉淀不完全,原因是 ;防止局部酸度過大的操作方法是 。
③“酸溶”后,將SO2通入TeCl4溶液中進行“還原”得到碲,該反應的化學方程式是 。
(1)Zn-2e-=Zn2+ Cu-2e-=Cu2+ (共4分,各2分)
(2)① TeO2+2NaOH=Na2TeO3+H2O (3分)
②TeO2是兩性氧化物,H2SO4過量會導致TeO2繼續與H2SO4反應導致損失。(3分)
緩慢加入H2SO4,并不斷攪拌 (3分)
③ TeCl4 + 2SO2 + 4H2O="Te" + 4HCl + 2H2SO4 (3分)
解析試題分析:(1)電解精煉粗銅時,粗銅中的Cu和少量Zn在陽極發生氧化反應,Zn比Cu活潑,先失電子,所以陽極電極反應式為Zn-2e-=Zn2+ Cu-2e-=Cu2+
(2)①TeO2是兩性氧化物,與氫氧化鈉發生類似氧化鋁與氫氧化鈉的反應,化學方程式為TeO2+2NaOH=Na2TeO3+H2O;
②因為TeO2是兩性氧化物,H2SO4過量會導致TeO2繼續與H2SO4反應導致損失。防止局部酸度過大的操作方法是緩慢加入H2SO4,并不斷攪拌;
③SO2還原TeCl4為Te,本身被氧化為硫酸,化學方程式為TeCl4+2SO2+4H2O=Te+4HCl+2H2SO4
考點:考查粗銅精煉的電解反應式的書寫,對給定條件的化學方程式的判斷及書寫,實驗操作的判斷


科目:高中化學 來源: 題型:單選題
(12分)工業以CH3OH與NaClO3為原料在酸性條件下制取ClO2,同時產生CO2氣體,已知該反應分為兩步進行,第一步為2ClO3- + 2Cl- + 4H+ = 2ClO2↑+ Cl2↑+ 2H2O。
(1)寫出第二步反應的離子方程式 。
(2)工業生產時需在反應物中加少量Cl-,其作用是 。
(3)生產中會發生副反應ClO3- + Cl- + H+ - Cl2↑+ H2O(未配平),若測得反應后的混合氣體中Cl2的體積分數為3/73,則起始投料時CH3OH與NaClO3的物質的量之比為 。
(寫出解題過程)
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(10分)有三份不同質量的鐵粉樣品①②③,甲、乙、丙三位同學各取一份樣品分別與含有0.8molHNO3的稀硝酸反應,反應后硝酸和鐵均無剩余,且硝酸的還原產物只有NO。據此回答下列問題:
(1)甲取樣品①,反應后的溶液中鐵只以Fe3+離子的形式存在,則樣品①的質量為 g。
(2)乙取樣品②,反應后的溶液中既含有Fe3+、又含有Fe2+離子,則樣品②的質量(設為ag)范圍是 。
(3)丙取樣品③,將其慢慢加入到稀硝酸中,并不斷攪拌,反應過程中溶液里Fe3+、Fe2+、NO3—三種離子中的兩種離子的物質的量的變化曲線如下圖所示,則該曲線表示的是 物質的量變化的曲線,請你在此圖中再畫出另外種離子的物質的量的變化曲線。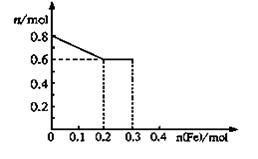
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
電解飽和食鹽水的反應為2NaCl+2H2O Cl2↑+H2↑+2NaOH。
Cl2↑+H2↑+2NaOH。
27. 在上述方程式上標出電子轉移的方向和數目。
28. 該反應中被氧化的元素是 。陰極產物之一為H2,陰極上發生的變化為 反應(選填“氧化”、“還原”)。
29. 電解產物氯氣既能作氧化劑,也能作還原劑。下列反應中氯氣只作氧化劑的是 (填寫編號)。
a.Cl2+2KI→2KCl+I2 b.Cl2 + 2NaOH →NaCl + NaClO + H2O
c.CuCl2 Cl2↑+ Cu d.3Cl2 + 2Fe
Cl2↑+ Cu d.3Cl2 + 2Fe 2FeCl3
2FeCl3
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
(15分)在航天發射時,肼(N2H4)及其衍生物常用作火箭推進劑。
⑴液態肼作火箭燃料時,與液態N2O4混合發生氧化還原反應,已知每1g肼充分反應后生成氣態水放出熱量為a KJ,試寫出該反應的熱化學方程式 。
⑵實驗室用N2H4·H2O與NaOH顆粒一起蒸餾,收集114~116℃的餾分即為無水肼。
①在蒸餾過程中不需要的儀器是 (填序號字母)。
| A.酒精燈 | B.長直玻璃導管 | C.錐形瓶 | D.直型冷凝管 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
A、B、X、Y、Z、W六種短周期主族元素,A是地殼中含量最多的金屬元素,短周期主族元素中B的原子半徑最大,X、Y、Z、W元素在周期表中的相對位置如下圖所示,其中Z元素原子最外層電子數是電子層數的2倍。請回答下列
問題: 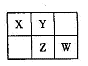
(1)W的最高價氧化物化學式是 ;Z的原子結構示意圖為 。
(2)A、B各自最高價氧化物對應的水化物反應的化學方程式為 。
(3)AW3可用于凈水,其原理是 。(請用離子方程式表示)
(4)工業合成X的簡單氣態氫化物是放熱反應。下列措施中既能提高
反應速率,又能提高原料轉化率的是 。
a.升高溫度
b.加入催化劑
c.將X的簡單氣態氫化物及時移離
d.增大反應體系的壓強
(5)標準狀況下,2.24L X的簡單氣態氫化物被200 mL l mol L-1X的最高價氧化物對應的水化物溶液吸收后,所得溶液中離子濃度從大到小的順序是(用離子符號表示) 。
(6)WY2在殺菌消毒的同時,可將劇毒氰化物氧化成無毒氣體而除去,寫出用WY2(沸點9.9℃)氧化除去CN-的離子方程式 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
臭氧是一種強氧化劑,常用于消毒、滅菌等。
(1)O3與KI溶液反應生成的兩種單質是________和________(填分子式)。
(2)O3在水中易分解,一定條件下,O3的濃度減少一半所需的時間(t)如下表所示。已知:O3的起始濃度為0.0216 mol/L。
①pH增大能加速O3分解,表明對O3分解起催化作用的是________。
②在30℃、pH=4.0條件下,O3的分解速率為________mol/(L·min)。
③據表中的遞變規律,推測O3在下列條件下分解速率依次增大的順序為________(填字母代號)。
a.40℃、pH=3.0 b.10℃、pH=4.0
c.30℃、pH=7.0
(3)O3可由臭氧發生器(原理如圖)電解稀硫酸制得。
①圖中陰極為________(填“A”或“B”),其電極反應式為_______________________。
②若C處通入O2,則A極的電極反應式為________。
③若C處不通入O2,D、E處分別收集到x L和y L氣體(標準狀況),則E處收集的氣體中O3所占的體積分數為________(忽略O3的分解)。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
在常見的非金屬及其化合物中:
(1)晶體硅的導電性介于導體和絕緣體之間,是良好的 材料;硅酸鈉水溶液俗稱為 ,是制備硅膠和木材防火劑的原料;陶瓷、 、水泥等硅酸鹽產品是使用量最大的無機非金屬材料。
(2)氯元素是重要的“成鹽元素”,將氯氣通入NaOH溶液中可以得到漂白液,反應的離子方程式是 ;漂白液有效成分的化學式為 。
(3)水是常見的非金屬元素化合物,請按要求寫出下列水參加的反應的化學方程式。
①水只作氧化劑:
②NO2氣體通入水中:
③水既作氧化劑又作還原劑:
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
氮氧化物是大氣污染物之一,消除氮氧化物的方法有多種。
(1)利用甲烷催化還原氮氧化物。已知:
CH4 (g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H =-574 kJ/mol
CH4(g)+4NO(g) = 2N2(g)+CO2(g)+2H2O(g) △H =-1160 kJ/mol
則CH4 將NO2 還原為N2 的熱化學方程式為 。
(2)利用NH3催化還原氮氧化物(SCR技術)。該技術是目前應用最廣泛的煙氣氮氧化物脫除技術。 反應的化學方程式為:2NH3(g)+NO(g)+NO2(g)  2N2(g)+3H2O(g) ΔH < 0
2N2(g)+3H2O(g) ΔH < 0
為提高氮氧化物的轉化率可采取的措施是 (寫出1條即可)。
(3)利用ClO2氧化氮氧化物。其轉化流程如下:
NO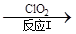 NO2
NO2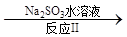 N2
N2
已知反應Ⅰ的化學方程式為2NO+ ClO2 + H2O = NO2 + HNO3 + HCl,則反應Ⅱ的化學方程式是 ;若生成11.2 L N2(標準狀況),則消耗ClO2 g 。
(4)利用CO催化還原氮氧化物也可以達到消除污染的目的。
已知質量一定時,增大固體催化劑的表面積可提高化學反應速率。如圖是反應2NO(g) + 2CO(g) 2CO2(g)+ N2(g) 中NO的濃度隨溫度(T)、等質量催化劑表面積(S)和時間(t)的變化曲線。據此判斷該反應的△H 0 (填“>”、“<”或“無法確定”);催化劑表面積S1 S2 (填“>”、“<”或“無法確定”)。
2CO2(g)+ N2(g) 中NO的濃度隨溫度(T)、等質量催化劑表面積(S)和時間(t)的變化曲線。據此判斷該反應的△H 0 (填“>”、“<”或“無法確定”);催化劑表面積S1 S2 (填“>”、“<”或“無法確定”)。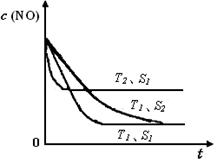
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com