(2010?浙江)甲醇是一種新型的汽車動力燃料,工業上可通過CO和H
2化合制備甲醇,該反應的熱化學方程式為:CO (g)+2H
2(g)?CH
3OH (g)△H
1(反應1)該反應的原料CO和H
2本身都可作為燃料提供動力,已知這兩種物質燃燒的熱化學方程式為:
CO(g)+O2(g)=CO2(g)△H
2=-283kJ?mol
-1(反應2)
H2(g)+O2(g)=H2O(g)△H
3=-242kJ?mol
-1(反應3)
某些化學鍵的鍵能數據如下表:
| 化學鍵 |
C-C |
C-H |
H-H |
C-O |
C≡O |
H-O |
| 鍵能/kJ?mol-1 |
348 |
413 |
436 |
358 |
1072 |
463 |
請回答下列問題:
(1)反應1的焓變△H
1=
-116kJ?mol-1
-116kJ?mol-1
.
(2)CH
3OH (g)燃燒生成CO
2(g)和H
2O(g)的熱化學方程式為:CH
3OH(g)+
O
2(g)═CO
2(g)+2H
2O(g)△H
4 該反應的焓變△H
4=
-651kJ?mol-1
-651kJ?mol-1
.與CO和H
2相比,甲醇作為汽車動力燃料的優點是
單位體積供能多,密度大易于運輸;單位產能耗氧量較少
單位體積供能多,密度大易于運輸;單位產能耗氧量較少
.
(3)反應1的平衡常數表達式為
.為提高甲醇的產率,可以采取的措施有
降低溫度、增加反應氣體的壓力、將反應生成的甲醇及時冷凝從反應體系中移去.
降低溫度、增加反應氣體的壓力、將反應生成的甲醇及時冷凝從反應體系中移去.
(寫出3點).既能提高產率,又能提高反應速率的措施是
增加反應氣體的壓強
增加反應氣體的壓強
.
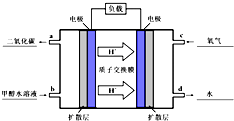
(4)甲醇-空氣燃料電池(DMFC)是一種高效能、輕污染電動汽車的車載電池,該燃料電池的電池反應式為:CH
3OH(l)+
O
2(g)═CO
2(g)+2H
2O(l).其工作原理如示意圖:

①在圖的橫線上標出a、b、c、d四個出入口通入或排出的物質名稱(或化學式)
②負極的電極反應式為
CH3OH+H2O-6e-=CO2+6H+
CH3OH+H2O-6e-=CO2+6H+
.