
【題目】中科院某課題組將二氧化錳和生物質置于一個由濾紙制成的折紙通道內形成電池(如圖所示),該電池可將可樂(pH=2.5)中的葡萄糖作為燃料獲得能量。下列說法中正確的是( )
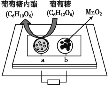
A. a極為正極
B. 隨著反應不斷進行,負極區的pH不斷增大
C. b極電極反應式為MnO2+2H2O+2e-=Mn2++4OH-
D. 消耗0.01mol葡萄糖,電路中轉移0.02mol電子
【答案】D
【解析】
A.失電子化合價升高的電極為負極,發生氧化反應;
B.負極區電極反應式為C6H12O6-2e-=C6H10O6+2H+,負極溶液中c(H+)增大;
C.b電極上二氧化錳得電子和氫離子反應生成水和Mn2+;
D.根據C6H12O6-2e-=C6H10O6+2H+計算轉移電子物質的量。
A.根據圖知,葡萄糖C6H12O6轉化為葡萄糖內脂C6H10O6,C元素化合價由0價轉化為+![]() ,則該電極上失電子發生氧化反應,所以a為負極,b為正極,A錯誤;
,則該電極上失電子發生氧化反應,所以a為負極,b為正極,A錯誤;
B.負極區電極反應式為C6H12O6-2e-=C6H10O6+2H+,負極溶液中c(H+)增大,則溶液的pH減小,B錯誤;
C.b電極上二氧化錳得電子和氫離子反應生成水和錳離子,電極反應式為MnO2+4H++2e-=Mn2++2H2O,C錯誤;
D.根據C6H12O6-2e-=C6H10O6+2H+可知,消耗1mol葡萄糖轉移2mol電子,則消耗0.01mol葡萄糖轉移0.02mol電子,D正確;
故合理選項是D。


 暑假作業海燕出版社系列答案
暑假作業海燕出版社系列答案 本土教輔贏在暑假高效假期總復習云南科技出版社系列答案
本土教輔贏在暑假高效假期總復習云南科技出版社系列答案 暑假作業北京藝術與科學電子出版社系列答案
暑假作業北京藝術與科學電子出版社系列答案科目:高中化學 來源: 題型:
【題目】t℃時,在體積不變的密閉容器中發生反應:X(g)+3Y(g)![]() 2Z(g),各組分在不同時刻的濃度如表,下列說法正確的是( )
2Z(g),各組分在不同時刻的濃度如表,下列說法正確的是( )
物質 | X | Y | Z |
初始濃度/mol/L | 0.1 | 0.2 | 0 |
2min末濃度/mol/L | 0.08 | a | b |
平衡濃度/mol/L | 0.05 | 0.05 | 0.1 |
A. 平衡時,X的轉化率為20% B. t℃時,該反應的平衡常數為40
C. 增大平衡后的體系壓強,v正增大,v逆減小,平衡向正反應方向移動 D. 前2min內,用Y的變化最表示的平均反應速率v(Y)=0.03mol/(L·min)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用X射線研究某金屬晶體,測得在邊長為360 pm的立方晶胞中含有4個金屬原子,此時金屬的密度為9.0 g/cm3。試回答下列問題:
(1)此金屬晶胞屬于哪一種類型?_______
(2)求每個晶胞的質量。_______
(3)求此金屬的相對原子質量。_______
(4)求此金屬原子的原子半徑(pm)。_______
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用酸性氫氧燃料電池為電源進行電解的實驗裝置如圖所示,下列說法正確的是( )
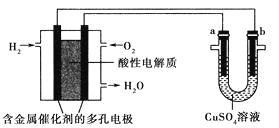
A. 燃料電池工作時,正極反應為O2+2H2O+4e-=4OH-
B. 電解精煉銅時,若轉移1mol電子,a極質量減少32g
C. 鐵表面鍍銅時,a為鐵,b為Cu,工作一段時間要使右池溶液復原可加入適量的CuO
D. 若a、b兩極均為石墨時,在相同條件下,a極產生的氣體與電池中消耗的O2體積相同
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】SCR和NSR技術可有效降低柴油發動機在空氣過量條件下的NOx排放。
(1)SCR(選擇性催化還原)工作原理:
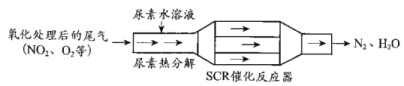
①尿素水溶液熱分解為NH3和CO2,該反應的化學方程式:___。
②反應器中NH3還原NO2的化學方程式:___。
③當燃油中含硫量較高時,尾氣中SO2在O2作用下會形成(NH4)2SO4,使催化劑中毒。用化學方程式表示(NH4)2SO4的形成:__。
④尿素溶液濃度影響NO2的轉化,測定溶液中尿素(M=60g·mol-1)含量的方法如下:取ag尿素溶液,將所含氮完全轉化為NH3,所得NH3用過量的v1mLc1mol·L-1H2SO4溶液吸收完全,剩余H2SO4用v2mLc2mol·L-1NaOH溶液恰好中和,則尿素溶液中溶質的質量分數是__。
(2)NSR(NOx儲存還原)工作原理:
NOx的儲存和還原在不同時段交替進行,如圖a所示。
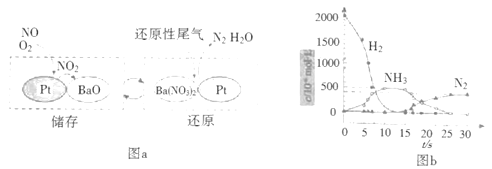
①通過BaO和Ba(NO3)2的相互轉化實現NOx的儲存和還原。儲存NOx的物質是__。
②用H2模擬尾氣中還原性氣體研究了Ba(NO3)2的催化還原過程,該過程分兩步進行,圖b表示該過程相關物質濃度隨時間的變化關系。第一步反應消耗的H2與Ba(NO3)2的物質的量之比是__。
③還原過程中,有時會產生笑氣(N2O)。用同位素示蹤法研究發現笑氣的產生與NO有關。在有氧條件下15NO與NH3以一定比例反應時,得到的笑氣幾乎都是15NNO。將該反應的化學方程式補充完整:___![]() □15NNO+□H2O___。
□15NNO+□H2O___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將 Na2CO3 和 Na2S 按 1∶2 的物質的量之比配成溶液,再通入 SO2,可制取 Na2S2O3,同時放出CO2。在該反應中( )
A.被氧化與被還原的原子個數比為 2∶1
B.相同條件下,每吸收 1 m3 SO2 就會放出 2.5 m3 CO2
C.每 1 mol Na2S 反應,則生成的 Na2S2O3 為 1.5 mol
D.若有 106 g Na2CO3 發生反應,反應中轉移的電子的物質的量為 4 mol
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溫度下,在固定容積的容器中,可逆反應A(g)+3B(g) ![]() 2C(g)達到平衡,此時測得n(A)∶n(B)∶n(C)=2∶2∶1。若保持溫度不變,以n(A)∶n(B)∶n(C)=2∶2∶1的比例向該容器中再充入A、B和C,下列敘述正確的是
2C(g)達到平衡,此時測得n(A)∶n(B)∶n(C)=2∶2∶1。若保持溫度不變,以n(A)∶n(B)∶n(C)=2∶2∶1的比例向該容器中再充入A、B和C,下列敘述正確的是
A. 剛充入時反應速率υ正減少,υ逆增大 B. 平衡不發生移動
C. 平衡向正反應方向移動,A的物質的量濃度減小 D. 物質C的質量分數增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上可用O2將HCl轉化為Cl2,反應為:O2(g)+4HCl(g)![]() 2Cl2(g)+2H2O(g)。請完成下列填空:
2Cl2(g)+2H2O(g)。請完成下列填空:
(1)該反應化學平衡常數K的表達式為_____________________;實驗測得P0壓強下,HCl平衡轉化率α(HCl)隨反應溫度T的變化如圖所示,則正反應是_________反應(填“吸熱”或者“放熱”)。
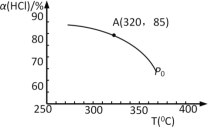
(2)寫出一種能提高HCl轉化率的方法___________________。
(3)上述實驗中若壓縮體積使壓強由P0增大至P1,在圖中畫出P1壓強下HCl平衡轉化率α(HCl)隨反應溫度T變化的曲線______,并簡要說明理由:_________________。
(4)根據圖中信息所示,在P0、320℃條件下進行,達平衡狀態A時,測得容器內n(Cl2)=7.2×10–3mol,則此時容器中n(HCl)=_____mol。
(5)氯元素能組成多種化合物,如常見的銨態氮肥,氯化銨溶液呈______性,其原因用離子方程式表示:___________________________。現有一瓶氯化銨、氯化鈉和氨水的混合液,經測定溶液呈中性,此時三種離子的關系是:[Na+]+[NH4+]_____[Cl-](填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(鋁用途廣泛,用鋁土礦(主要成分為Al2O3·nH2O、少量SiO2和Fe2O3)制取Al有如下途徑:
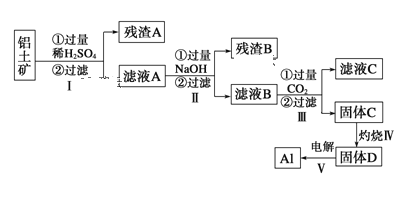
(1)濾液A加過量NaOH離子方程式表示為______________________________
(2)灼燒時盛放藥品的儀器名稱是_______
(3)步驟Ⅳ中發生反應的化學方程式是___________________________________
(4)步驟Ⅲ中生成固體C的離子反應方程式為_____________________________
(5)取濾液B 100mL,加入1 mol/L鹽酸200 mL,沉淀量達到最大且質量為11.7g,則濾液B中c(AlO2-)____mol/L,c(Na+)____6.5 mol/L (填“大于”、“小于”或“等于”)
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com