


分析 根據原子的最外層電子數與原子序數的關系,很容易推測出標號1至10依次是碳、氮、氧、氟、氖、鈉、鋁、硅、硫、氯元素,離子化合電子式書寫,同周期原子半徑的遞變規律,氫鍵對熔沸點的影響及離子方程式的書寫規律來解答.
解答 解:(1)圖中5號原子的最外層是8個電子,是氖元素,答案:Ne;
(2)圖中3號元素為氧元素,6號元素為鈉元素,形成原子數比為2:1的化合物為Na2O,故答案為:Na2O的電子式為 ;
;
(3)鋁、硅為同周期元素,隨核電數的遞增原子半徑逐漸減小,即原子半徑Al>Si,碳和硅為同一主族元素,核電荷數越大原子半徑越大,即原子半徑Si>C,故答案為:Al>Si>C;
(4)氧、氟、硫、氯四各元素形成的氣態氫化物分別為H2O、HF、H2S、HCl,因H2O和HF均存在分子間氫鍵,且H2O常溫下為液態可知H2O的沸點最高,答案:H2O;
(5)6號元素鈉的最高價氧化物的水化物為NaOH,7號元素鋁的最高價氧化物的水化物為Al(OH)3,二者之間反應的離子方程式為Al(OH)3+OH-═AlO2-+2H2O,故答案為:Al(OH)3+OH-═AlO2-+2H2O.
點評 本題考查元素周期律和元素周期表,明確常見主族元素的性質是解答的關鍵,注重基礎,對短周期元素不熟悉就可能做錯,但難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 化學危險品危害人類健康,應禁止生產 | |
| B. | 硝酸鉀呈中性,與氫化鈉一起儲存不存在危險 | |
| C. | 氰化氫、氰化鈉均為劇毒,受氰化鈉污染的土壤可用雙氧水氧化,為增強效果可先用硫酸酸化 | |
| D. | 這些化學品燃燒產生的火焰不能用水直接撲滅,只能通過用沙土覆蓋隔絕燃燒環境 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 土豪,原指地方上有錢有勢的家族或個人、鄉村中有錢的惡霸等,2013年土豪一詞專指網絡上無腦消費的人而成為流行語,將有望在2014年加入牛津詞典.下圖是土豪一詞的拼音縮寫,類似于某種有機物分子的鍵線式,若圖中的線段可以表示單鍵或雙鍵,請回答下列問題:
土豪,原指地方上有錢有勢的家族或個人、鄉村中有錢的惡霸等,2013年土豪一詞專指網絡上無腦消費的人而成為流行語,將有望在2014年加入牛津詞典.下圖是土豪一詞的拼音縮寫,類似于某種有機物分子的鍵線式,若圖中的線段可以表示單鍵或雙鍵,請回答下列問題:
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 結構示意圖 ,可以表示一種原子,也可以表示一種離子 ,可以表示一種原子,也可以表示一種離子 | |
| B. | 比例模型 可以表示二氧化碳分子,也可以表示二硫化碳分子分子 可以表示二氧化碳分子,也可以表示二硫化碳分子分子 | |
| C. | 電子式 可以表示羥基,也可以表示氫氧根離子 可以表示羥基,也可以表示氫氧根離子 | |
| D. | 分子式C2H4O2:可以表示乙酸,也可以表示甲酸甲酯 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等體積等濃度的Na2S溶液和Na2SO3溶液中,離子數目以前者為多 | |
| B. | 已知室溫時0.10mol/L NH4Cl溶液中c(H+)=7.5×10-6mol/L,室溫時0.10mol/L KCN溶液中c (OH-)=1.3×10-3mol/L.那么此時0.10mol/L NH4CN溶液中pH>7 | |
| C. | 等pH、等體積的醋酸和硫酸,分別與足量的碳酸氫鈉反應,在相同條件下,硫酸放出氣體更多 | |
| D. | 醋酸加到氫氧化鈉溶液中,若要使所得溶液呈中性,醋酸應稍過量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 核素就是同位素 | |
| B. | 元素的金屬性強弱與元素失去電子數的多少成正比 | |
| C. | 具有相同質子數的微粒一定是同一種元素 | |
| D. | 核內中子數為N的R2+,質量數為A,則該離子的核外電子數為A-N-2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
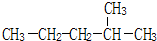 2-甲基戊烷
2-甲基戊烷 2,3-二甲基-1-丁烯
2,3-二甲基-1-丁烯 1,2-二溴乙烷
1,2-二溴乙烷 乙苯
乙苯查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com