
某同學需要用到120 mL 1 mol/L的鹽酸溶液,現用密度為1.18 g/mL,質量分數為36.5%濃鹽酸配制,填空并請回答下列問題:
(1)配制1 mol/L的鹽酸溶液
量筒量取濃鹽酸體積/mL | 應選用量筒的規格(可供選擇的規格10 mL、25 mL、50 mL) | 應選用容量瓶的規格(可供選擇的規格100 mL、250 mL、500 mL) | 除容量瓶外還需要的其它儀器 |
① | ② | ③ | ④ |
(2)配制時,其正確的操作順序是(字母表示,每個字母只能用一次) __ _____;
A、用30 mL水洗滌燒杯內壁和玻璃棒2—3次,洗滌液均注入容量瓶,振蕩
B、用量筒準確量取所需的濃鹽酸的體積,將量好的濃鹽酸倒入燒杯中,再加入少量水(約30 mL),用玻璃棒慢慢攪動,使其混合均勻
C、將已冷卻的鹽酸沿玻璃棒注入容量瓶中
D、將容量瓶蓋緊,振蕩,搖勻
E、繼續往容量瓶內小心加水,直到溶液凹面恰好與刻度相切
(3)指出本實驗的操作錯誤的地方,并進行更正 。
(4)若出現如下情況,對所配溶液濃度將有何影響(填“偏高”、“偏低”或“無影響”):
①所用的濃鹽酸長時間放置在密封不好的容器中 ;
②若加蒸餾水時不慎超過了刻度 ;
③若定容時俯視刻度線___________________;
④用量筒量取濃鹽酸時仰視 ;
 名師伴你成長課時同步學練測系列答案
名師伴你成長課時同步學練測系列答案科目:高中化學 來源:2016屆河南省高三第四次大考化學試卷(解析版) 題型:選擇題
若30g密度為d g/mL的AlCl3的溶液中含有0.9g Al3+(不考慮Al3+與水反應),則Cl-濃度為
A.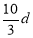 mol/L B.
mol/L B.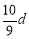 mol/L C.
mol/L C.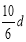 mol/L D.
mol/L D.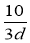 mol/L
mol/L
查看答案和解析>>
科目:高中化學 來源:2016屆河南省洛陽市高三上學期期中考試化學試卷(解析版) 題型:選擇題
過氧化鉀與水的反應類似于過氧化鈉與水的反應,其化學方程式為:2K2O2十2H2O=4KOH十O2↑,當0.5 mol K18O2與足量H2O完全反應后,下表對生成物O2的敘述中錯誤的是
K218O2的質量 | O2的敘述 | |
A | 57g | O2的質量是9g |
B | 57g | 生成標準狀況下O2的體積為5.6L |
C | 57g | O2的摩爾質量是32g•mol-1 |
D | 57g | 生成0.25mol O2 |
查看答案和解析>>
科目:高中化學 來源:2016屆廣東省粵西“四校”高三上學期第一次聯考化學試卷(解析版) 題型:選擇題
銅鋅原電池(如圖)工作時,下列敘述正確的是
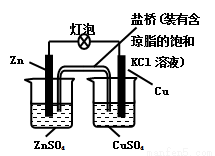
A.一段時間后,銅棒上有紅色物質析出
B.正極反應為:Zn-2e-=Zn2+
C.在外電路中,電流從負極流向正極
D.鹽橋中的K+移向ZnSO4溶液
查看答案和解析>>
科目:高中化學 來源:2016屆安徽省天長市高三第一次月考化學試卷(解析版) 題型:選擇題
讀下列藥品標簽,有關分析不正確的是
選項 | A | B | C | D |
物品 標簽 | 飽和氯水 1.01×105 Pa 20 ℃ | 藥品:×××
| 碳酸氫鈉 NaHCO3 俗名 小蘇打 (84 g/mol) | 濃硫酸 H2SO4 密度 1.84 g/mL 濃度98.0% |
分析 | 該試劑應裝在玻璃塞的棕色細口瓶中 | 該藥品不能與皮膚直接接觸 | 該物質受熱易分解 | 該物質濃度為9.6 mol/L |
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省高一上學期第一次月考化學試卷(解析版) 題型:選擇題
鈉塊長時間暴露在空氣中的最終產物為
A.Na2O B.NaOH C.Na2CO3 D.Na2O2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年吉林省扶余市高一上學期第一次月考化學試卷(解析版) 題型:選擇題
欲配制100ml 1.0 mol/L Na2SO4溶液,正確的方法是
①將32.2g Na2SO4·10H2O溶于少量水中,再用水稀釋至100 ml
②將14.2 g Na2SO4 溶于100ml水中制成溶液
③將20 ml 5.0 mol/L Na2SO4溶液用水稀釋至100 ml
A.①② B.①②③
C.①③ D.②③
查看答案和解析>>
科目:高中化學 來源:2016屆四川省高三9月月考化學試卷(解析版) 題型:填空題
(10分)過氧化氫(H2O2)的水溶液俗稱雙氧水,近年來倍受人們的青睞,被稱為“綠色氧化劑”。
(1)寫出H2O2的電子式 。
(2)你認為H2O2被稱為“綠色氧化劑”的主要原因是 。
(3)將雙氧水加入用鹽酸酸化的FeCl2溶液中,溶液由淺綠色變為棕黃色,寫出該反應的離子方程式為 ,反應中H2O2作 劑。
(4)雙氧水能使酸性高錳酸鉀溶液褪色,其反應的離子方程式如下,請將相關物質的化學計量數及化學式填寫在方框里: MnO4﹣+ H2O2+ H+═ Mn2++ H2O+ 。
查看答案和解析>>
科目:高中化學 來源:2016屆湖南省高三9月月考試化學試卷(解析版) 題型:實驗題
(14分)某研究性實驗小組欲驗證濃硝酸在與Cu、Ag合金的反應過程中除生成NO2氣體外,還會有少量NO生成、并測定Cu、Ag合金中Cu的質量分數.查閱相關資料表明:“常溫下,NO2與N2O4混合存在,在低于0℃時幾乎只有無色的N2O4液體或晶體存在.”為此,他們設計了如圖所示的裝置.
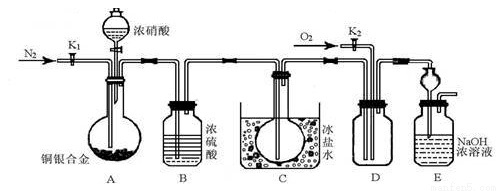
請回答下列問題
(1)寫出A中Cu與HNO3反應可能的化學方式 .
(2)實驗開始前先打開A部分的活塞K1,持續通入一段時間的氮氣再關閉K1,其目的是 ;裝置中B瓶的作用是 .
(3)停止反應后,打開D中的活塞K2并通入O2,若有NO生成,則D中出現的現象是 ;實驗發現,通入的O2溫度高低對實驗現象有較大影響,為便于觀察應通入(填“熱”或“冷”) 的O2.
(4)為減小實驗誤差,在A中反應完成和D中出現現象后,還應繼續進行的操作是 .
(5)實驗測得如下數據:實驗前,Cu、Ag合金的質量:15.0g,濃HNO3:40mL 13.5mol•L﹣1;實驗后A溶液:V=40mL c(H+)=1.0mol•L﹣1.假設反應中HNO3既無揮發也無分解,則:
①參加反應的HNO3的物質的量為 mol.
②若已測出反應后E裝置的生成物中含氮元素的質量,則為確定合金中Cu的質量分數還需測定的數據是 .
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com