
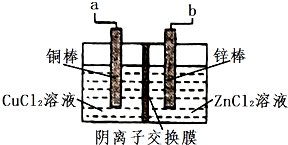
 一種使用陰離子交換膜(只也許陰離子通過)的銅鋅電池結構結構如圖,如表選項兩欄內容正確且相關聯的是( )
一種使用陰離子交換膜(只也許陰離子通過)的銅鋅電池結構結構如圖,如表選項兩欄內容正確且相關聯的是( )| 選項 | 操作與現象 | 解釋與推論 |
| A | 電池放電時化學能轉化為電能 | Zn(s)+Cu2+(aq)=Zn2++Cu(s)△H>0 |
| B | 該電池充電時銅棒變細 | 兩電極區溶液顏色都變深 |
| C | 該電池放電時銅棒是電池正極 | Cl-通過交換膜從左(銅棒區)向右(鋅棒區)移動 |
| D | 該電池充電時a接電源正極 | 電極反應Cu2++2e-=Cu |
| A. | A | B. | B | C. | C | D. | D |
分析 A、氧化反應:Zn-2e-═Zn2+,還原反應:Cu2++2e-═Cu,在原電池中,一般是負極與電解質溶液發生自發進行的氧化還原反應.負極Zn失去電子發生氧化反應,Cu2+在正極上得電子發生還原反應;
B、電池充電時銅棒電極反應式為:Cu-2e-=Cu2+,所以銅應變細,而陰極區是鋅離子放電生成單質鋅,陰極區溶液的顏色沒有明顯的變化;
C、Cu2+在正極上得電子發生還原反應,陰離子氯離子可以自由能通過,氯離子向負極移動;
D、充電時a接電源正極,a為陽極發生氧化反應,電極反應式為:Cu-2e-=Cu2+.
解答 解:A、電池放電時是將化學能轉化為電能,鋅與銅離子能自發的氧化還原反應,所以能構成原電池,故A正確;
B、電池充電時銅棒電極反應式為:Cu-2e-=Cu2+,陽極區溶液顏色變深,而陰極區是鋅離子放電生成單質鋅,陰極區溶液的顏色沒有明顯的變化,故B錯誤;
C、Cu2+在正極上得電子發生還原反應,陰離子氯離子可以自由能通過,氯離子向負極移動,即Cl-通過交換膜從左(銅棒區)向右(鋅棒區)移動,故C正確;
D、充電時a接電源正極,a為陽極發生氧化反應,電極反應式為:Cu-2e-=Cu2+,故D錯誤;
故選AC.
點評 本題考查可充可放電池設計,側重考查學生實驗設計、實驗操作能力,明確電池工作原理是解本題關鍵,原電池反應式中失電子化合價升高的金屬作負極,得電子發生還原反應的電解質為原電池電解質.


 特高級教師點撥系列答案
特高級教師點撥系列答案科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1MgCl2溶液中含有的Mg2+數目一定小于0.1NA | |
| B. | 標準狀況下,11.2 L CCl4中含有的分子數目為0.5NA | |
| C. | 28 g聚乙烯中含有的碳原子數目為2NA | |
| D. | 1 mol C${{H}_{5}}^{+}$中含有的電子數目為11NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol FeI2與足量氯氣反應時轉移的電子數為2NA | |
| B. | 1 L 1mol/L的鹽酸含有NA個HCl分子 | |
| C. | 標準狀況下,33.6 L四氯化碳中含有氯原子的數目為6NA | |
| D. | 5NH4NO3$\frac{\underline{\;\;△\;\;}}{\;}$2HNO3+4N2↑+9H2O反應中,生成28 g N2時,轉移的電子數目為3.75NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 0.1 mol•L-1NaHCO3溶液與0.1 mol•L-1NaOH溶液等體積混合:c(Na+)=2c(CO32-)+c(HCO3-)+2c(H2CO3) | |
| C. | 0.1 mol•L-1NaHCO3溶液與0.2 mol•L-1NaOH溶液等體積混合:c(Na+)>c(OH-)>0.05 mol•L-1>c(CO32-)>c(HCO3-) | |
| D. | 0.2 mol•L-1NaHCO3溶液與0.1 mol•L-1NaOH溶液等體積混合:c(CO32-)+c(OH-)=c(HCO3-)+3c(H2CO3)+2c(H+) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應屬加成反應 | B. | 乙烯可以通過石油裂解獲得 | ||
| C. | 乙醇官能團為羥基 | D. | 乙醇、乙醛和乙酸互為同系物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在溴富集過程中,可在分液漏斗中加入1mL溴水,再向其中加入3mL四氯化碳,振蕩,靜置,分液,得到下層液體 | |
| B. | 用鉑絲蘸取少量某溶液進行焰色反應,火焰呈黃色,該溶液一定是鈉鹽溶液 | |
| C. | 通常用產生氣泡的快慢,比較不同條件下Na2S2O3溶液與稀硫酸反應速率 | |
| D. | 用pH計分別測定0.1mol/L的FeCl3和0.01mol/L的FeCl3的pH,可以比較濃度對鹽類水解程度的影響 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
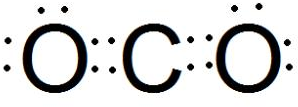 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 甲烷與氯氣混合后光照反應;乙烯使酸性高錳酸鉀溶液褪色 | |
| B. | 乙烯與溴的四氯化碳溶液反應;苯與氫氣在一定條件下反應生成環己烷 | |
| C. | 苯滴入濃硝酸和濃硫酸的混合液中,有油狀物生成; 乙烯與水生成乙醇的反應 | |
| D. | 在苯中滴入溴水,溴水褪色;乙烯自身生成聚乙烯的反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
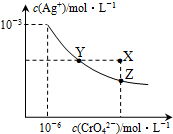 t℃時,AgCl的Ksp=2×10-10;Ag2CrO4是一種橙紅色固體,在水中的沉淀溶解平衡曲線如圖所示.下列說法正確的是( )
t℃時,AgCl的Ksp=2×10-10;Ag2CrO4是一種橙紅色固體,在水中的沉淀溶解平衡曲線如圖所示.下列說法正確的是( )| A. | 在t℃時,AgCl的溶解度大于Ag2CrO4 | |
| B. | 在t℃時,Ag2CrO4的Ksp=1×10-12 | |
| C. | 在飽和Ag2CrO4溶液中加入K2CrO4,可使溶液由Y點到X點 | |
| D. | 在t℃時,用AgNO3標準溶液滴定20mL未知濃度的KCl溶液,不能采用K2CrO4溶液為指示劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com