
【題目】A、B、C、D、E、F六種元素均位于周期表的前四周期,且原子序數依次增大。元素A是原子半徑最小的元素;B元素基態原子的核外電子分占四個原子軌道;D元素原子的已成對電子總數是未成對電子總數的3倍;E與D處于同一主族;F位于ds區,且原子的最外層只有1個電子。
⑴F+離子的電子排布式是______。
⑵B、C、D元素的第一電離能由大到小的順序是______。
⑶B、C元素的某些氫化物的分子中均含有18個電子,則B的這種氫化物的化學式是______;B、C的這些氫化物的沸點相差較大的主要原因是______。
⑷A、B、D可形成分子式為A2BD的某化合物,則該化合物分子中B原子的軌道雜化類型是______;1mol該分子中含有![]() 鍵的數目是______。
鍵的數目是______。
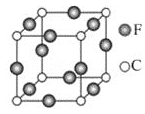
⑸C、F兩元素形成的某化合物的晶胞結構如圖所示,則該化合物的化學式是______,C原子的配位數是______。
【答案】1s22s22p63s23p63d10或[Ar]3d10 N > O > C C2H6 氮的氫化物(N2H4)分子間存在氫鍵 sp2 NA Cu3N 6
【解析】
A、B、C、D、E、F六種元素均位于周期表的前四周期,且原子序數依次增大;元素A是原子半徑最小的元素,則A是H元素;B元素基態原子的核外電子分占四個原子軌道,則B為C元素;D元素原子的已成對電子總數是未成對電子總數的3倍,則D是O元素,C元素原子序數大于B而小于D,則C是N元素;E與D處于同一主族,則E是S元素;F位于ds區,且原子的最外層只有1個電子,則F為Cu元素;
⑴Cu+是Cu原子失去最外層電子得到的離子,其離子核外有28個電子,根據構造原理書寫亞銅離子核外電子排布式為1s22s22p63s23p63d10或[Ar]3d10,故答案為:1s22s22p63s23p63d10或[Ar]3d10;
⑵B、C、D分別是C、N、O元素,且位于同一周期,同一周期元素第一電離能隨著原子序數增大而呈增大趨勢,但第IIA族、第VA族元素第一電離能大于其相鄰元素,所以這三種元素第一電離能大小順序是N > O > C,故答案為:N > O > C;
⑶C、N元素的某些氫化物的分子中均含有18個電子,則B的這種氫化物為C2H6;含有氫鍵的氫化物熔沸點較高,N2H4中含有氫鍵而C2H6中不含氫鍵,所以氮的氫化物熔沸點較高,故答案為:C2H6;氮的氫化物N2H4分子間存在氫鍵;
⑷H、C、O可形成分子式為H2CO的某化合物,為HCHO,該分子中C原子價層電子對個數是3且不含孤電子對,根據價層電子對互斥理論判斷C原子雜化方式為sp2;一個甲醛分子中含有1個π鍵,則1mol甲醛中含有1molπ鍵,數目為NA,故答案為:sp2;NA。
⑸N、Cu兩元素形成的某化合物的晶胞結構如圖所示,該晶胞中Cu原子個數![]() 、N原子個數
、N原子個數![]() ,所以其化學式為Cu3N;該晶胞中N原子配位數為6,故答案為:Cu3N;6。
,所以其化學式為Cu3N;該晶胞中N原子配位數為6,故答案為:Cu3N;6。


科目:高中化學 來源: 題型:
【題目】下列實驗操作能達到相應實驗目的的是
選項 | 實驗目的 | 實驗操作 |
A | 探究I-與Fe2+的還原性強弱 | 向FeCl3稀溶液中依次加入KI溶液、淀粉 |
B | 探究HPO42-在水溶液中的電離程度與水解程度的相對大小 | 測定0.1 mol·L-1NaH2PO4溶液的pH |
C | 配制0.1 mol·L-1鄰苯二甲酸氫鉀( | 稱取5.1 g鄰苯二甲酸氫鉀于燒杯中,加入少量蒸餾水溶解,轉移至500 mL容量瓶中定容 |
D | 比較CaCO3和CaSO4的Ksp大小 | 向澄清石灰水中滴入0.1 mol·L-1Na2CO3溶液至不再有沉淀產生,再滴加0.1 mol·L-1Na2SO4溶液 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學反應A(g)+3B(g)![]() 2C(g)+2D(g),在下列四個選項中是不同的情況下測得的不同物質的反應速率,其中表示該化學反應的反應速率最慢的是( )
2C(g)+2D(g),在下列四個選項中是不同的情況下測得的不同物質的反應速率,其中表示該化學反應的反應速率最慢的是( )
A.v(A)=0.20 mol·(L·min)-1B.v(B)=0.45 mol·(L·s)-1
C.v(C)=0.30 mol·(L·min)-1D.v(D)=0.35 mol·(L·min)-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】溫度為T時,向2.0 L恒容密閉容器中充入1.0 mol PCl5,發生反應:PCl5(g)![]() PCl3(g)+Cl2(g) ΔH=a kJ·mol-1(a>0)。0~10 min保持容器溫度不變,10 min時改變一種條件,整個過程中PCl5、PCl3、Cl2的物質的量隨時間的變化如圖所示。
PCl3(g)+Cl2(g) ΔH=a kJ·mol-1(a>0)。0~10 min保持容器溫度不變,10 min時改變一種條件,整個過程中PCl5、PCl3、Cl2的物質的量隨時間的變化如圖所示。

下列說法正確的是
A.0~4 min的平均速率v(PCl3)=0.025 mol·L-1·min-1
B.10 min時改變的條件是增加了一定量的PCl5
C.若起始時向該容器中充入2.0 mol PCl3和2.0 mol Cl2,保持溫度為T,反應達平衡時放出的熱量小于1.6a kJ
D.溫度為T,起始時向該容器中充入1.0 mol PCl5、0.10 mol PCl3和0.10 mol Cl2,反應達到平衡前v正<v逆
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學興趣小組在實驗室探究過渡金屬元素化合物的性質
I、鐵及其化合物

(1)向FeSO4溶液中滴加NaOH溶液,產生白色沉淀,但迅速變為灰綠色,最終變為紅褐色,為順利看到較長時間的白色沉淀,設計了圖①裝置:①檢查裝置氣密性,裝入藥品;②打開止水夾K;③在試管b出口收集氣體并驗純;④關閉止水夾K。以上操作正確的順序是:___。
(2)某實驗小組稱量3.60 g草酸亞鐵晶體(FeC2O4·2H2O)加熱過程中,固體質量變化如圖②所示:
①請寫出AB段發生反應的化學方程式:___。②C點成分為:___。
(3)向FeCl3溶液中加入過量Na2SO3溶液,設計實驗證明兩者發生了氧化還原反應并且為可逆反應。(簡要說明實驗步驟、現象和結論,儀器和藥品自選)___。
II、銅及其化合物
向2ml0.2mol·L-1Na2SO3溶液中滴加0.2mol·L-1CuSO4溶液,發現溶液變綠,繼續滴加產生棕黃色沉淀,經檢驗,棕黃色沉淀中不含SO42-,含有Cu+、Cu2+和SO32-。
已知:Cu+![]() Cu+Cu2+,Cu2+
Cu+Cu2+,Cu2+![]() CuI↓(白色)+I2。
CuI↓(白色)+I2。
(4)用稀硫酸證實沉淀中含有Cu+的實驗現象是___。
(5)向洗凈的棕黃色沉淀中加入足量KI溶液,產生白色沉淀,繼續向上層清液中加入淀粉溶液并沒有變藍的現象出現,請結合離子反應方程式解釋不變藍的原因___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】到目前為止,由化學能轉變的熱能或電能仍然是人類使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃燒生成CO2和液態水時放出352kJ的熱量,則表示甲醇燃燒熱的熱化學方程式為______。
(2)化學反應中放出的熱能(焓變,△H)與反應物和生成物的鍵能(E)有關。已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,E(H﹣Cl)=432kJ/mol,E(Cl﹣Cl)=243kJ/mol則E(H﹣H)=_____。
(3)納米級Cu2O由于具有優良的催化性能而受到關注.已知:2Cu(s)+ ![]() O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+
O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,則工業上用炭粉在高溫條件下還原CuO制取Cu2O和CO的熱化學方程式_____。
O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,則工業上用炭粉在高溫條件下還原CuO制取Cu2O和CO的熱化學方程式_____。
(4)如圖是N2(g)和H2(g)反應生成2molNH3(g)過程中能量變化示意圖:
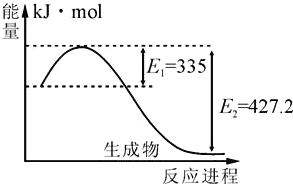
①請計算每生成1molNH3放出熱量為:______。
②若起始時向容器內充入1molN2和3molH2達平衡后N2的轉化率為20%,則反應放出的熱量為Q1kJ,則Q1的數值為_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】水資源非常重要,聯合國確定2003年為國際淡水年.海水淡化是海島地區提供淡水的重要手段,所謂海水淡化是指除去海水中的鹽分以獲得淡水的工藝過程![]() 又稱海水脫鹽
又稱海水脫鹽![]() ,其方法較多,如反滲透法、水合物法、電滲透法、離子交換法和壓滲法等.下列方法中也可以用來進行海水淡化的是
,其方法較多,如反滲透法、水合物法、電滲透法、離子交換法和壓滲法等.下列方法中也可以用來進行海水淡化的是
A.過濾法B.蒸餾法C.萃取法D.蒸發法
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖,某氣體X可能由H2、CO、CH4中的一種或幾種組成。將X氣體燃燒,把燃燒后生成的氣體通過A、B兩個洗氣瓶。試回答下列問題:

(1)若A洗氣瓶的質量增加,B洗氣瓶的質量不變,則氣體X是____________。
(2)若A洗氣瓶的質量不變,B洗氣瓶的質量增加,則氣體X是____________。
(3)若A、B兩個洗氣瓶的質量都增加,則氣體X可能是____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一定條件下,二氧化硫和氧氣發生如下反應:2SO2(g)+O2(g)2SO3(g) △H<0;
(1)寫出該反應的化學平衡常數表達式K=__________
(2)降低溫度,該反應K值__________,二氧化硫轉化率___________,化學反應速率___________(以上均填增大、減小或不變)。
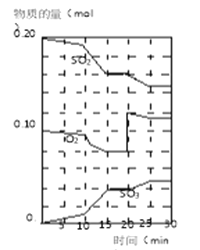
(3)600℃時,在一密閉容器中,將二氧化硫和氧氣混合,反應過程中SO2、O2、SO3物質的量變化如圖,反應處于平衡狀態時間是___________________________。
(4)據圖判斷,反應進行至20min時,曲線發生變化的原因是_______________________(用文字表達)。
(5)10min到15min的曲線變化的原因可能是____________(填寫編號)。
A、加了催化劑 B、縮小容器體積
C、降低溫度 D、增加SO3的物質的量。
(6)若該反應的密閉容器為2L,則反應15min時,v(SO2)=___________
(7)為使該反應的反應速率增大,且平衡向正反應方向移動的是(____)
A、及時分離出SO3氣體B、適當升高溫度
C、增大O2的濃度 D、選擇高效的催化劑
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com