
已知,鐵有α、γ、δ三種晶體結構,并且在一定條件下可以相互轉化(如圖),請回答相關的問題:
α-Fe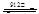 γ-Fe
γ-Fe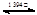 δ-Fe
δ-Fe
(1)鐵的三種晶體之間的轉化屬于 變化(填“物理”或“化學”),理由是: 。
(2)鐵的α、γ、δ三種晶體結構中,Fe原子的配位數之比為: 。
(3)設α-Fe晶胞邊長為a cm,δ-Fe晶胞邊長為b cm,計算確定:
兩種晶體的密度比為: 。(用a、b的代數式表示)
(4)Fe3C是工業煉鐵生產過程中產生的一種鐵的合金,在Fe3C晶體中,每個碳原子被6個位于頂角位置的鐵原子所包圍,成八面體結構,即碳原子配位數為6,那么,鐵原子配位數為 。
事實上,Fe3C是C與鐵的晶體在高溫下形成的間隙化合物(即碳原子填入鐵晶體中的某些空隙),根據相關信息,你認為形成碳化鐵的鐵的三種晶體結構中,最有可能的是: 。(選填“α-Fe”、“γ-Fe”或“δ-Fe”)
(1)物理 金屬鍵沒有變化(或“沒有化學鍵變化”;“沒有新物質生成”)
(2)2∶4∶1 (3)2b3∶a3 (4)2 γ-Fe
【解析】
試題分析:(1)鐵的三種晶體之間的轉化過程中并沒有新的物質生成,屬于物理變化。
(2)根據晶胞的結構可知,三種晶體中含有的鐵原子數分別是8×1/8+1=2、8×1/8+6×1/2=4、8×1/8=1,所以鐵的α、γ、δ三種晶體結構中,Fe原子的配位數之比為2∶4∶1。
(3)根據(2)可知, 、
、 ,所以兩種晶體的密度比為2b3∶a3。
,所以兩種晶體的密度比為2b3∶a3。
(4)每個碳原子被6個位于頂角位置的鐵原子所包圍,構成八面體結構,每個鐵原子又為兩個八面體共用,即碳原子配位數為6,鐵原子配位數為2;由于每個碳原子被6個位于頂角位置的鐵原子所包圍,成八面體結構,所以符合該結構的應該是γ-Fe。
考點:考查金屬晶體的有關判斷和計算
點評:由于描述晶體結構的基本單元叫做晶胞,所以在計算晶體中原子個數時,應該利用數學知識立體幾何,學會類推,要求學生樹立物體的空間感,然后靈活運用即可。


 小學課時作業全通練案系列答案
小學課時作業全通練案系列答案 金版課堂課時訓練系列答案
金版課堂課時訓練系列答案科目:高中化學 來源:2012-2013學年河南省周口市中英文學校高一下學期第三次月考化學卷(帶解析) 題型:填空題
(1)下列操作錯誤的是_________(填序號)
A. 用蒸發皿進行加熱蒸發實驗時,不墊石棉網。
B. 濃硫酸不慎沾到皮膚上,迅速用NaOH溶液清洗,再用水洗。
C. 聞氣體氣味時,用手在容器口輕輕扇動,使少量氣體飄入鼻孔中。
D. 使用分液漏斗和容量瓶時,首先檢查是否漏液。
E.做實驗時,剩余試劑一律不能放回原試劑瓶。
(2) 最近媒體報道了多起衛生間清洗時,因混合使用“潔廁靈”(主要成分是鹽酸)與“84消毒液”(有效成分是NaClO)發生氯氣中毒的事件。根據你所學的氧化還原反應知識,用離子方程式表示產生氯氣的原因: 。
(3) 已知向四羥基鋁酸鈉溶液中加入稀鹽酸有氫氧化鋁生成。某同學根據所學知識,提出不能使用該方法制取A1(OH)3,理由為 。(用離子方程式表示)
請你另舉出一種用氯化鋁溶液制取A1(OH)3的合理方法,該反應的離子方程式為 。
(4)據有關報道。目前已能冶煉出純度高達99.9999%的鐵,下列關于純鐵的敘述中,正確的是 (填字母)。
A.硬度比鋼小,熔點比鋼高 B.不能與鹽酸反應
C.與不銹鋼成分相同 D.在冷的濃硫酸中鈍化
(5)向沸水中逐滴滴加飽和FeCl3溶液,至液體呈透明的紅褐色時停止加熱,所得分散系的分散質大小范圍是 。
(6)合成氨工業生產中常用鐵觸媒做催化劑,其主要成分是FeO、Fe2O3。已知某鐵觸媒中,鐵、氧離子的物質的量之比為4∶5,其中Fe2+與Fe3+物質的量之比為 。
查看答案和解析>>
科目:高中化學 來源:2012-2013學年四川省綿陽市南山中學高二12月月考化學試卷(帶解析) 題型:填空題
已知,鐵有α、γ、δ三種晶體結構,并且在一定條件下可以相互轉化(如圖),請回答相關的問題:


α-Fe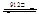 γ-Fe
γ-Fe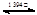 δ-Fe
δ-Fe
(1)鐵的三種晶體之間的轉化屬于 變化(填“物理”或“化學”),理由是: 。
(2)鐵的α、γ、δ三種晶體結構中,Fe原子的配位數之比為: 。
(3)設α-Fe晶胞邊長為a cm,δ-Fe晶胞邊長為b cm,計算確定:
兩種晶體的密度比為: 。(用a、b的代數式表示)
(4)Fe3C是工業煉鐵生產過程中產生的一種鐵的合金,在Fe3C晶體中,每個碳原子被6個位于頂角位置的鐵原子所包圍,成八面體結構,即碳原子配位數為6,那么,鐵原子配位數為 。
事實上,Fe3C是C與鐵的晶體在高溫下形成的間隙化合物(即碳原子填入鐵晶體中的某些空隙),根據相關信息,你認為形成碳化鐵的鐵的三種晶體結構中,最有可能的是: 。(選填“α-Fe”、“γ-Fe”或“δ-Fe”)
查看答案和解析>>
科目:高中化學 來源:2015屆河南省周口市英文學校高一下學期第三次月考化學卷(解析版) 題型:填空題
(1)下列操作錯誤的是_________(填序號)
A. 用蒸發皿進行加熱蒸發實驗時,不墊石棉網。
B. 濃硫酸不慎沾到皮膚上,迅速用NaOH溶液清洗,再用水洗。
C. 聞氣體氣味時,用手在容器口輕輕扇動,使少量氣體飄入鼻孔中。
D. 使用分液漏斗和容量瓶時,首先檢查是否漏液。
E.做實驗時,剩余試劑一律不能放回原試劑瓶。
(2) 最近媒體報道了多起衛生間清洗時,因混合使用“潔廁靈”(主要成分是鹽酸)與“84消毒液”(有效成分是NaClO)發生氯氣中毒的事件。根據你所學的氧化還原反應知識,用離子方程式表示產生氯氣的原因: 。
(3) 已知向四羥基鋁酸鈉溶液中加入稀鹽酸有氫氧化鋁生成。某同學根據所學知識,提出不能使用該方法制取A1(OH)3,理由為 。(用離子方程式表示)
請你另舉出一種用氯化鋁溶液制取A1(OH)3的合理方法,該反應的離子方程式為 。
(4)據有關報道。目前已能冶煉出純度高達99.9999%的鐵,下列關于純鐵的敘述中,正確的是 (填字母)。
A.硬度比鋼小,熔點比鋼高 B.不能與鹽酸反應
C.與不銹鋼成分相同 D.在冷的濃硫酸中鈍化
(5)向沸水中逐滴滴加飽和FeCl3溶液,至液體呈透明的紅褐色時停止加熱,所得分散系的分散質大小范圍是 。
(6)合成氨工業生產中常用鐵觸媒做催化劑,其主要成分是FeO、Fe2O3。已知某鐵觸媒中,鐵、氧離子的物質的量之比為4∶5,其中Fe2+與Fe3+物質的量之比為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com