
| V |
| Vm |
| 5.6L |
| 22.4L/mol |
| ||


科目:高中化學 來源: 題型:
| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)2 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Mn(OH)2 | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:
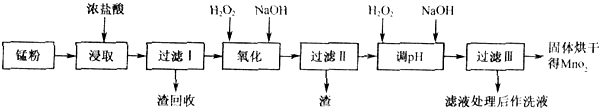
(16分)回收的廢舊鋅錳干電池經過處理后可得到錳粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由錳粉制取MnO2的步驟和數據如下:
| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
(1)在加熱條件下,用濃鹽酸浸取錳粉得到含有Mn2+、Fe3+等離子的溶液,MnO2與濃鹽酸反應的離子方程式 ,該處理方法的缺點 。
(2)步驟I中濾渣的化學式 ,步驟I中濾渣的化學式 。
(3)向步驟I的濾液中加足量H2O2的作用為 。再加NaOH溶液調節pH在3.7<pH<8.3,目的是 。
(4)向步驟II的濾液中H2O2溶液,再加NaOH溶液調節pH為9,使Mn2+轉化成MnO2,在這一過程中H2O2起 (填氧化劑、還原劑)的作用。
查看答案和解析>>
科目:高中化學 來源:廣東省惠州市2011屆高三第一次調研考試(理綜)化學部分 題型:填空題
(16分)回收的廢舊鋅錳干電池經過處理后可得到錳粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由錳粉制取MnO2的步驟和數據如下:
| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化學 來源:廣東省惠州市2010-2011學年高三第一次調研考試(理綜)化學部分 題型:填空題
(16分)回收的廢舊鋅錳干電池經過處理后可得到錳粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由錳粉制取MnO2的步驟和數據如下:

|
物質 |
開始沉淀 |
沉淀完全 |
|
Fe(OH)3 |
2.7 |
3.7 |
|
Fe(OH)2 |
7.6 |
9.6 |
|
Fe(OH)2 |
8.3 |
9.8 |
(1)在加熱條件下,用濃鹽酸浸取錳粉得到含有Mn2+、Fe3+等離子的溶液,MnO2與濃鹽酸反應的離子方程式 ,該處理方法的缺點 。
(2)步驟I中濾渣的化學式 ,步驟I中濾渣的化學式 。
(3)向步驟I的濾液中加足量H2O2的作用為 。再加NaOH溶液調節pH在3.7<pH<8.3,目的是 。
(4)向步驟II的濾液中H2O2溶液,再加NaOH溶液調節pH為9,使Mn2+轉化成MnO2,在這一過程中H2O2起 (填氧化劑、還原劑)的作用。
查看答案和解析>>
科目:高中化學 來源: 題型:
回收的廢舊鋅錳干電池經過處理后可得到錳粉(主要含MnO2、Mn(OH)2、Fe、NH4Cl和炭黑等),由錳粉制取MnO2的步驟和數據如下:

| 物質 | 開始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)2 | 8.3 | 9.8 |
(1)在加熱條件下,用濃鹽酸浸取錳粉得到含有Mn2+、Fe3+等離子的溶液,MnO2與濃鹽酸反應的離子方程式 ,該處理方法的缺點 。
(2)步驟I中濾渣的化學式 ,步驟I中濾渣的化學式 。
(3)向步驟I的濾液中加足量H2O2的作用為 。再加NaOH溶液調節pH在3.7<pH<8.3,目的是 。
(4)向步驟II的濾液中H2O2溶液,再加NaOH溶液調節pH為9,使Mn2+轉化成MnO2,在這一過程中H2O2起 (填氧化劑、還原劑)的作用。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com