
| 加入的物質 | 結論 | |
| A | 100mL 2mol•L-1H2SO4 | 反應結束后,c(Na+)=c(SO42-) |
| B | 0.20molCaO | 溶液中$\frac{c(O{H}^{-})}{c(HC{O}_{3}^{-})}$增大 |
| C | 200mL H2O | 由水電離出的c(H+)•c(OH-)不變 |
| D | 0.4molNaHSO4固體 | 反應完全后,溶液pH減小,c(Na+)不變 |
| A. | A | B. | B | C. | C | D. | D |
分析 n(Na2CO3)=0.2mol,碳酸鈉是強堿弱酸鹽,碳酸根離子水解導致溶液呈堿性,水解方程式為CO32-+H2O?HCO3-+OH-,
A.n(H2SO4)=2mol/L×0.1L=0.2mol,H2SO4和Na2CO3反應方程式為Na2CO3+H2SO4=Na2SO4+CO2↑+H2O,根據方程式知,二者恰好反應生成強酸強堿溶液Na2SO4,溶液呈中性,根據電荷守恒判斷c(Na+)、c(SO42-)相對大小;
B.CaO+H2O=Ca(OH)2、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,所以得CaO+H2O+Na2CO3=CaCO3↓+2NaOH,根據方程式知,二者恰好反應生成NaOH,反應后溶液中的溶質是NaOH;
C.加水稀釋促進碳酸鈉水解;
D.NaHSO4和Na2CO3反應方程式為:2NaHSO4+Na2CO3=Na2SO4+H2O+CO2↑,根據方程式知,二者恰好反應生成Na2SO4、H2O、CO2,溶液中的溶質是硫酸鈉,溶液呈中性.
解答 解:n(Na2CO3)=0.2mol,碳酸鈉是強堿弱酸鹽,碳酸根離子水解導致溶液呈堿性,水解方程式為CO32-+H2O?HCO3-+OH-,
A.n(H2SO4)=2mol/L×0.1L=0.2mol,H2SO4和Na2CO3反應方程式為Na2CO3+H2SO4=Na2SO4+CO2↑+H2O,根據方程式知,二者恰好反應生成強酸強堿溶液Na2SO4,溶液呈中性,則c(H+)=c(OH-),根據電荷守恒得(Na+)=2c(SO42-),故A錯誤;
B.CaO+H2O=Ca(OH)2、Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,隨著CO32-的消耗,CO32-+H2O?HCO3-+OH-向左移動,c(HCO3-)減小,反應生成OH-,則c(OH-)增大,導致溶液中$\frac{c(O{H}^{-})}{c(HC{{O}_{3}}^{-})}$增大,故B正確;
C.加水稀釋促進碳酸鈉水解,則由水電離出的n(H+)、n(OH-)都增大,但氫離子、氫氧根離子物質的量增大倍數小于溶液體積增大倍數,c(H+)、c(OH-)減小,二者濃度之積減小,故C錯誤;
D.NaHSO4和Na2CO3反應方程式為:2NaHSO4+Na2CO3=Na2SO4+H2O+CO2↑,根據方程式知,二者恰好反應生成Na2SO4、H2O、CO2,溶液中的溶質是硫酸鈉,溶液呈中性,溶液由堿性變為中性,溶液的pH減小,因為硫酸氫鈉中含有鈉離子,所以c(Na+)增大,故D錯誤;
故選B.
點評 本題為2015年高考題的改編題,考查離子濃度大小比較,為高頻考點,明確鹽類水解原理及物質之間的反應是解本題關鍵,結合電荷守恒、鹽類水解特點分析解答,易錯選項是C,注意C中計算的是水電離出的c(H+).c(OH-)之積而不是溶液中c(H+).c(OH-)之積,為易錯點.


科目:高中化學 來源: 題型:選擇題
| A. | ②③ | B. | ②④ | C. | ①② | D. | ①③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 物質 | 熔點/℃ | 沸點/℃ | 其他 |
| CCl4 | -23 | 76 | 與TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮濕空氣產生白霧,在550℃時能被氧氣氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 取用鈉、鉀、白磷時,沒用完的藥品要放回原瓶 | |
| B. | 用pH試紙測得氯水的pH為2 | |
| C. | 氯水、硝酸銀溶液存放在配有磨口塞的棕色細口瓶中 | |
| D. | 金屬鈉著火時,用細沙覆蓋滅火 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 濃硝酸一般要保存棕色試劑瓶中,置于陰涼處,原因是:4HNO3$\frac{\underline{\;見光或受熱\;}}{\;}$2NO2↑+O2↑+2H2O | |
| B. | 配制240ml濃度為1 mol•L-1的NaOH溶液,需將NaOH固體放在燒杯中,用托盤天平稱取10.00g,選用250ml的容量瓶進行配制 | |
| C. | 常溫下可用鐵質或鋁制容器儲運濃硝酸,是因為常溫下二者不發生反應 | |
| D. | 銨鹽在加熱時都會分解產生氨氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 172.5 kJ/mol | B. | -172.5 kJ/mol | C. | 393.5 kJ/mol | D. | -393.5 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | N2(g)+3H2(g)$?_{500℃、30MPa}^{催化劑}$2MH3(g)△H=-38.6kJ•mol-1 | |
| B. | N2(g)+3H2(g)═2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | N2(g)+3H2(g)═2NH3(g)△H=38.6kJ•mol-1 | |
| D. | 不能確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
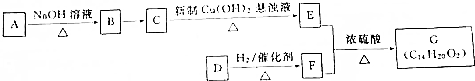
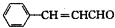 或
或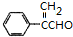 .
.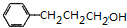 $→_{△}^{濃H_{2}SO_{4}}$
$→_{△}^{濃H_{2}SO_{4}}$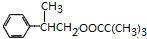 +H2O或(CH3)3CCOOH+
+H2O或(CH3)3CCOOH+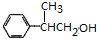 $→_{△}^{濃H_{2}SO_{4}}$
$→_{△}^{濃H_{2}SO_{4}}$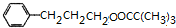 +H2O.
+H2O. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com