
 ,⑥與⑨形成的5原子分子的結(jié)構(gòu)式為
,⑥與⑨形成的5原子分子的結(jié)構(gòu)式為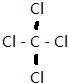 .
.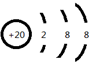
分析 根據(jù)元素在周期表中位置知,①為Na、②為K、③為Mg、④為Ca、⑤為Al、⑥為C、⑦為O、⑧為S、⑨為Cl、⑩為Si,
(1)元素⑦為氧元素,氧元素寫出的18電子氫化物為雙氧水,雙氧水為共價(jià)化合物,寫出雙氧水的電子式;⑥為C、⑨為Cl,二者形成的5原子分子為四氯化碳,寫出四氯化碳的結(jié)構(gòu)式;
(2 非金屬性越強(qiáng),元素最高價(jià)氧化物對應(yīng)水化物的堿性越強(qiáng);根據(jù)其化學(xué)式判斷含有的化學(xué)鍵類型;
(3)④為鈣元素,其形成的簡單離子為鈣離子,寫出鈣離子的離子結(jié)構(gòu)示意圖;
(4)⑨為Cl元素,第五周期元素中與⑨元素同主族的元素為I元素;氯氣能夠?qū)⒌怆x子氧化成碘單質(zhì),說明氯元素的非金屬性大于碘元素;
(5)⑦的氫化物為水,⑧的氫化物為硫化氫,水分子存在氫鍵導(dǎo)致其沸點(diǎn)較高;
(6)鋁與氫氧化鈉溶液反應(yīng)生成偏鋁酸鈉和氫氣,據(jù)此寫出反應(yīng)的離子方程式.
解答 解:根據(jù)元素在周期表中位置知,①為Na、②為K、③為Mg、④為Ca、⑤為Al、⑥為C、⑦為O、⑧為S、⑨為Cl、⑩為Si,
(1)元素⑦為O元素,氧元素可形成18電子的氫化物X為雙氧水,雙氧水為共價(jià)化合物,其電子式為: ;⑥為C、⑨為Cl,二者形成的5原子分子為四氯化碳,四氯化碳為共價(jià)化合物,其結(jié)構(gòu)式為:
;⑥為C、⑨為Cl,二者形成的5原子分子為四氯化碳,四氯化碳為共價(jià)化合物,其結(jié)構(gòu)式為: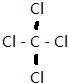 ,
,
故答案為: ;
;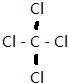 ;
;
(2 )①為Na、②為K、③為Mg、④為Ca、⑤為Al,非金屬性越強(qiáng),最高價(jià)氧化物對應(yīng)的水化物堿性越強(qiáng),則①②③④⑤五種元素最高價(jià)氧化物對應(yīng)水化物中,堿性最強(qiáng)的是KOH;氫氧化鉀屬于離子化合物,其化學(xué)式組成離子鍵和共價(jià)鍵,
故答案為:KOH;離子鍵、共價(jià)鍵;
(3)④為Ca元素,形成的簡單離子為鈣離子,鈣離子的核電荷數(shù)為20,核外電子總數(shù)為18,鈣離子的結(jié)構(gòu)示意圖為: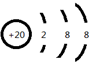 ,
,
故答案為: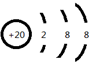 ;
;
(4)⑨為Cl元素,第五周期元素中與⑨元素同主族的元素為I元素,I的原子序數(shù)為54;根據(jù)反應(yīng)Cl2+2I-═2Cl-+I2可知Cl元素比I元素的非金屬性強(qiáng),
故答案為:54;Cl2+2I-═2Cl-+I2;
(5)⑦為O、⑧為S,二者氫化物分別為水和硫化氫,由于水分子存在氫鍵,則水的沸點(diǎn)大于硫化氫,
故答案為:水分子間有氫鍵;
(6)⑤的單質(zhì)為Al,①的最高價(jià)氧化物對應(yīng)的水化物為NaOH,二者反應(yīng)的離子方程式為:2Al+2OH-+2H2O═AlO2-+3H2↑,
故答案為:2Al+2OH-+2H2O═AlO2-+3H2↑.
點(diǎn)評 本題考查了元素周期表與元素周期律的綜合應(yīng)用,題目難度中等,熟練掌握元素周期表結(jié)構(gòu)、元素周期律的內(nèi)容為解答關(guān)鍵,注意明確常見化學(xué)用語的概念及書寫原則,能夠正確書寫常見反應(yīng)的離子方程式.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學(xué)生10分鐘應(yīng)用題系列答案
小學(xué)生10分鐘應(yīng)用題系列答案
| 年級 | 高中課程 | 年級 | 初中課程 |
| 高一 | 高一免費(fèi)課程推薦! | 初一 | 初一免費(fèi)課程推薦! |
| 高二 | 高二免費(fèi)課程推薦! | 初二 | 初二免費(fèi)課程推薦! |
| 高三 | 高三免費(fèi)課程推薦! | 初三 | 初三免費(fèi)課程推薦! |
科目:高中化學(xué) 來源:2017屆黑龍江省哈爾濱市高三上學(xué)期期中考試化學(xué)試卷(解析版) 題型:選擇題
一定條件下,通過下列反應(yīng)可以制備特種陶瓷的原料M gO: MgSO4(s)+ CO(g)  MgO(s)+ CO2(g)+SO2(g)△H>0該反應(yīng)在恒容的密閉容器中達(dá)到平衡后,若僅改變圖中橫坐標(biāo)x的值,重新達(dá)到平衡后,縱坐標(biāo)y隨x變化趨勢合理的是
MgO(s)+ CO2(g)+SO2(g)△H>0該反應(yīng)在恒容的密閉容器中達(dá)到平衡后,若僅改變圖中橫坐標(biāo)x的值,重新達(dá)到平衡后,縱坐標(biāo)y隨x變化趨勢合理的是
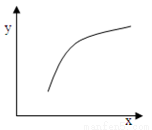
選項(xiàng) | x | y |
A | 溫度 | 容器內(nèi)混合氣體的密度 |
B | CO的物質(zhì)的量 | CO2與CO的物質(zhì)的量之比 |
C | SO2的濃度 | 平衡常數(shù)K |
D | MgSO4的質(zhì)量(忽略體積) | CO的轉(zhuǎn)化率 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | C2H4 | B. | C3H6 | C. | C6H6 | D. | CH4 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | 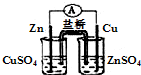 構(gòu)成鋅-銅原電池 | B. | 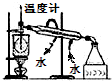 碘的CCl4溶液中分離I2并回收CCl4 | ||
| C. | 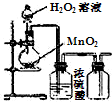 制取O2 | D. | 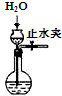 檢查裝置氣密性 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | 原子序數(shù):A>B>D>C | B. | 金屬性B>D,非金屬性A>C | ||
| C. | 原子半徑:D>B>C>A | D. | 簡單離子半徑:C>B>D>A |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
| A. | 乙烯、乙炔均能使溴水和酸性高錳酸鉀溶液褪色,但褪色的原理不一樣 | |
| B. | 石油的分餾、裂化和煤的干餾都是化學(xué)變化 | |
| C. | “乙醇汽油”是在汽油里加入適量乙醇而形成的一種燃料,它是一種新型化合物 | |
| D. | 乙炔在實(shí)驗(yàn)室制取時(shí),用長頸漏斗將飽和食鹽水加入圓底燒瓶中與電石反應(yīng) |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:選擇題
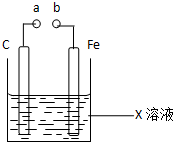
| A. | X如果是Fe2(SO4)3,則不論a和b是否用導(dǎo)線連接成通路,鐵片均發(fā)生氧化反應(yīng) | |
| B. | X如果是CuSO4,a和b分別連接直流電源正、負(fù)極,一段時(shí)間后鐵片質(zhì)量增加 | |
| C. | X如果是HCl,則不論a和b用導(dǎo)線連接還是a和b分別連接直流電源的正、負(fù)極時(shí),H+的移動方向均相同 | |
| D. | X如果是NaCl,則a和b連接時(shí),該裝置可模擬生鐵在食鹽水中被腐蝕的過程 |
查看答案和解析>>
科目:高中化學(xué) 來源: 題型:解答題
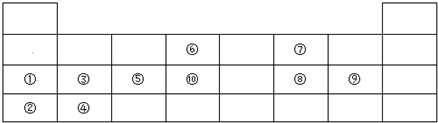
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ① | ⑦ | ④ | ||||
| 3 | ③ | ⑤ | ⑧ | ⑩ | ||||
| 4 | ② | ⑨ |
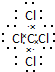 ,該分子含有極性(填“極性”或“非極性”)鍵. 26號Fe元素在元素周期表中的位置是第四周期ⅤⅢ族.
,該分子含有極性(填“極性”或“非極性”)鍵. 26號Fe元素在元素周期表中的位置是第四周期ⅤⅢ族. ;該化合物與二氧化碳的方程式為2Na2O2+2CO2=2Na2CO3+O2;④⑧⑨元素的離子的還原性由強(qiáng)到弱順序?yàn)锽r->Cl->F-(用離子符號答題).
;該化合物與二氧化碳的方程式為2Na2O2+2CO2=2Na2CO3+O2;④⑧⑨元素的離子的還原性由強(qiáng)到弱順序?yàn)锽r->Cl->F-(用離子符號答題).查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com