
下列各項操作中,不發生“先產生沉淀,然后沉淀又溶解”現象的是
①向飽和碳酸鈉溶液中通入過量的CO2
②向Fe(OH)3膠體中逐滴加入過量的稀硫酸
③向AgNO3溶液中逐滴加入過量氨水
④向硅酸鈉溶液中逐滴加入過量的鹽酸
A.①② B.①④
C.①③ D.②③
 華東師大版一課一練系列答案
華東師大版一課一練系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化學 來源:2017屆河南省高三上第三次周考化學卷(解析版) 題型:實驗題
甲同學進行Fe2+還原性的實驗,針對異常現象進行探究。
步驟一:制取FeCl2溶液.向0.1mol·L-1 FeCl3溶液中加足量鐵粉振蕩,靜置后取上層清液,測得pH<1。
實驗二:向2mL FeCl2溶液中滴加2滴0.1mol·L-1KSCN溶液,無現象;再滴加5滴5% H2O2溶液(物質的量濃度約為1.5mol·L-1、pH約為5),觀察到溶液變紅,大約10秒左右紅色褪去,有氣體生成(經檢驗為O2).
(1)用離子方程式表示步驟二中溶液變紅的原因:________________。
(2)甲探究步驟二中溶液褪色的原因:
Ⅰ.取褪色后溶液兩份,一份滴加FeCl3溶液無現象;另一份滴加KSCN溶液出現紅色;
Ⅱ.取褪色后溶液,滴加鹽酸和BaCl2溶液,產生白色沉淀。
Ⅲ.向2mL 0.1mol·L-1 FeCl3溶液中滴加2滴0.1mol·L-1KSCN溶液,變紅,通入O2,無明顯變化。
①實驗I的說明__________________;
②實驗Ⅲ的目的是____________________。
得出結論:溶液褪色的原因是酸性條件下H2O2將SCN-氧化成SO42-。
(3)①甲直接用FeCl2·4H2O配制_________mol·L-1的FeCl2溶液,重復步驟二中的操作,發現液體紅色并未褪去,進一步探究其原因:
②.用激光筆分別照射紅色液體和滴加了KSCN溶液的FeCl3溶液,前者有丁達爾效應,后者無.測所配FeCl2溶液的pH約為3.由此,乙認為紅色不褪去的可能原因是:____________________。
③.查閱資料后推測,紅色不褪去的原因還可能是pH較大時H2O2不能氧化SCN-.乙利用上述部分試劑,通過實驗排除了這一可能.乙的實驗操作及現象是:
步驟 | 試劑及操作 | 現 象 |
i | 生成白色沉淀 | |
ii | 向i所得溶液中滴加0.1mol·L-1 FeCl3溶液 |
查看答案和解析>>
科目:高中化學 來源:2017屆甘肅省高三上12月月考化學試卷(解析版) 題型:選擇題
普伐他汀是—種調節血脂的藥物,其結構簡式如圖所示(未表示出其空間構型)。下列關 于普伐他汀的描述不正確的是
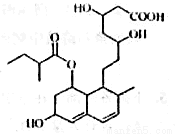
A.能使酸性KMnO4溶液褪色
B.能發生加成、取代、消去反應
C.其分子式為C23H35O7
D.1mol該物質最多可與2molNaOH反應
查看答案和解析>>
科目:高中化學 來源:2017屆甘肅省高三上12月月考化學試卷(解析版) 題型:選擇題
某小組同學用如圖所示裝置研究電化學原理。下列關于該原電池的說法不正確的是

A.原電池的總反應為Fe+Cu2+═Fe2++Cu
B.鹽橋中是KNO3溶液,則鹽橋中NO3﹣移 向乙燒杯
向乙燒杯
C.其他條件不變,若將CuCl2溶液換為NH4Cl溶液,石墨電極反應式為2H++2e﹣═H2↑
D.反應前,電極質量相等,一段時間后,兩電極質量相差12g,導線中通過0.2mol電子
查看答案和解析>>
科目:高中化學 來源:2017屆甘肅省高三上12月月考化學試卷(解析版) 題型:選擇題
氨催化氧化法制硝酸的原理為4NH3(g)+5O2(g) 4NO(g)+6H2O(g)。在濃氨水中通入空氣,將赤熱鉑絲插入氨水中引發反應后鉑絲保持紅熱狀態至反應停止。下列說法正確的是
4NO(g)+6H2O(g)。在濃氨水中通入空氣,將赤熱鉑絲插入氨水中引發反應后鉑絲保持紅熱狀態至反應停止。下列說法正確的是
A.上述反應在較高溫度下才能自發進行
B.該反應的正反應活化能小于逆反應活化能
C.該反應中,斷裂化學鍵的總鍵能大于形成化學鍵的總鍵能
D.若NH3和O2的混合氣發生上述反應,氣體通入足量水中,剩余氣體一定是O2
查看答案和解析>>
科目:高中化學 來源:2017屆甘肅省高三上12月月考化學試卷(解析版) 題型:選擇題
設NA為阿伏加德羅常數的值,下列與NA有關的說法正確的是
A.在反應KClO3+6HCl=KCl+3Cl2↑+3H2O中,當得到標準狀況下67.2 L Cl2時,反應中轉移的電子數為6 NA
B.6.0 g SiO2晶體中含有的硅氧鍵數目為0.2 NA
C.標準狀況下,22.4 L NO和11.2 L O2混合后氣體的分子總數為NA
D.S2和S8的混合物共6.4 g,其中所含硫原子數一定為0.2 NA
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二12月月考化學試卷(解析版) 題型:填空題
已知2A2(g)+B2(g) 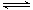 2C3(g);△H=-akJ·mol-1(a >0),在一個有催化劑的固定容積的容器中加入2mol A2和1mol B2,在500℃時充分反應達平衡后C3的濃度為w mol·L-1,放出熱量b kJ。請回答下列問題:
2C3(g);△H=-akJ·mol-1(a >0),在一個有催化劑的固定容積的容器中加入2mol A2和1mol B2,在500℃時充分反應達平衡后C3的濃度為w mol·L-1,放出熱量b kJ。請回答下列問題:
(1)比較a___________b填“>”、“=”、“<”)。
(2)若將反應溫度升高到700℃,該反應的平衡常數將_____________(“增大”、“減小”或“不變”)。
(3)能說明該反應已經達到平衡狀態的是
A.V(C3)=2V(B2) B.容器內氣體壓強保持不變
C.V逆(A2)=2V正(B2) D.容器內的氣體密度保持不變
(4)為使該反應的反應速率增大,且平衡向正反應方向移動的是_____________。
A.及時分離出C3氣體 B.適當升高溫度
C.增大B2的濃度 D.選擇高效的催化劑
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省高二12月月考化學試卷(解析版) 題型:選擇題
室溫下,向10mL0.1mol/L醋酸溶液中加水稀釋后,下列說法正確的是
A.溶液中粒子的數目減小
B.再加入CH3COONa固體能促進醋酸的電離
C.醋酸的電離程度增大,c(H+)亦増大
D.溶液中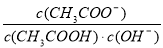 不變
不變
查看答案和解析>>
科目:高中化學 來源:2016-2017學年內蒙古高一期中化學卷(解析版) 題型:選擇題
下列有關四種基本反應類型與氧化還原反應關系的說法中正確的是
A.化合反應一定是氧化還原反應
B.分解反應一定不是氧化還原反應
C.置換反應一定是氧化還原反應
D.復分解反應不一定是氧化還原反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com