
某校化學研究性學習小組對氯氣的性質和用途進行了調查分析,了解了氯氣能應用 于衣物漂白、水體的殺菌和消毒的原理。
(1) 氯氣溶于水可用于漂白、消毒的原因是_______,反應的離子方程式為_______ ;
(2) 通常使用漂白液(NaClO溶液)作漂白劑而不用氯氣的理由是_____(寫出一項即可);
(3) 在一定量的石灰乳中通入一定量的氯氣,二者恰好完全反應 (發生的反應均為放熱反應)。最終生成物中含有Cl-、 ClO-、ClO3-三種含氯元素的離子,其中ClO-、ClO3-兩種離 子的物質的量(n)與反應時間(t)的變化曲線如下圖所示。
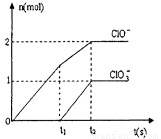
①O-t1時間內,Ca(OH)2與Cl2發生反應的化學方程式為_______;
②t2時,Ca(OH)2與Cl2發生反應的總的化學方程式為_______
③該石灰乳中含有Ca(OH)2的質量是_______g;
(9分)
(1)氯氣和水反應生成強氧化性的次氯酸(1分), Cl2+H2O=HClO+H++ClO-(1分) ;
(2)NaClO更穩定,便于儲存和運輸(1分);
(3)①2Ca(OH)2+2Cl2=Ca(C1O)2+CaCl2+2H2O(2分);
②10Ca(OH)2+10Cl2=2Ca(C1O)2+Ca(C1O3)2+7CaCl2+10H2O(2分);
③370 g (2分)
【解析】
試題分析:(1)氯氣和水反應生成次氯酸,次氯酸具有很強的氧化性,故氯氣溶于水可用于漂白、消毒的原因是氯氣和水反應生成強氧化性的次氯酸,反應的離子方程式為Cl2+H2O=HClO+H++ClO-。
(2)氯氣有毒,且不容易使用,故通常使用漂白液(NaClO溶液)作漂白劑而不用氯氣的理由是NaClO更穩定,便于儲存和運輸。
(3) ①由圖像分析,t1時刻沒有ClO3-離子生成,故O-t1時間內,Ca(OH)2與Cl2發生反應的化學方程式為2Ca(OH)2+2Cl2=Ca(C1O)2+CaCl2+2H2O。
②由圖像分析,t2時有ClO-、ClO3-離子生成,故t2時,Ca(OH)2與Cl2發生反應的總的化學方程式為10Ca(OH)2+10Cl2=2Ca(C1O)2+Ca(C1O3)2+7CaCl2+10H2O。
③由化學方程計算得該石灰乳中含有Ca(OH)2的質量是370 g。
考點:氯氣的性質
點評:本題考查的是氯氣的性質的相關知識,題目難度中等,考查學生對基礎知識的掌握程度和計算能力。


科目:高中化學 來源: 題型:閱讀理解
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解

| ||
| ||
查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
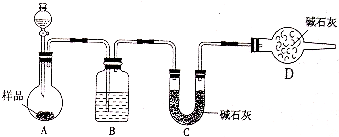
 某校化學研究性學習小組設計如下實驗方案,測定放置己久的小蘇打樣品中純堿的質量分數.
某校化學研究性學習小組設計如下實驗方案,測定放置己久的小蘇打樣品中純堿的質量分數.查看答案和解析>>
科目:高中化學 來源:2011-2012學年黑龍江哈爾濱市第六中學高三上學期期末考試化學試卷 題型:填空題
(14分)某校化學研究性學習小組設計如下實驗方案,測定放置已久的小蘇打樣品中純堿的質量分數。
(1)方案一:稱取一定質量的樣品,置于坩堝中加熱至恒重后,冷卻,稱量剩余固體質量,計算。實驗中加熱至恒重的目的是 。
(2)方案二:稱取一定量樣品,置于小燒杯中,加適量水溶解,向小燒杯中加入足量氯化鋇溶液,過濾洗滌,干燥沉淀,稱量固體質量,計算:
①過濾操作中,除了燒杯、漏斗外還用到的玻璃儀器有______________________;
②試驗中判斷沉淀是否完全的方法是_______________________________________
③若加入試劑改為氫氧化鋇,已知稱得樣品9.5g,干燥的沉淀質量為19.7g,則樣品中碳酸鈉的質量分數為_________________(保留一位小數)。
查看答案和解析>>
科目:高中化學 來源:2012屆黑龍江哈爾濱市高三上學期期末考試化學試卷 題型:填空題
(14分)某校化學研究性學習小組設計如下實驗方案,測定放置已久的小蘇打樣品中純堿的質量分數。
(1)方案一:稱取一定質量的樣品,置于坩堝中加熱至恒重后,冷卻,稱量剩余固體質量,計算。實驗中加熱至恒重的目的是 。
(2)方案二:稱取一定量樣品,置于小燒杯中,加適量水溶解,向小燒杯中加入足量氯化鋇溶液,過濾洗滌,干燥沉淀,稱量固體質量,計算:
①過濾操作中,除了燒杯、漏斗外還用到的玻璃儀器有______________________;
②試驗中判斷沉淀是否完全的方法是_______________________________________
③若加入試劑改為氫氧化鋇,已知稱得樣品9.5g,干燥的沉淀質量為19.7g,則樣品中碳酸鈉的質量分數為_________________(保留一位小數)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com