
【題目】在容積一定的密閉容器中,置入一定量的NO(g)和足量C(s),發生反應C(s)+2NO(g) ![]() CO2(g)+N2(g),平衡狀態時NO(g)的物質的量濃度[NO]與溫度T的關系如圖所示。則下列說法中正確的是( )
CO2(g)+N2(g),平衡狀態時NO(g)的物質的量濃度[NO]與溫度T的關系如圖所示。則下列說法中正確的是( )

A. 該反應的ΔH>0
B. 若該反應在T1、T2時的平衡常數分別為K1、K2,則K1<K2
C. 在T2時,若反應體系處于狀態D,則此時一定有v正<v逆
D. 在T3時,若混合氣體的密度不再變化,則可以判斷反應達到平衡狀態C
 期末復習檢測系列答案
期末復習檢測系列答案 超能學典單元期中期末專題沖刺100分系列答案
超能學典單元期中期末專題沖刺100分系列答案 黃岡360度定制密卷系列答案
黃岡360度定制密卷系列答案 陽光考場單元測試卷系列答案
陽光考場單元測試卷系列答案 名校聯盟沖刺卷系列答案
名校聯盟沖刺卷系列答案科目:高中化學 來源: 題型:
【題目】反應4NH3+5O2=4NO+6H2O(g)在5L密閉容器中進行,半分鐘后,NO的物質的量增加了0.3mo1,則此反應的平均速率Vx為( )
A. VO2=0.01mo1L-1s-1B. VNO=0.008mo1L-1s-1
C. VH2O=0.002mo1L-1s-1D. VNH3=0.002mo1L-1s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】榮獲2019年諾貝爾化學獎的吉野彰是最早開發具有商業價值的鋰離子電池的日本科學家,他設計的可充電電池的工作原理示意圖如圖所示。該可充電電池的放電反應為LixCn+Li(1-x)CoO2=LiCoO2+nC。NA表示阿伏伽德羅常數的值。下列說法錯誤的是( )
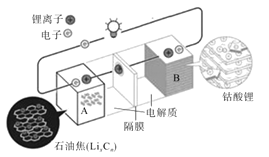
A.該電池用于電動汽車可有效減少光化學煙霧污染
B.充電時,正極反應為LiCoO2-xe-=Li(1-x)CoO2+xLi+
C.放電時,Li+由A極移向B極
D.若初始兩電極質量相等,當轉移2NA個電子時,兩電極質量差為14g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】可逆反應3H2+N2![]() 2NH3的正、逆反應速率可用各反應物或生成物濃度的變化來表示,下列各關系中能說明反應已達到平衡狀態的是
2NH3的正、逆反應速率可用各反應物或生成物濃度的變化來表示,下列各關系中能說明反應已達到平衡狀態的是
A. v正(N2)=v正(H2)B. v正(N2)=v逆(NH3)
C. 2v正(H2)=3v逆(NH3)D. v正(N2)=3v逆(H2)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室用MnO2和濃鹽酸制取氯氣時,有14.6 g氯化氫被氧化,所得Cl2全部用石灰水吸收,可制得漂白粉的質量是
A. 14.3 g B. 25.4 g C. 28.6 g D. 50.8 g
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】壽山石![]() 是我國四大印章石之首,被稱為國石。X,Y,M,N是原子序數依次增大的短周期元素,M元素是地殼中含量最高的金屬元素,N元素的單質常用來制造太陽能電池,
是我國四大印章石之首,被稱為國石。X,Y,M,N是原子序數依次增大的短周期元素,M元素是地殼中含量最高的金屬元素,N元素的單質常用來制造太陽能電池,![]() 和
和![]() 含有相同的電子數。下列說法正確的是
含有相同的電子數。下列說法正確的是
A.原子半徑:![]()
B.簡單氫化物的穩定性:![]()
C.第82號元素與M位于同一主族
D.X和M形成的化合物溶于水顯酸性
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】兩種金屬混合粉末15g,與足量的鹽酸反應時生成11.2L H2(標況下),符合上述情況的金屬混合物是( )
A. Mg、Fe B. Zn、Ag C. Fe、Zn D. Mg、Al
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵是生產生活中應用最廣泛的金屬,煉鐵技術備受關注,已知:
①![]()
![]()
②![]()
![]()
③斷裂![]() 氣體中的化學鍵需要吸收1076kJ的能量,斷裂
氣體中的化學鍵需要吸收1076kJ的能量,斷裂![]() 氣體中的化學鍵需要吸收1490kJ的能量。
氣體中的化學鍵需要吸收1490kJ的能量。
請回答:
(1)斷裂![]() 中所有化學鍵需要吸收的能量為________kJ。
中所有化學鍵需要吸收的能量為________kJ。
(2)T1℃時,向密閉容器中加入一定量的![]() 和C,發生反應①,達到平衡后
和C,發生反應①,達到平衡后![]() 的濃度為
的濃度為![]() ;其他條件不變,縮小容器體積,再次達到平衡時,
;其他條件不變,縮小容器體積,再次達到平衡時,![]() 的濃度為
的濃度為![]() ,則a________b(選填“>”“<”或“=”)。
,則a________b(選填“>”“<”或“=”)。
(3)起始溫度均為T2℃時,向容積為10L的三個恒容密閉容器中,分別加入一定量的![]() 和CO發生反應②,測得相關數據如表所示:
和CO發生反應②,測得相關數據如表所示:
編號 | 容器 | 起始時物質的量/mol | 平衡時物質的量/mol | 平衡常數(K) | |
|
|
| |||
1 | 恒溫 | 0.5 | 1.5 | 0.8 K1 | |
2 | 恒溫 | 2 | 3 | M | K2 |
3 | 絕熱 | 1 | 1.5 | n | K3 |
①T2℃時,容器1中反應的平衡常數K1=_______。
②容器2中,5min達到平衡,則0~5min以![]() 表示該反應的速率
表示該反應的速率![]() ___________。
___________。
③對于三個容器中的反應,下列說法正確的是(填字母)_________。
A.![]() B.容器1和容器2中
B.容器1和容器2中![]() 的平衡轉化率
的平衡轉化率![]()
C.![]() D.平衡時氣體壓強:
D.平衡時氣體壓強:![]()
(4)一定條件下,向恒壓密閉容器中充入0.5mol ![]() 和1.0mol CO,發生反應②,CO和
和1.0mol CO,發生反應②,CO和![]() 的物質的量濃度(c)與時間(t)的關系如圖所示:
的物質的量濃度(c)與時間(t)的關系如圖所示:

①6min時改變的外界條件為________________。
②若在6min時,恒溫將容器體積擴大到10L,請在圖中畫出6~10min![]() 的物質的量濃度隨時間變化的曲線_________。
的物質的量濃度隨時間變化的曲線_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列敘述正確的是( )
A.膠體的本質特征是丁達爾效應
B.焰色反應是元素的性質,屬于化學變化
C.密度為1.84g/ml、98%的硫酸,其物質的量濃度為1.84mol/L
D.NA個HCl分子的質量(以克為單位)與其相對分子質量在數值上相等
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com