
I.利用含錳廢水(主要含Mn2+、SO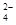 、H+、Fe2+、Al3+、Cu2+)可制備高性能磁性材料碳酸錳(MnCO3)。其中一種工業流程如下:
、H+、Fe2+、Al3+、Cu2+)可制備高性能磁性材料碳酸錳(MnCO3)。其中一種工業流程如下: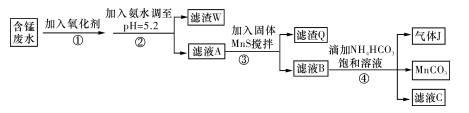
已知某些物質完全沉淀的pH如下表: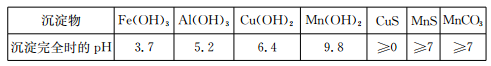
回答下列問題:
(1)過程②中,所得濾渣的主要成分是 。
(2)過程③中,發生反應的離子方程式是 。
(3)過程④中,若生成的氣體J可使澄清石灰水變渾濁,則生成MnCO3的反應的離子方程式是 。
(4)由MnCO3可制得重要的催化劑MnO2:2MnCO3+O2=2MnO2+2CO2。
現在空氣中加熱460.0 g MnCO3,得到332.0 g產品,若產品中雜質只有MnO,則該產品中MnO2的質量分數是 (用百分數表示,小數點后保留1位)。
Ⅱ.常溫下,濃度均為0.1 mol/L的下列六種溶液的pH如下表: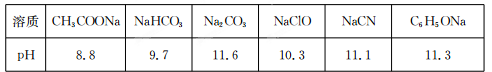
(1)上述鹽溶液中的陰離子,結合H+能力最強的是 。
(2)根據表中數據判斷,濃度均為0.0l mol/L的下列物質的溶液中,酸性最強的是
(填序號)。
A.HCN B.HC1O C.C6H5OH D.CH3 COOH E.H2 CO3
(3)據上表數據,請你判斷下列反應不能成立的是 (填序號)。
A.HCN+ Na2 CO3=NaHCO3+NaCN
B.CH3 COOH+NaCN=CH3 COONa+HCN
C.CO2 +H2O+2C6 H5ONa=Na2 CO3 +2C6 H5OH
D.CH3 COONa+HClO=NaClO十CH3 COOH
I.(1)Fe(OH)3,Al(OH)3
(2)MnS + Cu2+ = Mn2+ + CuS
(3)Mn2++2HCO3- =MnCO3 +CO2↑+H2O
(4)78.6%
II.(1)CO32-;(2)D;(3)CD。
解析試題分析:I.(1)調節pH在5.2,由題意知Fe2+和Al3+均以Fe(OH)3和Al(OH)3沉淀狀態存在;(2)加入MnS是為了使其中Cu2+產生CuS沉淀除去,故攪拌目的是使MnS 與 Cu2+快速、充分反應,離子方程式MnS + Cu2+ = Mn2+ + CuS↓;(3)由題意知Mn2+和加入的HCO3-反應,產生CO2氣體和MnCO3沉淀,故離子方程式Mn2++2HCO3- =MnCO3 +CO2↑+H2O;(4)MnCO3受熱分解為MnO,MnO部分氧化為MnO2,產品中雜質有MnO,460.0 gMnCO3,物質的量為4mol,受熱產生4molMnO,設產生MnO2物質的量為xmol,即有xmolMnO氧化,剩余MnO為(4-x)mol,產物的總質量為(4-x)mol×71g·mol-1+xmol×87g·mol-1=332g,x=3,則MnO2的質量分數=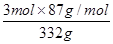 =78.6%。
=78.6%。
II.(1)對應酸的酸性越弱,其陰離子越易水解,其陰離子結合質子能力越強,根據表格中數據可知CO32-結合質子能力最強;(2)對應酸的酸性越弱,其陰離子越易水解,其鹽溶液堿性越強,所以PH最小的酸性最強,所以CH3COOH酸性最強,故答案為D;(3)復分解反應中,堿性強的物質置換堿性弱的物質,酸性強的物質置換酸性弱的物質,根據以上知識對各選項進行判斷即可;故答案為CD。
考點:考查鐵鹽和亞鐵鹽的相互轉變;難溶電解質的溶解平衡;離子方程式的書寫等。


 快樂暑假暑假能力自測中西書局系列答案
快樂暑假暑假能力自測中西書局系列答案科目:高中化學 來源: 題型:填空題
25 ℃時,將0.01 mol CH3COONa和0.002 mol HCl溶于水,形成1 L混合溶液。
(1)該溶液中存在著三個平衡體系,用電離方程式或離子方程式表示:
① _________________________;
② _________________________;
③ _________________________。
(2)溶液中共有 種不同的粒子(指分子和離子)。
(3)在這些粒子中,濃度為0.01 mol·L-1的是 ,濃度為0.002 mol·L-1的是 。
(4) 和 兩種粒子物質的量之和等于0.01 mol。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
弱電解質電離情況可以用電離度和電離平衡常數表示,表1是常溫下幾種弱酸的電離平衡常數(Ka)和弱堿的電離平衡常數(Kb),表2是常溫下幾種難(微)溶物的溶度積常數(Ksp)。
表1
| 酸或堿 | 電離平衡常數(Ka或Kb) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 4.6×10-4 |
| HCN | 5×10-10 |
| HClO | 3×10-8 |
| NH3·H2O | 1.8×10-5 |
| 難(微)溶物 | 溶度積常數(Ksp) |
| BaSO4 | 1×10-10 |
| BaCO3 | 2.6×10-9 |
| CaSO4 | 7×10-5 |
| CaCO3 | 5×10-9 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
工業生產Na2S常用方法是無水芒硝(Na2SO4)一碳還原法,其流程示意圖如下:
(1)若煅燒階段所得氣體為等物質的量的CO和CO2。寫出煅燒時發生的總反應方程式:______________________。
(2)用堿液浸出產品比用熱水更好,理由是__________________。
(3)廢水中汞常用硫化鈉除去,汞的除去率與溶液pH和硫化鈉實際用量與理論用量比值x的關系如圖所示。為使除汞達到最佳效果,應控制條件是________________。
(4)取Na2S(含少量NaOH),加入到CuSO4溶液中,充分攪拌,若反應后溶液pH=4,此時溶液中c(S2-)=________mol·L-1[已知:CuS的Ksp=8.8×10-36;Cu(OH)2的Ksp=2.2×10-20(保留2位有效數字)]。
(5)納米Cu2O常用電解法制備,制備過程用銅棒和石墨棒做電極,Cu(NO3)2做電解液。電解生成Cu2O應在________;該電極pH將________(填“升高”“不變”或“降低”),用電極方程式解釋pH發生變化的原因______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
現有0.175mol/L醋酸鈉溶液500mL(已知醋酸的電離常數Ka=1.75x10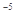 )
)
(1)寫出醋酸鈉水解反應的化學方程式_____________________。
(2)下列圖像能說明醋酸鈉的水解反應達到平衡的是_____________________。
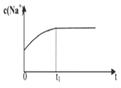 | 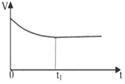 | 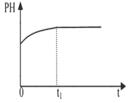 |  |
| A.溶液中c (Na+)與反應時間t的關系 | B.CH3COO-的水解速率與反應時間t的關系 | C.溶液的PH與反應時間t的關系 | D.KW與反應時間t的關系 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
水溶液中存在多種平衡,請根據所學化學知識回答下列問題:
(1)在濃度均為0.1mol/L①CH3COONH4 ②NH4HSO4 ③NH3.H2O ④(NH4)2SO4溶液中,NH4+濃度由大到小的順序為 (填序號)
(2)濃度均為0.1 mol·L-1的下列溶液:①硫酸、②醋酸、③氫氧化鈉、④氯化銨四種溶液中由水電離出的H+濃度由大到小的順序是(填序號) 。
(3)恒溫下,向pH=6的蒸餾水中加入2.3g金屬鈉,充分反應后,再加蒸餾水稀釋到1L,所得溶液的pH= 。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
為了證明一水合氨(NH3·H2O)是弱電解質,甲、乙、丙三人分別選用下列試劑進行實驗:0.010 mol·L-1氨水、0.1 mol·L-1NH4Cl溶液、NH4Cl晶體、酚酞試劑、pH試紙、蒸餾水。
(1)甲用pH試紙測出0.010 mol·L-1氨水的pH為10,則認定一水合氨是弱電解質,你認為這一方法是否正確?________(填“是”或“否”)并說明理由______________
(2)乙取出10 mL 0.010 mol·L-1氨水,用pH試紙測出其pH=a,然后用蒸餾水稀釋至1 000 mL,再用pH試紙測出其pH為b,若要確認NH3·H2O是弱電解質,則a、b值應滿足什么關系?________(用“等式”或“不等式”表示)。
(3)丙取出10 mL 0.010 mol·L-1氨水,滴入2滴酚酞溶液,顯粉紅色,再加入NH4Cl晶體少量,顏色變淺。你認為這一方法能否證明NH3·H2O是弱電解質?并說明原因:______________________________________________________________________。
(4)請你根據所提供的試劑,再提出一個合理又簡便的方案證明NH3·H2O是弱電解質:__________________________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
下表是不同溫度下水的離子積的數據:
| 溫度/℃ | 25 | t1 | t2 |
| 水的離子積 | 1×10-14 | a | 1×10-12 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
電離平衡常數是衡量弱電解質電離程度強弱的量。已知如表數據。
| 化學式 | 電離平衡常數(25℃) |
| NH3·H2O | Kb=1.77×10-5 |
| HCN | Ka=4.93×10-10 |
| CH3COOH | Ka=1.76×10-5 |
| H2CO3 | Ka1=4.30×10-7,Ka2=5.61×10-11 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com