

| A.圖①表示化學反應中能量的變化,反應CO(g)+H2O(g)=CO2(g)+H2(g)的△H大于0 |
| B.圖②為氫氧燃料電池示意圖,正、負極通入氣體體積之比為2:1 |
| C.圖③表示物質(zhì)a、b的溶解度曲線,可以用結晶方法從a、b混合物中提純a |
D.圖④表示壓強對可逆反應2A(g)+2B(g)  3C(g)+D(s)的影響,乙的壓強大 3C(g)+D(s)的影響,乙的壓強大 |
 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案科目:高中化學 來源:不詳 題型:單選題
| A.實驗①中,反應生成的Mn2+可能是該反應的催化劑 |
| B.實驗②中,該反應是太陽能轉變?yōu)楣饽?/td> |
| C.實驗③中,有氣泡產(chǎn)生的棒是鐵棒 |
| D.實驗④中,加入的水是反應的催化劑,且該反應能自發(fā)進行 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
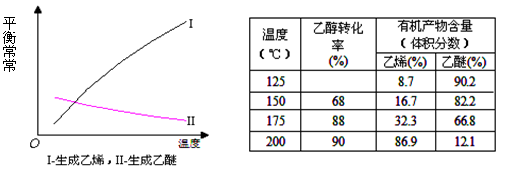
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.常溫下,向飽和Na2CO3溶液中加入少量BaSO4粉末,過濾,向洗凈的沉淀中加稀鹽酸,有氣泡產(chǎn)生,則常溫下Ksp (BaCO3)<Ksp (BaSO4) |
| B.常溫下,向純水中加入鈉或氫氧化鈉都能使水的電離平衡逆向移動,水的離子積不變 |
| C.常溫下,反應4Fe(OH)2(s)+ O2(g) +2H2O(l) =4Fe(OH)3(s)的△H<0、△S<0 |
| D.鉛蓄電池在工作過程中,負極質(zhì)量減少,陽極質(zhì)量增加 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題

 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O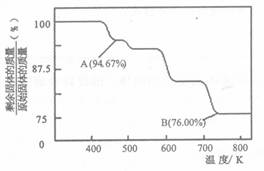
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 CO2+NO △H =" a" kJ/mol達到平衡后,降低溫度,混和氣體的顏色變淺。下列判斷正確的是
CO2+NO △H =" a" kJ/mol達到平衡后,降低溫度,混和氣體的顏色變淺。下列判斷正確的是| A.a(chǎn)<0 |
| B.降低溫度,各物質(zhì)的濃度不變 |
| C.降低溫度,CO的平衡轉化率降低 |
| D.使用催化劑能加快反應速率并提高反應物的平衡轉化率 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
| A.二氧化碳能溶于水,可用于生產(chǎn)碳酸型飲料 |
| B.固體二氧化碳俗稱干冰,可用于人工降雨 |
| C.二氧化碳用于滅火是因為降低了可燃物的著火點 |
| D.超臨界二氧化碳作萃取溶劑用于從天然產(chǎn)物提取和凈化活性組分 |
 CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,測得C02和CH3OH(g)的濃度隨時間變化如圖所示。
CH3OH(g)+H2O(g) ΔH=-49.0kJ.m01-1,測得C02和CH3OH(g)的濃度隨時間變化如圖所示。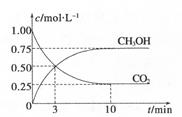
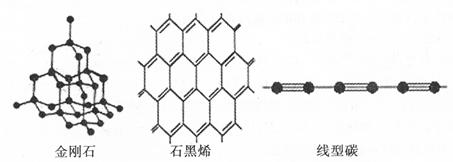
查看答案和解析>>
科目:高中化學 來源:不詳 題型:填空題
 2NH3(g),若在恒溫、恒壓條件下向平衡體系中通入氬氣,則平衡 移動(填“向左”“向右”或“不”);使用催化劑,上述反應的△H________(填“增大” “減小” 或“不改變”)。
2NH3(g),若在恒溫、恒壓條件下向平衡體系中通入氬氣,則平衡 移動(填“向左”“向右”或“不”);使用催化劑,上述反應的△H________(填“增大” “減小” 或“不改變”)。 式),生成該沉淀的離子方程式為____________。已知25℃時Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。
式),生成該沉淀的離子方程式為____________。已知25℃時Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cu(OH)2]=2.2×10-20。 中性,則Va︰Vb= 。
中性,則Va︰Vb= 。

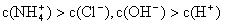

 NH3·H2O + H+,則該反應常溫下的平衡常數(shù)K= (已知:常溫下,NH3·H2O的電離平衡常數(shù)Kb=1.7×10—5 mol·L—1)
NH3·H2O + H+,則該反應常溫下的平衡常數(shù)K= (已知:常溫下,NH3·H2O的電離平衡常數(shù)Kb=1.7×10—5 mol·L—1)查看答案和解析>>
科目:高中化學 來源:不詳 題型:實驗題
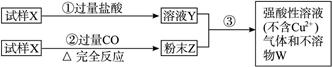
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com