

 2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:
2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
 ,
, ;2H++2e-→H2↑;
;2H++2e-→H2↑; 2H2(g)+O2(g)
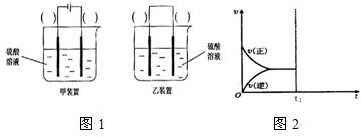
2H2(g)+O2(g) =1.7×10-6mol/L,由圖可知H2的濃度隨時間降低,改變條件瞬間H2濃度不變,所以不保持溫度不變,將容器的體積縮小,
=1.7×10-6mol/L,由圖可知H2的濃度隨時間降低,改變條件瞬間H2濃度不變,所以不保持溫度不變,將容器的體積縮小, ,
, .
.

科目:高中化學 來源: 題型:閱讀理解
| 光 |
| Cu2O |
| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
查看答案和解析>>
科目:高中化學 來源:諸城市模擬 題型:問答題

| 光 |
| Cu2O |
| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
查看答案和解析>>
科目:高中化學 來源:2010年山東省濰坊市四縣市聯考高考化學模擬試卷(解析版) 題型:解答題

 2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:
2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
查看答案和解析>>
科目:高中化學 來源:2010年山東省濰坊市四縣市聯考高考化學模擬試卷(解析版) 題型:解答題

 2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:
2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
查看答案和解析>>
科目:高中化學 來源:2010年山東省濰坊市四縣市聯考高考化學模擬試卷(解析版) 題型:解答題

 2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:
2H2(g)+O2(g)△H>0,不同時段產生O2的量見下表:| 時間/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com