(2009?宿遷模擬)工業合成氨與制備硝酸一般可連續生產,流程如圖1:

在800℃、鉑催化劑存在條件下,氨與氧氣反應的主要產物是NO 和H
2O.在實際生產中氨的氧化率與混合氣中氧氨比(氧氣與氨氣物質的量比,以γ{n(O
2)/n(NH
3)}表示)的關系如圖2所示.
請回答下列各題:
(1)若氨氧化率達到100%,理論上γ{n(O
2)/n (NH
3)}為1.25,而實際生產要將γ值維持在1.7~2.2之間,其原因是
一方面提高氧氣量,增大氨的氧化率;另方面γ值在該范圍,氨的氧化率已高達95~99%,再提高,氨的氧化率上升空間已有限,反而會增加能耗,提高生產成本
一方面提高氧氣量,增大氨的氧化率;另方面γ值在該范圍,氨的氧化率已高達95~99%,再提高,氨的氧化率上升空間已有限,反而會增加能耗,提高生產成本
.
(2)若使氨的氧化率達到95%,應控制氨在氨、空氣混合氣體中的體積分數約為
10.5%
10.5%
(設氧氣占空氣的體積分數為20%).將γ=1.75的氨、空氣混合氣體通入800℃、盛有鉑催化劑的氧化爐,充分反應后導入到吸收塔的氣體的主要成分是
N2、NO2、H2O
N2、NO2、H2O
.
(3)現以a mol NH
3和足量空氣為原料(不考慮N
2的反應)最大程度制取NH
4NO
3,經過一系列轉化反應后,向反應后的混合物中加入b g水,得到密度為ρ g?mL
-1的溶液,計算該溶液中NH
4NO
3物質的量濃度可能的最大值
.





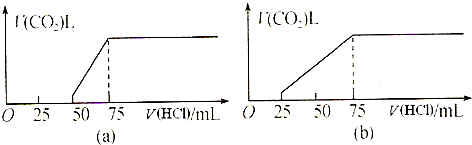

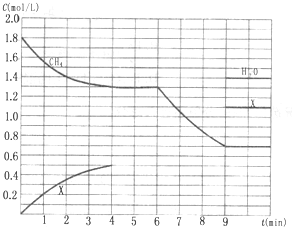 向反應體系中同時通入甲烷、氧氣和水蒸氣,發生的主要化學反應有:
向反應體系中同時通入甲烷、氧氣和水蒸氣,發生的主要化學反應有: