
【題目】有硫酸鎂溶液500mL,它的密度是1.20g·cm3,其中鎂離子的質量分數是4.8%,則有關該溶液的說法不正確的是
A. 溶質的質量分數是24% B. 溶液的物質的量濃度是2.4mol·L1
C. 溶質和溶劑的物質的量之比約為1∶21.1 D. 硫酸根離子的質量是230.4g
 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
【題目】某溫度下,在一固定容積的容器中進行反應:SO3(g)+NO(g)![]() NO2 (g)+SO2(g),下列情況一定能說明已經達到化學反應限度的是
NO2 (g)+SO2(g),下列情況一定能說明已經達到化學反應限度的是
A.體系總壓強不再隨時間而改變 B.體系總質量不再隨時間而改變
C.NO(g)和 NO2(g)的生成速率相同 D.SO3 (g)和 NO(g)的濃度比為 1:1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】乙烯在化工生產領域應用廣泛。
(1)乙烯能合成很多有實用價值的有機物。

①試劑a是_____________。
②反應Ⅰ的反應類型是_____________。
(2)以原油為起始原料合成聚乙烯的路線如下圖所示。

①聚乙烯的結構簡式是_____________。
②寫出分子式符合C4H10的有機物的結構簡式_____________。
(3)已知:CH3CHO![]() CH3COOH。以CH2=CH2為起始原料,選用必要的無機試劑合成乙酸乙酯,寫出合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)。
CH3COOH。以CH2=CH2為起始原料,選用必要的無機試劑合成乙酸乙酯,寫出合成路線(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)。
____________________________________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知常溫下0.1mol/L的NH4HCO3溶液pH =7.8, 已知含氮(或含碳)各微粒的分布分數(平衡時某種微粒的濃度占各種微粒濃度之和的分數)與pH的關系如下圖所示。下列說法不正確的是
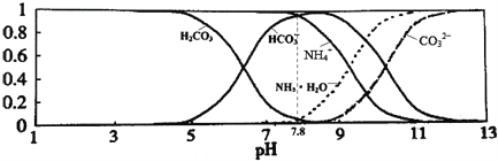
A. 溶液的pH=9時,溶液中存在下列關系:c(HCO3-)>c(NH4+)>c(NH3·H2O)>c(CO32-)
B. NH4HCO3溶液中存在下列守恒關系:c(NH4+)+c(NH3·H2O)=c(HCO3-)+c(CO32-)+c(H2CO3)
C. 通過分析可知常溫下 :Kb(NH3·H2O)<Ka1(H2CO3)
D. 在此溶液中滴加少量濃鹽酸,溶液中c(CO32-) / c(HCO3-)減小
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣中的主要污染物是NO和CO。為減輕大氣污染,人們提出通過以下反應來處理汽車尾氣:
(1)已知:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) △H=﹣746.5kJ/mol
2CO2(g)+N2(g) △H=﹣746.5kJ/mol
2C(s)+O2(g)![]() 2CO(g) △H=﹣221 kJ/mol
2CO(g) △H=﹣221 kJ/mol
C(s)+O2(g)![]() CO2(g) △H=﹣393.5 kJ/mol
CO2(g) △H=﹣393.5 kJ/mol
則N2(g)+O2(g)═2NO(g) △H=____________ kJ/mol
(2)T℃下,在一容積不變的密閉容器中,通入一定量的NO和CO,用氣體傳感器測得不同時間NO和CO的濃度如下表:
時間/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/10-4mol/L | 10.0 | 4.50 | C1 | 1.50 | 1.00 | 1.00 |
c(CO)/10-3mol/L | 3.60 | 3.05 | C2 | 2.75 | 2.70 | 2.70 |
則C2較合理的數值為_________(填字母標號)
A.4.20 B.4.00 C.2.95 D.2.85
(3)將不同物質的量的H2O(g)和CO(g)分別通入體積為2L的恒容密閉容器中,進行反應:H2O(g)+CO2(g) ![]() CO2(g)+H2(g)得到如下三組數據:
CO2(g)+H2(g)得到如下三組數據:
實驗組 | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所需時間/min | ||
H2O | CO | CO | H2 | |||
i | 650 | 2 | 4 | 2.4 | 1.6 | 5 |
ii | 900 | 1 | 2 | 1.6 | 0.4 | 3 |
iii | 900 | a | b | C | d | 1 |
若a=2,b=1,則c=____,三組實驗對應平衡常數的關系K(i)_____ K(ii) _____ K(iii)(填“>”、“<”或“=”)。
(4)控制反應條件,CO和H2可以用來合成甲醇和二甲醚,其中合成二甲醚的化學方程式為:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g),在相同條件下合成二甲醚和合成甲醇的原料平衡轉化率隨氫碳比
CH3OCH3(g)+CO2(g),在相同條件下合成二甲醚和合成甲醇的原料平衡轉化率隨氫碳比![]() 的變化如圖所示:
的變化如圖所示:

①合成二甲醚的最佳氫碳比為__________。
②甲醇使用不當會導致污染,可用電解法消除這種污染。其原理是電解CoSO4、稀硫酸和CH3OH的混合溶液,將Co2+氧化為Co3+,Co3+再將CH3OH氧化成CO2,Co3+氧化CH3OH的離子方程式為________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列關于金屬氧化物的說法不正確的是( )
A.Fe3O4是具有磁性的黑色晶體
B.Al2O3能溶于酸和強堿,是兩性氧化物
C.Na2O是堿性氧化物,可與H2O、CO2反應
D.FeO不穩定,在空氣中受熱迅速被氧化為Fe2O3
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】最近有研究人員發現了一種處理高濃度乙醛廢水的新方法一隔膜電解法,乙醛分別在陰、陽極發生反應,轉化為乙醇和乙酸。實驗室以一定濃度的乙醛—Na2SO4 溶液為電解質溶液,模擬乙醛廢水的處理過程,其裝置如圖所示。下列說法正確的是

A. 電解過程中,兩極除分別生成乙酸和乙醇外,均產生了無色氣體,則陽極產生的是O2
B. 陽極反應為CH3CHO-2e-+2H+=CH3COOH+H2O
C. 電解過程中,陰極區Na2SO4的物質的量增大
D. 若以CH4—空氣燃料電池為直流電源,燃料電池的b 極應通入空氣
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,相同的鎂條與下列酸溶液反應,反應開始時放出H2最快的是( )
A.10mL 1mol/L 硫酸B.10mL 1mol/L 醋酸
C.10mL 3mol/L 硝酸D.40mL 1mol/L 鹽酸
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在恒容絕熱條件下,一定能說明反應A(g)+B(?)![]() 2C(g)已達到平衡狀態的是
2C(g)已達到平衡狀態的是
A. 容器內的密度不再變化 B. C的生成速率與A的分解速率之比為2:1
C. 混合物的平均摩爾質量不再變化 D. 容器內的溫度不再發生變化
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com