
【題目】X 、Y 、Z、W 、R 、M 、Q 是7種短周期元素,原子序數依次增大。已知X與其它6種元素不在同一周期,Y原子最外層電子數是次外層電子數的2倍,W是地殼中含量最多的元素,R、M、Q處于同一周期,R是該短周期中半徑最大的元素,M與W同一主族。請用化學用語回答下列問題:
(1)Y在周期表中的位置是________________;M、 W、R的簡單離子半徑大小順序為___________。(用離子符號表示)
(2)X、W、Q按照原子個數比1∶1∶1形成的化合物的電子式為_____________。
(3)W與R形成的化合物可作供氧劑,該化合物含有的化學鍵類型有:__________________________。
(4)M、Q的陰離子還原性較強的是:____________(用離子符號表示),用一個置換反應證實這一結論(寫化學方程式)____________________________________。
(5)以上幾種元素中,其中有一種元素的氣態氫化物可與它的最高價氧化物的水化物發生非氧化還原反應,請寫出反應的化學方程式:_____________________________________________________________
【答案】第二周期第、ⅣA族 S2->O2->Na+ ![]() 離子鍵 、共價鍵 S2- Cl2+Na2S=2NaCl+S↓ 或Cl2+H2S=S↓+2HCl NH3+HNO3=NH4NO3
離子鍵 、共價鍵 S2- Cl2+Na2S=2NaCl+S↓ 或Cl2+H2S=S↓+2HCl NH3+HNO3=NH4NO3
【解析】
X 、Y 、Z、W 、R 、M 、Q 是7種短周期元素,原子序數依次增大。已知X與其它6種元素不在同一周期,說明為第一周期,即氫元素,Y原子最外層電子數是次外層電子數的2倍,為碳元素,W是地殼中含量最多的元素,為氧元素,則Z為氮元素。R、M、Q處于同一周期,R是該短周期中半徑最大的元素,為鈉元素,M與W同一主族,為硫元素,則Q為氯元素。
(1)Y為碳元素,在第二周期第IVA族;根據電子層越多半徑越大、核外電子排布相同的離子序大徑小分析,半徑關系為 S2->O2->Na+;
(2)氫氧氯三種元素按原子個數比為1:1:1形成的化合物為次氯酸,其電子式為: ![]() ;
;
(3)氧和鈉形成的可做供氧劑的物質為過氧化鈉,含有離子鍵 、共價鍵;
(4)硫離子和氯離子比較,因為氯元素非金屬性比硫強,所以硫離子的還原性較強。用置換反應證實時可以用氯氣和硫化鈉或硫化氫的反應,方程式為: Cl2+Na2S=2NaCl+S↓ 或Cl2+H2S=S↓+2HCl;
(5) 氮元素的氫化物為氨氣,氮元素的最高價氧化物對應的水化物為硝酸,二者可以反應生成硝酸銨,方程式為:NH3+HNO3=NH4NO3。


科目:高中化學 來源: 題型:
【題目】某無機化合物的二聚分子結構如圖,該分子中A、B兩種元素都是第三周期的元素,分子中所有原子最外層都達到8電子穩定結構。關于該化合物的說法不正確的是( )

A. 化學式是Al2Cl6
B. 不存在離子鍵和非極性共價鍵
C. 在固態時所形成的晶體是分子晶體
D. 是離子化合物,在熔融狀態下能導電
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖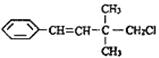 ,關于該有機物的下列敘述中不正確的是( )
,關于該有機物的下列敘述中不正確的是( )
A. 一定條件下,能發生加聚反應
B. 1mol該有機物在一定條件下最多能與4molH2發生反應
C. 能使酸性KMnO4溶液、溴水褪色,且原理相同
D. 該有機物苯環上的一溴代物有3種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業以濃縮海水為原料提取溴的部分過程如下:

某課外小組在實驗室模擬上述過程設計以下裝置進行實驗(所有橡膠制品均已被保護,夾持裝置已略去):

(1)實驗開始時,A裝置中不通熱空氣,先通入a氣體的目的是(用離子方程式表示)_________。
(2)A裝置中通入a氣體一段時間后,停止通入,改通熱空氣。通入熱空氣的目的是_________。
(3)反應過程中,B裝置中Br2與SO2反應的化學方程式____________________。
(4)C裝置的作用是___________________。
(5)該小組同學向反應后B裝置的溶液中通入氯氣,充分反應得到混合液。
①一位同學根據溴的沸點是59℃,提出采用____________________方法從該混合液中分離出溴單質。
②另一位同學向該混合液中加入四氯化碳,充分振蕩、靜置后放出下層液體,這種方法是________。
(6)某同學提出證明反應后B裝置的溶液中含有溴離子的實驗方案是:取出少量溶液,先加入過量新制氯水,再加入KI淀粉溶液,觀察溶液是否變藍色。該方案是否合理并簡述理由: _______。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的幾種。①若加入鋅粒,產生無色無味的氣體;②若加入NaOH溶液,產生白色沉淀,且產生的沉淀量與加入NaOH的物質的量之間的關系如圖所示。則下列說法正確的是( )

A. 溶液中一定不含CO32﹣,可能含有SO42-和NO3-
B. 溶液中n(NH4+)="0.2" mol
C. 溶液中的陽離子只有H+、Mg2+、Al3+
D. n(H+)︰n(Al3+)︰n(Mg2+)=1︰1︰1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組構想將汽車尾氣(NO、NO2)轉化為重要的化工原料HNO3,其原理如圖所示,其中A、B為多孔材料.下列說法正確的是
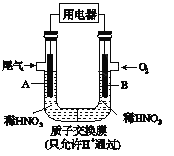
A. 電極A表面反應之一為NO2-e-+H2O= NO3_+2H+
B. 電極B附近的c(NO3_)增大
C. 電解質溶液中電流的方向由B到A,電子的流向與之相反
D. 該電池工作時,每轉移4mol電子,消耗22.4L O2
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】單斜硫和正交硫轉化為二氧化硫的能量變化如下圖所示。下列說法正確的是( )

A. 由圖可知,單斜硫轉化為正交硫的反應為吸熱反應
B. 正交硫比單斜硫性質活潑
C. 相同條件下,等量的正交硫比單斜硫所含有的能量低
D. 相同條件下,生成等量的二氧化硫氣體,正交硫放出的熱量多
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】中國科學院科研團隊研究表明,在常溫常壓和可見光下,基于 LDH(一種固體催化劑) 合成 NH3 的原理示意圖,化學方程式為 2N2+6H2O=4NH3+3O2。下列說法不正確的是()
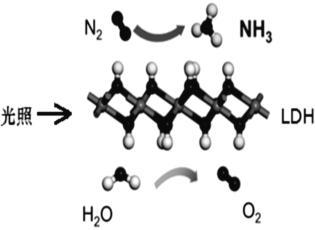
A. 該過程將太陽能轉化成為化學能
B. 該過程中,只涉及共價鍵的斷裂與生成
C. 氧化產物與還原產物的物質的量之比為 4∶3
D. 2molN2 與足量水充分反應,能制得氨氣 4mol
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com