
2008年10月8日,美籍華裔科學家錢永健獲得2008年度諾貝爾化學獎。16歲時,他憑借一個金屬易受硫氰酸鹽腐蝕的調查項目,榮獲“美國西屋科學天才獎”。下列敘述正確的是( )
A. 金屬腐蝕就是金屬失去電子被還原的過程
B. 合金的熔點都高于它的成分金屬,合金的耐腐蝕性也都比其成分金屬強
C. 銅板上的鐵鉚釘處在潮濕的空氣中直接發生反應:Fe-3e-= Fe3+,繼而形成鐵銹
D. 將水庫中的水閘(鋼板)與外加直流電源的負極相連,正極連接到一塊廢鐵上可防止水閘被腐蝕
 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2016-2017學年甘肅省嘉峪關市高二上學期期末考試化學試卷(解析版) 題型:選擇題
理論上不能設計為原電池的化學反應是( )
A. CH4(g)+2O2(g)==CO2(g)+2H2O(l) △H<0
B. HNO3(aq)+NaOH(aq)==NaNO3(aq)+H2O(l) △H<0
C. 2H2(g)+O2(g)==2H2O(l) △H<0
D. 2FeCl3(aq)+Fe(s)==3FeCl3(aq) △H<0
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省新余市高二下學期入學考試化學試卷(解析版) 題型:填空題
下表為常見幾種弱酸的電離常數,
酸 | 電離常數(Ka) | 酸 | 電離常數(Ka) |
CH3COOH | 1.8×10-5 | HClO | 3×10-8 |
H2O2 | K1=2.4×10-12 K2=1×10-25 | H2CO3 | K1=4.4×10-7 K2=4.7×10-11 |
I.結合上表回答下列問題(均為常溫下的數據):
(1)在常溫下,相同物質的量濃度的①CH3COONa②Na2CO3③NaClO三種溶液的pH由小到大的順序為______________________(用序號回答)
(2)向Na2CO3溶液中通入氯氣,可制得某種生產和生活中常用的漂白、消毒的鈉鹽,同時還有另兩種鈉鹽生成,該反應的化學方程式為_________________
II.過氧化氫(H2 O2)為淡藍色粘稠液體,是中學常見試劑.
(1)H2O2含有的共價鍵類型為_____________________
(2)實驗室可用稀硫酸與BaO2反應來制取H2 O2,該反應的化學方程式為__________________
(3)經測定H2O2為二元弱酸,酸性比碳酸還弱,不穩定易分解.已知Na2O2中通人干燥的CO2不反應,但通人潮濕的CO2卻可以產生O2,試用化學方程式表示這一過程___________________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省新余市高二下學期入學考試化學試卷(解析版) 題型:選擇題
下面是某學生利用數據分析的情況,其中正確的是( )
A. 根據氣體的相對分子質量,不可以比較相同狀況下氣體密度的大小
B. 根據甲烷和乙烷的熔點,不能比較二者晶體中的分子間作用力的大小
C. 比較同主族金屬元素原子半徑的大小,可以推斷元素的金屬性強弱
D. 根據液體密度的大小,可以判斷液體的揮發性的強弱
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省大同市高二2月月考化學試卷(解析版) 題型:選擇題
鉛蓄電池的電極材料是Pb和PbO2,電解質是硫酸溶液。現用鉛蓄電池電解飽和硫酸鈉溶液一段時間。已知蓄電池放電時發生的反應為PbO2+Pb+2H2SO4=2PbSO4+2H2O,假設電解時溫度不變且用惰性電極,下列結論不正確的是( )
A. 電解后,c(Na2SO4)不變,且溶液中有晶體析出
B. 電解池的陽極反應式為:4OH--4e-=2H2O+O2↑
C. 蓄電池電池放電時,每消耗0.1molPb,共生成0.1molPbSO4
D. 蓄電池中每生成2molH2O,電解池中就消耗1molH2O
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省大同市高二2月月考化學試卷(解析版) 題型:選擇題
下列敘述中正確的是( )
A. 化學反應中的能量變化,都表現為熱量的變化
B. 需要加熱才能發生的反應,一定是吸收能量的反應
C. 釋放能量的反應在常溫下一定很容易發生
D. 是吸收能量的反應還是釋放能量的反應,必須看反應物的總能量和生成物的總能量的相對大小
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山西省大同市高二2月月考化學試卷(解析版) 題型:選擇題
“活化分子”是衡量化學反應速率快慢的重要依據,下列對“活化分子”的說法不正確的是( )
A. 活化分子之間的碰撞一定是有效碰撞
B. 增大反應物的濃度,可使單位體積內活化分子增多,反應速率加快
C. 對于有氣體參加的反應增大壓強,可使單位體積內活化分子增多,反應速率加快
D. 催化劑能降低反應的活化能,使單位體積內活化分子百分數大大增加
查看答案和解析>>
科目:高中化學 來源:2016-2017學年遼寧省葫蘆島市高一下學期選拔考試化學試卷(解析版) 題型:選擇題
在某無色透明的酸性溶液中,能共存的離子組是( )
A. NH4+、NO3﹣、Al3+、Cl﹣ B. Na+、AlO2﹣、K+、NO3﹣
C. MnO4﹣、K+、SO42﹣、Na+ D. K+、SO42﹣、HCO3﹣、Na+
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二下學期開學考試化學試卷(解析版) 題型:實驗題
某實驗小組用0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液進行中和熱的測定。
Ⅰ.配制0.50 mol/L NaOH溶液
若實驗中大約要使用245 mL NaOH溶液,至少需要稱量NaOH固體_____g。
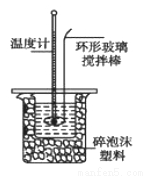
Ⅱ.測定稀硫酸和稀氫氧化鈉中和熱的實驗裝置如圖所示。
(1)寫出該反應的熱化學方程式(中和熱為57.3 kJ/mol):_____________。
(2)取50 mL NaOH溶液和30 mL硫酸溶液進行實驗,實驗數據如下表。
①請填寫下表中的空白:
起始溫度t1/℃ | 終止溫度 t2/℃ | 溫度差平均值 (t2-t1)/℃ | |||
H2SO4 | NaOH | 平均值 | |||
1 | 26.2 | 26.0 | 26.1 | 30.1 | ______ |
2 | 27.0 | 27.4 | 27.2 | 33.3 | |
3 | 25.9 | 25.9 | 25.9 | 29.8 | |
4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似認為0.50 mol/L NaOH溶液和0.50 mol/L硫酸溶液的密度都是1 g/cm3,中和后生成溶液的比熱容c=4.18 J/(g·℃)。則中和熱△H=______________取小數點后一位)。
③上述實驗數值結果與57.3 kJ/mol有偏差,產生偏差的原因可能是:______。
A.實驗裝置保溫、隔熱效果差
B.量取NaOH溶液的體積時仰視讀數
C.分多次把NaOH溶液倒入盛有硫酸的小燒杯中
D.用溫度計測定NaOH溶液起始溫度后直接測定H2SO4溶液的溫度
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com