



| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:
(2011?南京一模)下列實驗操作、實驗現象及解釋與結論都正確的是( )
|
查看答案和解析>>
科目:高中化學 來源: 題型:
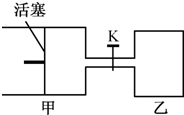 (2011?南京一模)如圖所示,向甲和乙兩容器中都充入2molX和2molY(K關閉) 起始V甲=0.8aL,V乙=aL,在相同恒定溫度下,兩容器中各自發生下列反應:X(g)+Y(g)═2Z(g)+W(g),達到平衡時,V甲=0.9aL,則下列說法錯誤的是( )
(2011?南京一模)如圖所示,向甲和乙兩容器中都充入2molX和2molY(K關閉) 起始V甲=0.8aL,V乙=aL,在相同恒定溫度下,兩容器中各自發生下列反應:X(g)+Y(g)═2Z(g)+W(g),達到平衡時,V甲=0.9aL,則下列說法錯誤的是( )查看答案和解析>>
科目:高中化學 來源: 題型:閱讀理解
 是一種可限量使用的鐵強化劑
是一種可限量使用的鐵強化劑
| 步驟 | 實驗操作與現象 |
| ① | 取富馬酸亞鐵產品l.5g,加入稀硫酸25mL,用水稀釋至50ml,加熱使其完全溶解并反應,冷卻后過濾(除去生成的富馬酸及可能過量的反應物),保存濾液. |
| ② | 取少量濾液,滴加KSCN溶液,不顯紅色 取少量濾液,滴加KSCN溶液,不顯紅色 |
| ③ | 取酸性高錳酸鉀溶液適量,向其中滴加濾液至溶液褪色 取酸性高錳酸鉀溶液適量,向其中滴加濾液至溶液褪色 |
| ④ | 取上述褪色后的溶液,滴加KSCN溶液顯紅色 取上述褪色后的溶液,滴加KSCN溶液顯紅色 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com