
【題目】化學是一門以實驗為基礎的科學。
(1)用下列實驗裝置完成對應的實驗(部分儀器略去),能達到實驗目的的是_____(填字母)。
A | B | C | D |
|
|
|
|
干燥氯氣 | 吸收NH3 | 石油的分餾 | 制取乙酸乙酯 |
(2)為除去粗鹽中的MgCl2、CaCl2、Na2SO4以及泥沙等雜質,某同學設計了一種制備精鹽的實驗方案,步驟如下(用于沉淀的試劑稍過量):
稱取粗鹽![]() 濾液
濾液![]() 精鹽
精鹽
①第Ⅰ步操作的名稱是______。
②若第Ⅱ、Ⅳ步順序顛倒,是否會對實驗結果產生影響?_____(填“有影響”或“無影響”)。
③第Ⅴ步操作所需玻璃儀器的名稱是________。
【答案】B 溶解 有影響 燒杯、漏斗、玻璃棒
【解析】
(1)A. Cl2進入后沒有出口,無法收集干燥的Cl2;
B. NH3不溶于CCl4,不會引起倒吸,且上層的水會吸收NH3,防止NH3逸出;
C. 石油分餾中,溫度計的水銀球應在蒸餾燒瓶的支管口處;
D. 由于蒸出的乙酸乙酯中含有乙醇、乙酸,它們的溶解性很強,當導管口插入液面以下時易發生倒吸。
(2)由流程可知,稱取一定質量的粗鹽后,應該加水溶解,然后向溶液中加氯化鋇可除去硫酸根離子,III中加NaOH除去鎂離子,IV中加碳酸鈉可除去鋇離子、鈣離子,過濾后濾液主要為氯化鈉、氫氧化鈉和碳酸鈉,VI中加鹽酸反應后溶液中溶質為NaCl,然后蒸發結晶得到NaCl,以此解答該題。
(1)A. 裝置是用濃硫酸干燥Cl2,裝置中Cl2進入后沒有出口,無法收集干燥的Cl2,導氣管應該長進短出,A錯誤;
B. 裝置中NH3不溶于CCl4,不會引起倒吸,且上層的水會吸收NH3,可以防止NH3逸出,B正確;
C. 在石油分餾中,溫度計是測量蒸氣溫度的,溫度計的水銀球應在蒸餾燒瓶的支管口處,不能在液面以下,C錯誤;
D. 由于蒸出的乙酸乙酯中含有未反應的乙醇、乙酸,它們的溶解性很強,當導管口插入液面以下時易發生倒吸,不能達到除雜的目的,有關將飽和食鹽水改為飽和Na2CO3溶液,且導氣管在液面以上,D錯誤;
故合理選項是B;
(2)①粗鹽中的MgCl2、CaCl2、Na2SO4以及泥沙等雜質,加水溶解后過濾除去泥沙,所以第Ⅰ步操作的名稱是溶解;
②若第Ⅱ步為加入過量BaCl2溶液除去Na2SO4、第III步加入過量NaOH溶液除去MgCl2,第IV加入過量Na2CO3除去原食鹽溶液中的CaCl2及加入的過量除雜試劑BaCl2,使二者轉化為沉淀,然后過濾除去,若第Ⅱ步與第IV順序顛倒,又引入新的雜質過量BaCl2溶液,過量的Ba2+不能除去,不能達到除去的目的,因此會對實驗結果產生影響;
③第Ⅴ步操是分離難溶性固體與溶液的方法,名稱為過濾,所需玻璃儀器的名稱是燒杯、漏斗、玻璃棒。


科目:高中化學 來源: 題型:
【題目】苯甲醛在堿性條件下可發生反應: 2C6H5CHO + NaOH→C6H5CH2OH+C6H5COONa。相關物質的物理性質如下表:
苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |||
溶 解 性 | 水中 | 微溶 | 微溶 | 溫度 | 溶解度 | 不溶 |
17℃ | 0.21 g | |||||
25℃ | 0.34 g | |||||
100℃ | 5.9 g | |||||
有機溶劑中 | 易溶 | 易溶 | 易溶 | 易溶 | ||
密度(20℃)/g·cm-3 | 1.0 | 1.0 | 1.3 | 0.9 | ||
沸點/℃ | 178 | 205 | 249 | 80 | ||
熔點/℃ | 26 | -15 | 122 | 5.4 | ||
制備苯甲醇和苯甲酸的實驗流程及涉及的主要實驗裝置(部分加熱和固定裝置已略)如下:
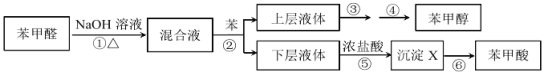
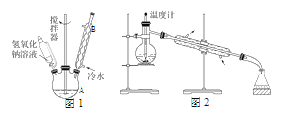
(1)第①步所用裝置(如圖 1),用攪拌器的目的是______________。儀器 B 的作用是_______________。
(2)第②步所用玻璃儀器有燒杯、_______________。
(3)第③步采用沸水浴加熱蒸餾,收集到的餾分為_________;再進行第④步,操作如圖 2 所示。圖 2 中有一處明顯錯誤,正確的應改為_________________________。
(4)第⑤步反應的離子方程式為________________________________________; 冷水洗滌沉淀 X 的優點是_________________________;檢驗沉淀 X 洗滌干凈與否的操 作:______________。
(5)第⑥步經過濾、洗滌、干燥得苯甲酸產品,然后用電子天平準確稱取 0.2440 g 苯甲酸樣品于錐形瓶中,加 100 mL 蒸餾水溶解,再用 0.1000 mol·L-1 的標準 NaOH 溶液 進行滴定,經平行實驗,測得消耗 NaOH 溶液的平均值為 19.20 mL,則苯甲酸樣品的純 度為_________ (質量百分數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某小組在驗證反應“Fe+2Ag+=Fe2++2Ag”的實驗中檢測到Fe3+,發現和探究過程如下。向硝酸酸化的0.05mol·L-1硝酸銀溶液(pH≈2)中加入過量鐵粉,攪拌后靜置,燒杯底部有黑色固體,溶液呈黃色。
(1)檢驗產物:取出少量黑色固體,洗滌后,___(填操作和現象),證明黑色固體中含有Ag。
(2)針對“溶液呈黃色”,甲認為溶液中有Fe3+,乙認為鐵粉過量時不可能有Fe3+,乙依據的原理是___(用離子方程式表示)。針對兩種觀點繼續實驗:

①取上層清液,滴加KSCN溶液,溶液變紅,證實了甲的猜測。同時發現有白色沉淀產生,且溶液顏色深淺、沉淀量多少與取樣時間有關,對比實驗記錄如下:
(資料:Ag+與SCN-生成白色沉淀AgSCN)
②對Fe3+產生的原因作出如下假設:
假設a:可能是鐵粉表面有氧化層,能產生Fe3+;
假設b:空氣中存在O2,由于___(用離子方程式表示),可氧化產生Fe3+;
假設c:酸性溶液中存在的___離子具有氧化性,可氧化產生Fe3+;
假設d:根據加入KSCN溶液后產生白色沉淀的現象,判斷溶液中一定存在Ag+,Ag+可氧化Fe2+產生Fe3+。
③下述實驗Ⅰ可證實假設a、b、c不是產生Fe3+的主要原因。實驗Ⅱ可證實假設d成立。
實驗Ⅰ:向硝酸酸化的___溶液(pH≈2)中加入過量鐵粉,攪拌后靜置,不同時間取上層清液滴加KSCN溶液。3min時溶液呈淺紅色,30min后溶液幾乎無色。
實驗Ⅱ:設計實驗證明假設d成立___。
(3)根據ⅰ~ⅲ實驗現象,結合本題涉及的三個方程式,推測實驗ⅰ~ⅲ中Fe3+濃度變化的原因(用離子方程式和文字結合表述):___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關實驗原理或操作正確的是
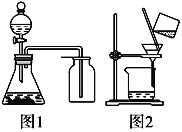
A. 選擇合適的試劑,用圖1所示裝置可分別制取少量CO2、NO和O2
B. 除去干燥CO2中混有的少量SO2,可將混合氣體依次通過盛有足量酸性KMnO4溶液、濃硫酸的洗氣瓶
C. 洗滌沉淀時(如圖2),向漏斗中加適量水,攪拌并濾干
D. 將碘水倒入分液漏斗,加適量乙醇,振蕩后靜置,可將碘萃取到乙醇中
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】亞硝酰氯(ClNO)是有機物合成中的重要試劑,其沸點為 -5.5℃,易水解。已知:AgNO2 微溶于水,能溶于硝酸,AgNO2+HNO3=AgNO3 +HNO2,某學習小組在實驗室用Cl2和NO制備ClNO并測定其純度,相關實驗裝置如圖所示。
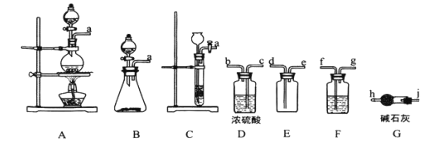
(1)制備 Cl2 的發生裝置可以選用 _________ (填字母代號)裝置,發生反應的離子方程式為________________________________________ 。
(2)欲收集一瓶干燥的氯氣,選擇合適的裝置,其連接順序為 a→_______→______→ _____→________→_______→______→______→______。(按氣流方向,用小寫字母表示,根據需要填,可以不填滿,也可補充)。
(3)實驗室可用下圖示裝置制備亞硝酰氯。其反應原理為:Cl2+2NO=2ClNO
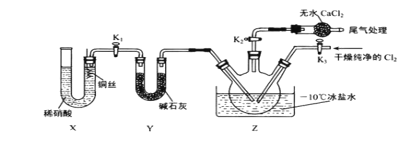
①實驗室也可用 B 裝置制備 NO , X 裝置的優點為___________________ 。
②檢驗裝置氣密性并裝入藥品,打開 K2,然后再打開 K3,通入一段時間氣體,其目的是 ___________________,然后進行其他操作,當 Z 中有一定量液體生成時,停止實驗。
(4)已知:ClNO 與 H2O 反應生成 HNO2 和 HCl。
①設計實驗證明 HNO2 是弱酸:_________________________________________。(僅提供的試劑:1 molL-1 鹽酸、 1 molL-1HNO2 溶液、 NaNO2 溶液、紅色石蕊試紙、藍色石蕊試紙)。
②通過以下實驗測定ClNO 樣品的純度。取 Z 中所得液體m g 溶于水,配制成 250 mL 溶液;取出 25.00 mL 樣品溶于錐形瓶中,以 K2CrO4 溶液為指示劑,用 c molL-1 AgNO3標準溶液滴定至終點,消耗標準溶液的體積為 20.00mL。滴定終點的現象是_____亞硝酰氯(ClNO)的質量分數為 _________。(已知: Ag2CrO4 為磚紅色固體;Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=1×10-12)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NO、NO2是大氣污染物,但只要合理利用,NO、NO2也是重要的資源。回答下列問題:
(1)氨的合成。已知:N2和H2生成NH3的反應為:![]() N2(g)+
N2(g)+![]() H2(g)
H2(g)![]() NH3(g) ΔH=-46.2kJ·mol-1
NH3(g) ΔH=-46.2kJ·mol-1
在Fe催化劑作用下的反應歷程為(※表示吸附態):
化學吸附:N2(g)→2N※;H2(g)![]() 2H※;
2H※;
表面反應:N※+H※![]() NH※;NH※+H※
NH※;NH※+H※![]() NH2※;NH2※+H※
NH2※;NH2※+H※![]() NH3※;
NH3※;
脫附:NH3※![]() NH3(g)
NH3(g)
其中N2的吸附分解反應活化能高、速率慢,決定了合成氨的整體反應速率。則利于提高合成氨平衡產率的條件有(________)
A.低溫 B.高溫 C.低壓 D.高壓 E.催化劑
(2)NH3還原法可將NO還原為N2進行脫除。已知:
①4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-1530kJ·mol-1
②N2(g)+O2(g)=2NO(g) ΔH2=+180kJ·mol-1
寫出NH3還原NO的熱化學方程式__。
(3)亞硝酰氯(ClNO)是合成有機物的中間體。將一定量的NO與Cl2充入一密閉容器中,發生反應:2NO(g)+Cl2(g)![]() 2ClNO(g) △H<0。平衡后,改變外界條件X,測得NO的轉化率α(NO)隨X的變化如圖所示,則條件X可能是__(填字母代號)。
2ClNO(g) △H<0。平衡后,改變外界條件X,測得NO的轉化率α(NO)隨X的變化如圖所示,則條件X可能是__(填字母代號)。
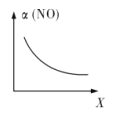
a.溫度 b.壓強 c.![]() d.與催化劑的接觸面積
d.與催化劑的接觸面積
(4)在密閉容器中充入4molCO和5molNO發生反應2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H=-746.5kJmol-1,如圖甲為平衡時NO的體積分數與溫度、壓強的關系曲線圖。
N2(g)+2CO2(g) △H=-746.5kJmol-1,如圖甲為平衡時NO的體積分數與溫度、壓強的關系曲線圖。
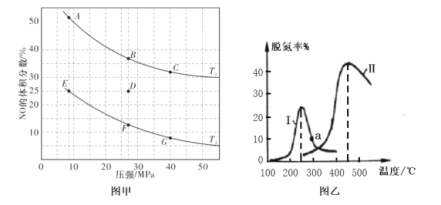
①溫度T1__T2(填“>”或“<”)。
②若反應在D點達到平衡,此時對反應進行升溫且同時擴大容器體積使平衡壓強減小,則重新達到平衡時,D點應向圖中A~G點中的__點移動。
③探究催化劑對CO、NO轉化的影響。某研究小組將NO和CO以一定的流速通過兩種不同的催化劑進行反應,相同時間內測量逸出氣體中NO含量,從而確定尾氣脫氮率(即NO的轉化率),結果如圖乙所示。溫度低于200℃時,圖中曲線I脫氮率隨溫度升高而變化不大的主要原因為__;a點__(填“
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,將一定濃度的鹽酸和醋酸加水稀釋,溶液的導電能力隨溶液體積變化的曲線如圖所示。下列說法中正確的是( )
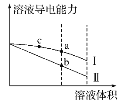
A.兩溶液稀釋前的濃度相同
B.a、b、c三點溶液的pH由大到小順序為a>b>c
C.a點的Kw值比b點的Kw值大
D.a點水電離的c(H+)大于c點水電離的c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】物質分類是中學化學重要的學科思想。對“一些物質與水反應”的分類圖,請按要求填空:
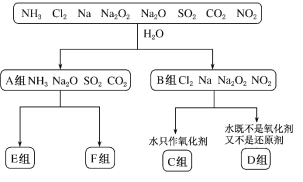
上述分類方法是________________;A組物質中屬于電解質的是_____(填化學式);C組物質與水反應的離子方程式為______________________________ ;D組物質與水反應中,氧化劑和還原劑物質的量之比為1∶2的物質是________ (填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】芳香化合物A是一種基本化工原料,可以從煤和石油中得到。OPA是一種重要的有機化工中間體。A、B、C、D、E、F和OPA的轉化關系如下所示:
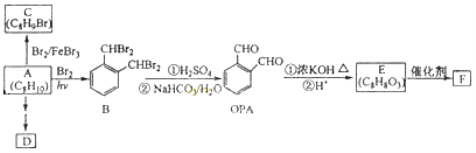
回答下列問題:
(1)A的化學名稱是 ;
(2)由A生成B 的反應類型是 。在該反應的副產物中,與B互為同分異構體的化合物的結構簡式為 ;
(3)寫出C所有可能的結構簡式 ;
(4)D(鄰苯二甲酸二乙酯)是一種增塑劑。請用A、不超過兩個碳的有機物及合適的無機試劑為原料,經兩步反應合成D。用化學方程式表示合成路線 ;
(5)OPA的化學名稱是 ,OPA經中間體E可合成一種聚酯類高分子化合物F,由E合成F的反應類型為 ,該反應的化學方程式為 。(提示![]() )
)
(6)芳香化合物G是E的同分異構體,G分子中含有醛基、酯基和醚基三種含氧官能團,寫出G所有可能的結構簡式
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com