
下表是元素周期表的一部分,除標出的元素外,表中的每個編號代表一種元素,請根據要求回答問題:
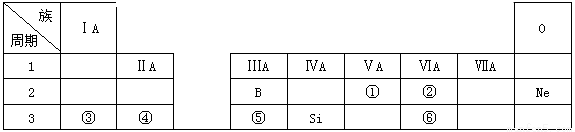
(1)①的元素符號是
(2)②和⑥兩種元素的原子半徑大小關系: (填“>”或“<”);
(3)③和⑤兩種元素的金屬性強弱關系: (填“>”或“<”);
(4)④的單質與⑥的最高價氧化物對應的水化物的稀溶液反應的離子方程式: 。
 勵耘書業暑假銜接寧波出版社系列答案
勵耘書業暑假銜接寧波出版社系列答案科目:高中化學 來源:2016屆陜西省高三下最后一次模擬理綜化學試卷(解析版) 題型:實驗題
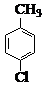
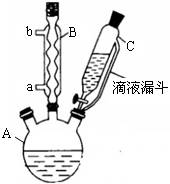
(14 分) 對氯苯甲酸是合成非甾族消炎鎮痛藥的中間體,還能用于燃料和農藥的合成,實驗室中制備對氯苯甲酸的反應、裝置圖如下:
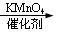
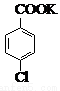 +MnO2
+MnO2 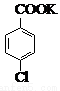
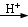
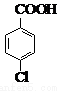
常溫條件下的有關數據如下表所示:
相對分子質量 | 熔點/℃ | 沸點/℃ | 密度/g·cm-3 | 顏色 | 水溶性 | |
對氯甲苯 | 126.5 | 7.5 | 162 | 1.07 | 無色 | 難溶 |
對氯苯甲酸 | 156.5 | 243 | 275 | 1.54 | 白色 | 微溶 |
對氯苯甲酸鉀 | 194.5 | 具有鹽的通性,屬于可溶性鹽 | ||||
實驗步驟:在規格為250mL的裝置A中加入一定量的催化劑、適量KMnO4、100mL水;安裝好裝置,在滴液漏斗中加入6.00mL對氯甲苯,在溫度為93℃左右時,逐滴滴入對氯甲苯;控制溫度在93℃左右,反應2h,過濾,將濾渣用熱水洗滌,使洗滌液與濾液合并,加入稀硫酸酸化,加熱濃縮;然后過濾,將濾渣用冷水進行洗滌,干燥后稱量其質量為7.19g。
請回答下列問題:
(1)裝置B的名稱是 。
(2)量取6.00mL對氯甲苯應選用的儀器是 。(填選儀器序號)
A.10mL量筒 B.50mL容量瓶 C.50mL酸式滴定管 D.50mL堿式滴定管
(3)控制溫度為93℃左右的方法是 。對氯甲苯的加入方法是逐滴加入而不是一次性加入,原因是 。
(4)第一次過濾的目的是 ,濾液中加入稀硫酸酸化,可觀察到的實驗現象是 。
(5)第二次過濾所得濾渣要用冷水進行洗滌,其原因是 。
(6)本實驗的產率是 (填標號)。A.60% B.70% C.80% D.90%
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三第九次月考化學試卷(解析版) 題型:填空題
己知合成氨反應在某溫度下2L的密閉容器中進行,測得如下數據:
N2(g)+3H2(g)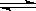 2NH3(g)△H=-92.60kJ/mol
2NH3(g)△H=-92.60kJ/mol

根據表中數據回答:
(1)反應進行到20min時放出的熱量為__________kJ。
(2)0-10min內的平均反應速率v(N2)為__________mol/(L·min)
(3)此溫度下該逆反應的化學平衡常數K(逆)=__________(保留兩位小數).
(4)反應達到平衡后,若往平衡體系中再加入N2、H2和NH3各1.00mol,化學平衡將__________(填“正向移動”或“逆向移動”或“不移動”)。
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省高三5月高考模擬理綜化學試卷(解析版) 題型:填空題
一定條件下,由CO2和H2制備甲醇的過程中含有下列反應:
反應1:CO2(g)+H2(g) CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1
反應2:CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
反應3:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH3
CH3OH(g)+H2O(g) ΔH3
其對應的平衡常數分別為K1、K2、K3,它們隨溫度變化的曲線如圖l所示。反應1、3的活化能如圖2所示。

(1)則ΔH2________ΔH3(填“大于”、“小于”或“等于”),理由是________。
(2)反應1中ΔS1______0(填>、=或<=),指出有利于自發進行的溫度條件____(填“較高溫度”或:“較低溫度”)
(3)將體積比為1:1的H2和CO2充入容積可變密閉容器內,若只進行反應1,下列措施中能使平衡時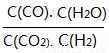 增大的是____________(填序號)
增大的是____________(填序號)
A.升高溫度B.增大壓強C.充入一定量的CO2 D.再加入一定量鐵粉
(4)為了提高CO2和H2制備甲醇生產效率和產量;工業生產中通常采取的措施是____________
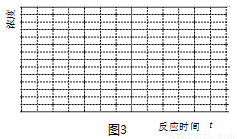
(5)在溫度為300℃時,使-定量合適體積比為的H2和CO2在體積恒定的密閉容器內進行反應。該溫度下反應2進行程度很小可看成不進行,請在圖3中畫出CO、CH3OH濃度隨時間變化至平衡的定性曲線圖。
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省高三5月高考模擬理綜化學試卷(解析版) 題型:選擇題
R、W、X、Y、Z為原子序數依次遞增的同一短周期元素,m、n均為正整數,下列說法正確的是
A.離子半徑:Rn+>Zm-
B.若Y的最高價氧化物對應的水化物HnYOm為強酸,則X的氫化物沸點一定比Y的氫化物的沸點低
C.若X的氣態氫化物能使濕潤的石蕊試紙變藍,則標準狀況下,18g Y的氫化物的體積為2.24 L
D.若R(OH)n為弱電解質,則W(OH)n+1可與KOH溶液反應
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省高二下期中文科化學試卷(解析版) 題型:選擇題
將一小段鎂帶投入到盛有稀鹽酸的試管中,發生劇烈反應。一段時間后,用手觸摸試管外壁感覺燙手。這個實驗事實說明該反應
A.為放熱反應 B.為吸熱反應
C.過程中熱能轉化為化學能 D.反應物的總能量低于生成物的總能量
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省高二下期中文科化學試卷(解析版) 題型:選擇題
我國是一個淡水資源比較匱乏的國家,右圖是海水淡化原理的一種示意圖,符合此原理的方法稱為
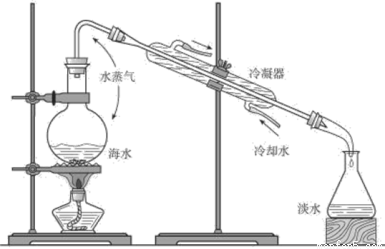
A.蒸餾法 B.電滲析法
C.離子交換法 D.太陽能蒸發法
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南師大附中高一下期中化學試卷(解析版) 題型:選擇題
已知三價鐵離子的氧化性比銅離子強。現將amol鐵和bmol銅的混合物與含有cmolHNO3的稀溶液充分反應,設還原產物為NO。下列結論:①若只有一種氧化產物,則3c=8a;②若只有二種氧化產物,被還原的硝酸物質的量為0.25c mol;③若有三種氧化產物,被還原的硝酸物質的量為0.25c mol;④若剩余金屬0.5a mol,則氧化產物為一種或二種。其中正確的組合是
A.只有② B.①② C.②③ D.③④
查看答案和解析>>
科目:高中化學 來源:2015-2016學年湖南省高一下期中化學試卷(解析版) 題型:選擇題
下列有關物質性質的說法錯誤的是
A.熱穩定性:H2O>H2S B.原子半徑:Na>Mg
C.酸性:H3PO4>H2SO4 D.還原性: I- >Cl-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com