
一定溫度下,向飽和NaOH溶液中加入一定量的鈉塊,充分反應后恢復到原來溫度,下列說法正確的是
A.溶液中溶質質量增加,溶劑質量減少,溶液中溶質的質量分數變大
B.溶液的pH不變,有氫氣放出
C.溶液中的Na+數目減小,有氧氣放出
D.溶液中的c(Na+)增大,有氫氣放出
科目:高中化學 來源:2016屆河北省高三9月月考化學試卷(解析版) 題型:選擇題
關于氧化鈉和過氧化鈉的敘述正確的是
A.都屬于堿性氧化物 B.溶于水后,所得水溶液的成分相同
C.都能和水發生化合反應 D.都可和二氧化碳反應生成不同的鹽
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省邯鄲市高二上第一次月考化學試卷(解析版) 題型:選擇題
下列說法正確的是
A.HCl溶液中無OH-
B.NaOH溶液中無H+
C.NaCl溶液中既無OH-,也無H+
D.常溫下,任何物質的稀溶液中都有H+和OH-,且Kw=c(H+)·c(OH-)=10-14
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省高三上學期第一次模擬考試化學試卷(解析版) 題型:填空題
(8分)丙烯是重要的化工原料,一定條件下可發生下列轉化:

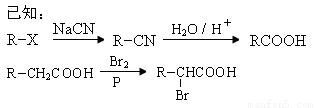
回答下列問題:
(1)以下化合物中含有羧基的是 。
A.化合物B B.化合物C C.化合物D D.化合物E
(2)上述反應中未涉及的反應類型是 。
A.取代反應 B.加成反應 C.還原反應 D.加聚反應
(3)寫出含碳數最少且與D互為同系物的有機物的結構簡式___________;寫出D與足量乙醇發生反應的化學方程式 。
查看答案和解析>>
科目:高中化學 來源:2016屆云南省高三上學期第一次月考化學試卷(解析版) 題型:填空題
(14分)常見的五種鹽A、B、C、D、E,它們的陽離子可能是Na+、NH4+、Cu2+、Ba2+、Al3+、Ag+、Fe3+,陰離子可能是Cl-、NO3-、SO42-、CO32-,已知:
①五種鹽均溶于水,水溶液均為無色。
②D的焰色反應呈黃色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈堿性。
④若在這五種鹽的溶液中分別加入Ba(NO3)2溶液,只有A、C的溶液不產生沉淀。
⑤若在這五種鹽的溶液中,分別加入氨水,E和C的溶液中生成沉淀,繼續加氨水,C中沉淀消失。
⑥把A的溶液分別加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
請回答下列問題。
(1)五種鹽中,一定沒有的陽離子是 ;所含陰離子相同的兩種鹽的化學式是 。
(2)D的化學式為 ,D溶液顯堿性的原因是(用離子方程式表示) 。
(3)A和C的溶液反應的離子方程式是 ;E和氨水反應的離子方程式是 。
(4)若要檢驗B中所含的陽離子,正確的實驗方法是 。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省齊魯教科研協作體19所高三上學期第一次聯考化學試卷(解析版) 題型:填空題
(6分)T℃時,向體積為2L的恒容密閉容器中充入4molA和2molB氣體,發生如下反應:4A(g)+B(g)  xC(g),保持溫度不變,5min時反應達到平衡狀態,剩余1.6 molB,并測得C的濃度為0.8mol/L,請填寫下列空白:
xC(g),保持溫度不變,5min時反應達到平衡狀態,剩余1.6 molB,并測得C的濃度為0.8mol/L,請填寫下列空白:
(1)x=__________,該反應平衡常數的表達式為:K= 。
(2)該溫度下,此反應達到平衡時,A的轉化率為α(A)= 。
(3)在T℃時,若向原平衡混合物的容器中再充入amolC,同時改變容器體積保持壓強不變,欲使達到新的平衡時,各物質的體積分數與原平衡相同,則應再充入________molB (用a表示)。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省齊魯教科研協作體19所高三上學期第一次聯考化學試卷(解析版) 題型:選擇題
當我們查看葡萄酒標簽上的成分信息時,常發現其成分中含有少量SO2。下列關于SO2說法正確的是
A.SO2屬于非法添加劑,不該添加到葡萄酒中
B.SO2具有還原性,少量的SO2可防止葡萄酒氧化變質
C.SO2具有還原性,不能用濃硫酸干燥
D.SO2可以使酸性KMnO4溶液褪色,體現了它的漂白性
查看答案和解析>>
科目:高中化學 來源:2016屆甘肅省張掖市高三上學期第一次質量檢測化學試卷(解析版) 題型:填空題
煤化工中兩個重要反應為①C(s)+H2O(g)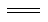 H2(g)+CO(g) ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g)
H2(g)+CO(g) ΔH=+131.3 kJ·mol-1,②CO(g)+ H2O(g) CO2(g) + H2(g)。
CO2(g) + H2(g)。
(1)下列說法正確的是 。
A.當反應①的容器中混合氣體的密度不再變化時反應達到最大限度
B.反應②的熵變△S >0
C.反應①中增加C固體的量能增大反應速率
D.在反應中②及時分離出產生的H2對正反應速率無影響
(2)若工業上要增加反應①的速率,最經濟的措施為 。
(3)現將不同量的CO(g)和H2O(g)分別通入2L恒容密閉容器中進行反應,得到如下三組數據:
實驗組] | 溫度/℃ | 起始量/mol | 平衡量/mol | 達到平衡所 需時間/ min | ||
CO | H2O | H2 | CO2 | |||
I | 650 | 4 | 2 | 1.6 | 1.6 | 5 |
Ⅱ | 900 | 2 | 1 | 0.5 | 0.5 | 3 |
Ⅲ | 900 | a | b | c | d | t |
①實驗I中,從反應開始到反應達到平衡時,H2O的平均反應速率為___。
②CO(g)和H2O(g)反應的△H 0(填“大于”、“小于”或“等于”)
③實驗III中,若平衡時,CO的轉化率大于水蒸氣,則a、b必須滿足的關系是_____,與實驗Ⅱ相比,化學平衡常數 (填“增大”、“減小”或“不變”)。
④若在900℃時,實驗II反應達到平衡后,向此容器中再加入1 mol CO、0.5 mol H2O、0.2 mol CO2、0.5 mol H2,平衡向________方向移動(填“正反應”、“逆反應”“不移動”)。
(4)CO、H2可用于甲醇和甲醚,其反應為(m、n均大于0):
反應①:CO(g)+2H2(g) CH3OH(g) ΔH= -mkJ·mol-1
CH3OH(g) ΔH= -mkJ·mol-1
反應②: 2CO(g)+4 H2(g) CH3OCH3(g) +H2O(g) ΔH=-nkJ·mol-1
CH3OCH3(g) +H2O(g) ΔH=-nkJ·mol-1
反應③:2CH3OH(g) CH3OCH3(g)+ H2O(g) △H<0
CH3OCH3(g)+ H2O(g) △H<0
則m與n的關系為 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省高二上學期第一次月考化學試卷(解析版) 題型:填空題
(8分)紅磷P(s)和Cl2(g)發生反應生成PCl3(g)和PCl5(g)。反應過程和能量關系如圖所示(圖中的ΔH表示生成1 mol產物的數據)。根據圖回答下列問題:
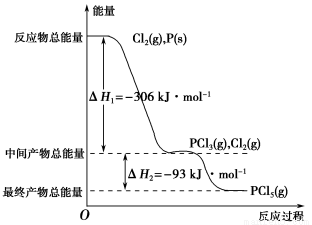
(1)P和Cl2反應生成PCl3的熱化學方程式是 。
(2)PCl5分解成PCl3和Cl2的熱化學方程式是 。
(3)P和Cl2分兩步反應生成1 mol PCl5的ΔH3=____________,P和Cl2一步反應生成1mol PCl5的ΔH4____ΔH3(填“大于”“小于”或“等于”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com