
準確稱取6g鋁土礦(含Al2O3,Fe2O3,SiO2)樣品,放入盛有100mL某濃度的H2SO4溶液的燒杯中,充分反應后過濾,向濾液中加入10mol·L-1 NaOH溶液,產生沉淀的量(g)與所加入NaOH溶液的體積(mL)的關系如圖所示:
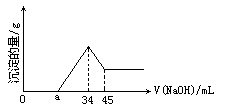
(1)H2SO4溶液的物質的量濃度是多少?
(2)若a=2.3,則鋁土礦中各組成成分的質量分數分別是多少?
(3)a值的范圍應在________之間;在該范圍內,a值越大,鋁土礦中的Fe2O3,SiO2含量變化是________.
|
(1)c(H2SO4)=1.75mol·L-1 (2)Al2O3 85%,Fe2O3 12%,SiO2 3% (3)1.625<a<5,Fe2O3的含量越小,SiO2的含量越大 導解:(1)由圖像可知,當加入35mL NaOH溶液時,濾液中過量的H2SO4被中和,且Fe3+,Al3+全部沉淀,溶液中只存在Na2SO4. Na2SO4~2NaOH~H2SO4 n(H2SO4)= c(H2SO4)= 由圖像可知,加入NaOH在35~45mL之間時,發生如下反應:Al(OH)3+NaOH 有Al2O3~2Al(OH)2~2NaOH, n(Al2O3)=(45-35)×10-3×10× ω(Al2O3)=0.05×102× 沉淀Al3+消耗NaOH為: n(NaOH)=3n(Al3+)=3×0.05×2=0.3mol. (2)沉淀Fe3+消耗NaOH為: 10×(35-a)×10-3-0.3=(0.05-0.01a)mol, 所以,n(Fe3+)= ω(Fe2O3)=0.009× 則SiO2的質量分數=1-85%-12%=3%. (3)因Al2O3的質量分數與a值無關,即為85%,則Fe2O3的質量分數必須滿足:0<40×(5-a)/a%<15%, 1.625<a<5, a值越大,Fe2O3的含量越小,SiO2的含量越大. |


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案科目:高中化學 來源: 題型:
 準確稱取6g鋁土礦(含Al2O3、Fe2O3、SiO2)樣品,放入盛有100mL 稀H2SO4溶液的燒杯中,充分反應后過濾去掉沉淀,向濾液中加入10mol/L的NaOH溶液,產生沉淀的質量和加入的NaOH溶液的體積(mL)如圖所示.試回答下列問題:
準確稱取6g鋁土礦(含Al2O3、Fe2O3、SiO2)樣品,放入盛有100mL 稀H2SO4溶液的燒杯中,充分反應后過濾去掉沉淀,向濾液中加入10mol/L的NaOH溶液,產生沉淀的質量和加入的NaOH溶液的體積(mL)如圖所示.試回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
 (1)現有含Fe2O380%的赤鐵礦100t,理論上可冶煉含Fe95%的生鐵多少噸?
(1)現有含Fe2O380%的赤鐵礦100t,理論上可冶煉含Fe95%的生鐵多少噸?查看答案和解析>>
科目:高中化學 來源: 題型:
(16分)鋁土礦(主要成分為Al2O3,還含有SiO2、Fe2O3)是工業上制備氧化鋁的主要原料。工業上提取氧化鋁的工藝流程如下:
(1)沉淀A、B的成分分別是 、 ;
(2)步驟②中的試劑a是 ;
(3)試寫出步驟③中發生反應的離子方式 ;
(4)在實驗室模擬上述實驗過程中,需要用到一定濃度的鹽酸溶液。在配制250mi。該鹽酸溶液時,某同學轉移溶液的操作如圖所示,圖中的主要錯誤是:
① ;
② 。
(4)準確稱取6g鋁土礦樣品,加入100mL鹽酸溶液,充分反應后向濾液中加入10 mol·L-1試劑a的溶液,產生沉淀的質量與加入試劑a的體積關系如圖所示,則所用鹽酸溶液的物質的量濃度為 ,樣品中Al2O3的百分含量為 。
查看答案和解析>>
科目:高中化學 來源:2010年山東省諸城一中高三上學期第一次月考(化學) 題型:填空題
(16分)鋁土礦(主要成分為Al2O3,還含有SiO2、Fe2O3)是工業上制備氧化鋁的主要原料。工業上提取氧化鋁的工藝流程如下:
(1)沉淀A、B的成分分別是 、 ;
(2)步驟②中的試劑a是 ;
(3)試寫出步驟③中發生反應的離子方式 ;
(4)在實驗室模擬上述實驗過程中,需要用到一定濃度的鹽酸溶液。在配制250mi。該鹽酸溶液時,某同學轉移溶液的操作如圖所示,圖中的主要錯誤是:
① ;
② 。
(4)準確稱取6g鋁土礦樣品,加入100mL鹽酸溶液,充分反應后向濾液中加入10 mol·L-1試劑a的溶液,產生沉淀的質量與加入試劑a的體積關系如圖所示,則所用鹽酸溶液的物質的量濃度為 ,樣品中Al2O3的百分含量為 。
查看答案和解析>>
科目:高中化學 來源:2010-2011學年廣東省梅州市高三上學期期末考試(理綜)化學部分 題型:填空題
鋁土礦(主要成分為Al2O3,還含有SiO2、Fe2O3)是工業上制備氧化鋁的主要原料。工業上提取氧化鋁的工藝流程如下:

(1)沉淀 A、B的成分分別是 、 ;
(2)步驟②中的試劑a是 ;
(3)試寫出步驟③中發生反應的離子方式 ;
(4)準確稱取6g鋁土礦樣品,加入100mL鹽酸溶液,充分反應后向濾液中加入10 mol·L-1試劑a的溶液,產生沉淀的質量與加入試劑a的體積關系如下圖所示,則所用鹽酸溶液的物質的量濃度為 ,樣品中Al2O3的百分含量為 。

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com