
【題目】催化還原CO2是解決溫室效應及能源問題的重要手段之一。研究表明,在Cu/ZnO催化劑存在下,CO2和H2可發生兩個平衡反應,分別生成CH3OH和CO。反應的熱化學方程式如下:
CO2(g)+3 H2(g)![]() CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CH3OH(g)+H2O(g)ΔH1=-53.7kJ·mol-1 I
CO2(g)+ H2(g)![]() CO(g)+H2O(g)ΔH2 II
CO(g)+H2O(g)ΔH2 II
某實驗室控制CO2和H2初始投料比為1:2.2,經過相同反應時間測得如下實驗數據:

【備注】Cat.1:Cu/ZnO納米棒;Cat.2:Cu/ZnO納米片;甲醇選擇性:轉化的CO2中生成甲醛的百分比
已知:①CO和H2的標準燃燒熱分別為-283.0kJ·mol-1和-285.8kJ·mol-1
②H2O(l)![]() H2O(g) ΔH3=44.0kJ·mol-1
H2O(g) ΔH3=44.0kJ·mol-1
請回答(不考慮溫度對ΔH的影響):
(1)反應I的平衡常數表達式K= ;反應II的ΔH2= kJ·mol-1。
(2)有利于提高CO2轉化為CH3OH平衡轉化率的措施有 。
A.使用催化劑Cat.1
B.使用催化劑Cat.2
C.降低反應溫度
D.投料比不變,增加反應物的濃度
E.增大CO2和H2的初始投料比
(3)表中實驗數據表明,在相同溫度下不同的催化劑對CO2轉化成CH3OH的選擇性有顯著的影響,其原因是 。
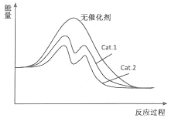
(4)在右圖中分別畫出I在無催化劑、有Cat.1和由Cat.2三種情況下“反應過程-能量”示意圖。

(5)研究證實,CO2也可在酸性水溶液中通過電解生成甲醇,則生成甲醇的反應發生在___ 極,該電極反應式是 。
【答案】(1)c(CH3OH)×c(H2O)/[c(CO2)×c3(H2)], +41.2;(2)CD;(3)表中數據表明此時反應未達到平衡,不同的催化劑對反應Ⅰ的催化能力不同,因而在該時刻下對甲醇選擇性有影響;
(4) ;(5)陰,CO2+6H++6e-==CH3OH+H2O。
;(5)陰,CO2+6H++6e-==CH3OH+H2O。
【解析】
試題分析:(1)根據化學平衡常數定義,K= c(CH3OH)×c(H2O)/[c(CO2)×c3(H2)],CO的燃燒熱:CO(g)+1/2O2(g)=CO2(g) △H=-283.0kJ·mol-1 ①,H2燃燒熱:H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ·mol-1 ②,H2O(l)=H2O(g) △H=+44.0kJ·mol-1 ③,②+③-①得出:CO2(g)+H2(g)=CO(g)+H2O(g) △H=(44-285.8+283.0)kJ·mol-1=+41.2kJ·mol-1;(2)使用催化劑,對化學平衡無影響,只提高化學反應速率,故選項AB錯誤;C、CO2→CH3OH,此反應是放熱反應,根據勒夏特列原理,降低溫度,平衡向正反應方向移動,CO2的轉化率提高,故正確;D、投料比不變,增加反應物的濃度,根據勒夏特列原理,提高反應物的濃度,平衡向正反應方向移動,CO2的轉化率提高,故正確;E、增大CO2和H2的初始投料比,是提高CO2的量,雖然平衡向正反應方向移動,但CO2的轉化率降低,故錯誤;(3)因為催化劑對化學平衡無影響,因此表中數據表明此時反應未達到平衡,不同的催化劑對反應Ⅰ的催化能力不同,因而在該時刻下對甲醇選擇性有影響;(4)催化劑降低活化分子的活化能,根據表格數據,Cat.2的甲醇選擇性大于Cat.1,因此圖像是: ;(5)CO2中C的化合價為+4價,甲醇中C的化合價為-2價,化合價降低,根據電解原理,甲醇應在陰極上產生,因此電極反應式為:CO2+6H++6e-=CH3OH+H2O。
;(5)CO2中C的化合價為+4價,甲醇中C的化合價為-2價,化合價降低,根據電解原理,甲醇應在陰極上產生,因此電極反應式為:CO2+6H++6e-=CH3OH+H2O。


 捷徑訓練檢測卷系列答案
捷徑訓練檢測卷系列答案 小夫子全能檢測系列答案
小夫子全能檢測系列答案科目:高中化學 來源: 題型:
【題目】硫酸亞鐵銨[(NH4)2Fe(SO4)2]是一種重要的工業原料,能溶于水,不溶于乙醇,其工業制法如下。請回答:
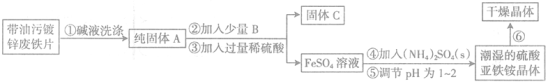
(1)步驟①中堿液洗滌的目的是 。若將堿液換為酸液,可能產生的問題是_ 。
(2)步驟②中B可以是 (填字母),加入少量B的目的是 。
a.CuCl2 b.CuO c.Cu(NO3)2 d.CuSO4
(3)步驟⑥中要用到少量乙醇洗滌,其目的是 。
(4)用硫酸亞鐵按晶體配制溶液時,需加入一定量硫酸,目的是 。工業上常用酸性KMnO4溶液通過滴定的方法測定硫酸亞鐵銨樣品的純度,反應的離子方程式為 。準確量取硫酸亞鐵銨溶液時,硫酸亞鐵銨溶液應盛放于 (填“酸式”或“堿式”)滴定管中。
(5)硫酸亞鐵銨晶體的樣品中可能含有的雜質離子是 ,實驗室的檢驗方法是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】2015年科學家首次利用X射線觀測到化學反應過渡態的形成。在固體催化劑表面“抓取”CO分子和O原子,并“配對”生成CO2分子。 下列關于說法正確的是

A.CO與CO2均為酸性氧化物
B.大量CO2的排放可導致酸雨的形成
C.CO與O形成化學鍵過程中有電子轉移
D.相同條件下,CO的密度比CO2的密度大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鐵炭混合物(鐵屑和活性炭的混合物)、納米鐵粉均可用于處理水中污染物。
(1)鐵炭混合物在水溶液中可形成許多微電池。將含有Cr2O72-的酸性廢水通過鐵炭混合物,在微電池正極上Cr2O72-轉化為Cr3+,其電極反應式為_____________。
(2)在相同條件下,測量總質量相同、鐵的質量分數不同的鐵炭混合物對水中Cu2+和Pb2+的去除率,結果如圖所示0。
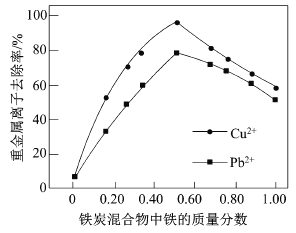
①當鐵炭混合物中鐵的質量分數為0時,也能去除水中少量的Cu2+和Pb2+,其原因是__________。
②當鐵炭混合物中鐵的質量分數大于50%時,隨著鐵的質量分數的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是_____________。
(3)納米鐵粉可用于處理地下水中的污染物。
①一定條件下,向FeSO4溶液中滴加堿性NaBH4溶液,溶液中BH4-(B元素的化合價為+3)與Fe2+反應生成納米鐵粉、H2和B(OH)4-,其離子方程式為 。
②納米鐵粉與水中NO3-反應的離子方程式為4Fe+NO3-+10H+=4Fe2++NH4++3H2O
研究發現,若pH偏低將會導致NO3-的去除率下降,其原因是 。
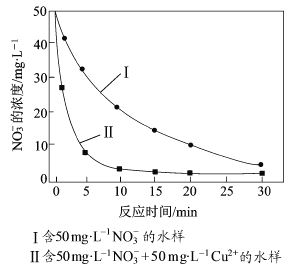
③相同條件下,納米鐵粉去除不同水樣中NO3-的速率有較大差異(見右圖),產生該差異的可能原因是 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以NaCl、CO2、NH3為原料發生反應,制得NaHCO3和NH4Cl是“侯氏制堿法”的重要步驟。相關物質的溶解度曲線如圖所示。下列說法不正確的是
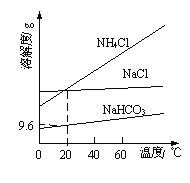
A.將NaHCO3加熱分解可得純堿
B.常溫下碳酸氫鈉的溶解度大于碳酸鈉
C.采用蒸發結晶從溶液中分離出NaHCO3
D.20℃時,NaHCO3飽和溶液的物質的量濃度約為1.1mol/L
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鯊魚是世界上唯一不患癌癥的動物,科學研究表明,鯊魚體內含有一種角鯊烯,具有抗癌性.已知角鯊烯分子中含有30個碳原子及6個C=C且不含環狀結構,則其分子式為( )
A.C30H60 B.C30H56 C.C30H52 D.C30H50
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】CuCl廣泛應用于化工和印染等行業。某研究性學習小組擬熱分解CuCl2·2H2O制備CuCl,并進行相關探究。
【資料查閱】
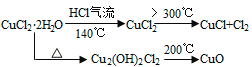
【實驗探究】該小組用下圖所示裝置進行實驗(夾持儀器略)。
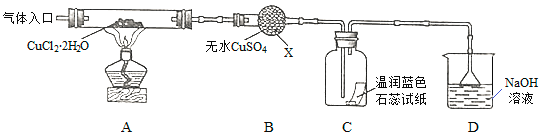
請回答下列問題:
(1)儀器X的名稱是__________。
(2)實驗操作的先后順序是a→______→c(填操作的編號)
a.檢查裝置的氣密性后加入藥品
b.熄滅酒精燈,冷卻
c.在“氣體入口”處干燥HCl
d.點燃酒精燈,加熱
e.停止通入HCl,然后通入N2
(3)在實驗過程中,觀察到B中物質由白色變為藍色,C中試紙的顏色變化是_______。
(4)裝置D中發生的氧化還原反應的離子方程式是________________。
(5)反應結束后,取出CuCl產品進行實驗,發現其中含有少量的CuCl2或CuO雜質,根據資料信息分析:
①若雜質是CuCl2,則產生的原因是________________。
②若雜質是CuO,則產生的原因是________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】從某些反應看,NH3和H2O、NH4+和H3O+、NH2—和OH-、N3-和O2-兩兩類似。據此判斷下列反應正確的是
①CaO+2NH4Cl===CaCl2+2NH3↑+H2O②2Na+2NH3===2NaNH2+H2↑
③3Mg(NH2)2===Mg3N2+4NH3↑④NH4Cl+NaNH2===NaCl+2NH3↑
A.只有③
B.只有①
C.①和②
D.都正確
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列說法不正確的是( )
A. 二氧化硅可制玻璃、單質硅、光導纖維;
B. 食鹽、糖、醋可作調味劑,不可作食品防腐劑;
C. 金屬腐蝕的本質是金屬原子失電子被氧化的過程;
D. 大量服用阿司匹林會出現水楊酸中毒癥,可靜脈滴注NaHCO3溶液。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com