
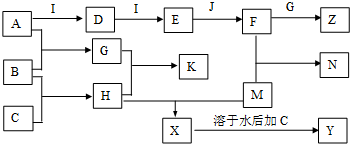
分析 A、B、C、D、E、G、H、I均為氣體,A、B、C、I、M為單質,根據題中各物質轉化關系,A和B反應生成G,B和C反應生成H,G和H相遇時產生白煙,則該反應為氨氣與氯化氫的反應,所以K為NH4Cl,B為H2,A能與I連續反應,且E與J反應,J為常見的液態物質,所以I為O2,J為H2O,則A為N2,所以G為NH3,則H為HCl,D為NO,E為NO2,F為HNO3,F和G反應生成Z為NH4NO3,M能與H鹽酸反應生成X,X可以繼續與C反應,且M為常用金屬,則M為Fe,所以X為FeCl2,Y為FeCl3,鐵與硝酸反應生成N為Fe(NO3)3,據此答題.
解答 解:A、B、C、D、E、G、H、I均為氣體,A、B、C、I、M為單質,根據題中各物質轉化關系,A和B反應生成G,B和C反應生成H,G和H相遇時產生白煙,則該反應為氨氣與氯化氫的反應,所以K為NH4Cl,B為H2,A能與I連續反應,且E與J反應,J為常見的液態物質,所以I為O2,J為H2O,則A為N2,所以G為NH3,則H為HCl,D為NO,E為NO2,F為HNO3,F和G反應生成Z為NH4NO3,M能與H鹽酸反應生成X,X可以繼續與C反應,且M為常用金屬,則M為Fe,所以X為FeCl2,Y為FeCl3,鐵與硝酸反應生成N為Fe(NO3)3,
(1)根據上面的分析可知,A為N2,K為NH4Cl,Z為NH4NO3,故答案為:N2;NH4Cl;NH4NO3;
(2)①實驗室用氯化銨與氫氧化鈣反應制取氨氣,反應的化學方程式為2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案為:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
②實驗室檢驗氨氣是否收集滿的方法可以用濕潤的紅色石蕊試紙置于集氣瓶口,如果紅色石蕊試紙變藍,則說明收集滿,
故答案為:用濕潤的紅色石蕊試紙置于集氣瓶口,如果紅色石蕊試紙變藍,則說明收集滿;
③氨氣在一定條件下催化氧化也可生成NO,該反應的化學方程式為4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6H2O,故答案為:4NH3+5O2$\frac{\underline{催化劑}}{△}$4NO+6 H2O;
(3)過量的鐵與稀硝酸反應生成硝酸亞鐵,反應的離子方程式為3Fe+8H++2NO3-(稀)═3Fe2++2NO↑+4H2O,
故答案為:3Fe+8H++2NO3-(稀)═3Fe2++2NO↑+4H2O;
(4)檢驗FeCl3中的氯離子的方法為取少量樣品試液,滴入硝酸酸化的硝酸銀溶液,如果有白色沉淀產生,則說明原溶液中有氯離子,
故答案為:取少量樣品試液,滴入硝酸酸化的硝酸銀溶液,如果有白色沉淀產生,則說明原溶液中有氯離子;
(5)①濃硝酸與木炭在加熱的條件下反應,反應的化學方程式為C+4HNO3(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20,
故答案為:C+4HNO3(濃)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H20;
②濃硝酸部分分解,溶液中含有少量的二氧化氮,所以溶液呈黃色,其化學方程式為4HNO3(濃)=O2+4NO2+2H20,
故答案為:4HNO3(濃)=O2+4NO2+2H20;
③若要消除黃色可向其中通入一定量的氧氣,二氧化氮、氧氣、水反應生成硝酸,故答案為:氧氣.
點評 本題考查無機物的推斷,明確物質的顏色及性質是解答本題的關鍵,注意B、K是解答本題的突破口,并規范化學用語的應用,題目難度中等.


 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案科目:高中化學 來源: 題型:選擇題
| A. | 還原性:X的氫化物>Y的氫化物>Z的氫化物 | |
| B. | 簡單離子的半徑:M的離子>Z的離子>Y的離子>X的離子 | |
| C. | YX2與M2Y的水溶液在酸性條件下不能反應 | |
| D. | Z元素最高價氧化物對應的水化物的化學式為HZO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
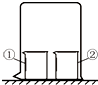 用圖所示裝置進行下列實驗,實驗結果與預測現象不一致的是( )
用圖所示裝置進行下列實驗,實驗結果與預測現象不一致的是( )| 選項 | ①中物質 | ②中物質 | 預測現象 |
| A | 酚酞溶液 | 濃氨水 | ①中無色變紅色 |
| B | CCl4 | 液溴 | ①中變橙色 |
| C | 濃氨水 | 濃硫酸 | 空氣中產生白煙 |
| D | NaAlO2溶液 | 濃鹽酸 | ①中有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | FeCl3 | B. | 濃硫酸 | C. | NaCl | D. | NaNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在化學反應進行的過程中放出或吸收的熱量稱為反應熱 | |
| B. | 在稀溶液中,1mol酸跟1mol堿發生中和反應所放出的熱量叫做中和熱 | |
| C. | 氫氧化鋇晶體與氯化銨晶體混合是吸熱反應 | |
| D. | 化學反應中的能量變化與參加反應的物質的量成正比 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 ,B為18電子分子,其結構式為
,B為18電子分子,其結構式為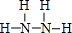 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 25℃時,0.1mol•L-1HF溶液中pH=1 | |
| B. | Ksp(CaF2)隨溫度和濃度的變化而變化 | |
| C. | 該體系中沒有沉淀產生 | |
| D. | 該體系中有CaF2產生沉淀 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com