
| A. | ②③④⑥⑦ | B. | ②③⑤⑦ | C. | ①③⑦ | D. | ①②③④⑥ |
分析 ①Zn和濃硫酸反應生成硫酸鋅、二氧化硫,和稀硫酸反應生成硫酸鋅和氫氣;
②過量的氫氣與少量的氮氣在催化劑存在下充分反應,該反應存在可逆性;
③MnO2與濃鹽酸在加熱條件下反應生成氯氣,和稀鹽酸不反應;
④加熱條件下,Cu和濃硫酸反應,和稀硫酸不反應;
⑤過量稀硝酸與鐵反應生成硝酸鐵和NO;
⑥過量的水與一定量的氯氣反應生成HCl和HClO,該反應存在可逆性;
⑦常溫下,Al和濃硫酸發生鈍化現象.
解答 解:①Zn和濃硫酸反應生成硫酸鋅、二氧化硫,和稀硫酸反應生成硫酸鋅和氫氣,所以過量的鋅和濃硫酸反應時,濃硫酸能完全反應,故不選;
②過量的氫氣與少量的氮氣在催化劑存在下充分反應,該反應存在可逆性,所以一種物質過量,另一種物質仍不能完全反應,故選;
③MnO2與濃鹽酸在加熱條件下反應生成氯氣,和稀鹽酸不反應,所以一種物質過量,另一種物質仍不能完全反應,故選;
④加熱條件下,Cu和濃硫酸反應,和稀硫酸不反應,所以一種物質過量,另一種物質仍不能完全反應,故選;
⑤過量稀硝酸與鐵反應生成硝酸鐵和NO,所以不存在稀硝酸過量,鐵不完全反應現象,故不選;
⑥過量的水與一定量的氯氣反應生成HCl和HClO,該反應存在可逆性,所以存在一種物質過量,另一種物質仍不能完全反應,故選;
⑦常溫下,Al和濃硫酸發生鈍化現象而導致鋁、濃硫酸都不完全反應,所以存一種物質過量,另一種物質仍不能完全反應,故選;
故選A.
點評 本題考查物質之間反應,為高頻考點,明確物質性質、反應條件是解本題關鍵,注意有些化學反應與反應物的量、反應物濃度、反應條件有關,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 向Ba(OH)2溶液中滴加稀硫酸:Ba2++2OH-+2H++SO${\;}_{4}^{2-}$═BaSO4↓+2H2O | |
| B. | 酸性介質中KMnO4氧化H2O2:2MnO${\;}_{4}^{-}$+5H2O2+6H+═2Mn2++5O2↑+8H2O | |
| C. | 0.01mol•L-1NH4Al(SO4)2溶液與0.02mol•L-1Ba(OH)2溶液等體積混合:NH${\;}_{4}^{+}$+Al5++SO${\;}_{4}^{2-}$+Ba2++4OH-═BaSO4↓+Al(OH)5↓+NH5•H2O | |
| D. | 鉛蓄電池充電時的正極反應:PbSO4+2H2O-2e-═PbO2+4H++SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示.下列描述正確的是( )
一定溫度下,在2L的密閉容器中,X、Y、Z三種氣體的物質的量隨時間變化的曲線如圖所示.下列描述正確的是( )| A. | 反應開始到10s時,用Z表示的反應速率為0.158 mol•(L•s)-1 | |
| B. | 反應開始到10s時,X的物質的量濃度減少了0.79 mol•L-1 | |
| C. | 反應的化學方程式為X(g)+Y(g)?2Z(g) | |
| D. | 反應開始到10 s時,Y的轉化率為39.5% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
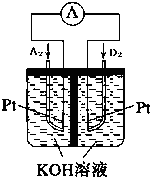 A、B、C、D、E、F、G均為短周期元素,原子序數依次遞增.A元素原子核內無中子,B元素原子最外層電子數是次外層電子數的2倍,D是地殼中含量最多的元素,E是短周期中金屬性最強的元素,F與G位置相鄰,G是同周期元素中原子半徑最小的元素.請用化學用語回答:
A、B、C、D、E、F、G均為短周期元素,原子序數依次遞增.A元素原子核內無中子,B元素原子最外層電子數是次外層電子數的2倍,D是地殼中含量最多的元素,E是短周期中金屬性最強的元素,F與G位置相鄰,G是同周期元素中原子半徑最小的元素.請用化學用語回答: .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 .
. 生成
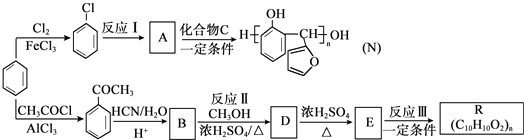
生成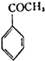 的反應類型是取代反應,D生成E的過程中,濃硫酸的作用催化劑和吸水劑.
的反應類型是取代反應,D生成E的過程中,濃硫酸的作用催化劑和吸水劑. .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
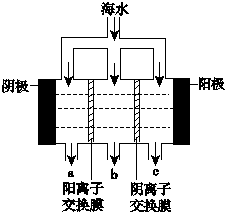 《科學》曾評出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一種重要的自然資源,是人類賴以生存不可缺少的物質.水質優劣直接影響人體健康.海洋是化學資源寶庫,海洋資源的綜合利用具有廣闊的前景.人類把海水淡化,就可以得到大量的飲用水,常規蒸餾法,技術和工藝比較完備,但也存在較大缺陷,大量推廣離子交換法和電滲析法.
《科學》曾評出10大科技突破,其中“火星上‘找’到水的影子”名列第一.水是一種重要的自然資源,是人類賴以生存不可缺少的物質.水質優劣直接影響人體健康.海洋是化學資源寶庫,海洋資源的綜合利用具有廣闊的前景.人類把海水淡化,就可以得到大量的飲用水,常規蒸餾法,技術和工藝比較完備,但也存在較大缺陷,大量推廣離子交換法和電滲析法.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
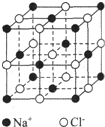
| A. | 2Na:兩個鈉元素 | |
| B. | 2OH-:兩個氫氧根離子 | |
| C. | $\stackrel{+2}{M}$g:鎂元素的化合價為+2價 | |
| D. | NO2:一個二氧化氮分子含有兩個氧原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
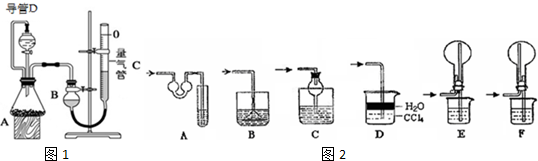
| 實驗 | 藥品 | 制取氣體 | 量氣管中的液體 |
| Ⅰ | Cu、稀HNO3 | H2O | |
| Ⅱ | NaOH固體、濃氨水 | NH3 | |
| Ⅲ | 鎂鋁合金、足量NaOH溶液 | H2 | H2O |
| 編號 | 鎂鋁合金質量 | 量氣管第一次讀數 | 量氣管第二次讀數 |
| ① | 1.0g | 10.0mL | 376.6mL |
| ② | 1.0g | 10.0mL | 364.7mL |
| ③ | 1.0g | 10.0mL | 377.0mL |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com