
【題目】甲醇(CH3OH)的合成與應用具有廣闊的發(fā)展前景。
Ⅰ.合成甲醇的部分工藝流程如下:
![]()
(1)甲烷與水蒸氣反應制備合成甲醇的原料氣CO、CO2和H2。CH4(g)+H2O(g)=CO(g)+3H2(g) 、H =+206.2 kJ·mol-1,CO(g) + H2O(g) =CO2(g) + H2(g)H =41.0 kJ·mol-1,甲烷與水蒸氣反應生成CO2和H2的熱化學方程式為________。
(2)在催化劑的作用下,200~300℃時,合成反應器內(nèi)發(fā)生反應:ⅰ. CO(g)+2H2(g)![]() CH3OH(g)H<0,ⅱ.CO2(g)+3H2(g)
CH3OH(g)H<0,ⅱ.CO2(g)+3H2(g)![]() CH3OH(g) + H2O(g)H<0。
CH3OH(g) + H2O(g)H<0。
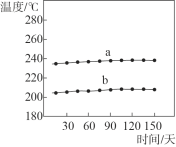
①一段時間內(nèi),記錄合成反應器出、入口樣品的溫度,數(shù)據(jù)如圖所示。曲線_________是合成反應器出口樣品的溫度。
②如果你是工程師,請對合成反應器中壓強的控制提出建議并說明理由:_______。合成反應器中有少量的副反應,會生成二甲醚(CH3OCH3)、甲酸甲酯等。已知沸點:甲醇 64.7℃;二甲醚 -24.9℃;甲酸甲酯32.0℃。
③CO和H2生成二甲醚的化學方程式是_________。
④從合成反應器出來的產(chǎn)品經(jīng)分離提純可以得到甲醇,請簡述該方法_______。
Ⅱ.下圖為甲醇燃料電池的示意圖。
(3)①負極的電極反應式是_______。
②質(zhì)子交換膜材料的合成是燃料電池的核心技術。我國科研人員研發(fā)的一種質(zhì)子交換膜材料的結(jié)構(gòu)片段如下,它由三種單體縮聚而成。
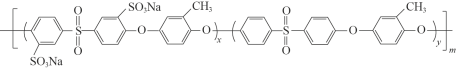
已知:ROH + R’Cl → R—O—R’ + HCl,單體的結(jié)構(gòu)簡式是: 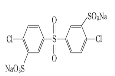 、 _____、___。
、 _____、___。
【答案】CH4(g) + 2H2O(g) =CO2(g) + 4H2(g) H = +165.2kJ·mol-1 a 適當加壓。加壓能使該反應速率增大、原料轉(zhuǎn)化率升高,也會增加設備和動力成本 2CO+4H2 ![]() CH3OCH3+ H2O 降溫冷凝得到液態(tài)甲醇粗品再蒸餾提純 CH3OH-6e-+H2O = CO2+6H+
CH3OCH3+ H2O 降溫冷凝得到液態(tài)甲醇粗品再蒸餾提純 CH3OH-6e-+H2O = CO2+6H+ 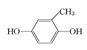
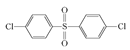 或
或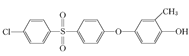
【解析】
I、(1)應用蓋斯定律寫出熱化學方程式;
(2)①兩個反應都是放熱反應,合成反應器出口樣品的溫度更高一些;
②兩個反應都是氣體體積減小的反應,從平衡的角度來看,高壓更合適,但是壓強高,意味著設備要好,這就需要加大成本的投入,因此需要適當加壓;
③題中告知反應物和生成物,寫完整方程式即可;
④題中給出了幾個物質(zhì)的沸點,甲醇的沸點較高,且和其他物質(zhì)的沸點相差較大,可以通過降溫冷凝的方法得到甲醇;
II、(3)①燃料電池的構(gòu)造中有質(zhì)子交換膜,則說明反應中產(chǎn)生H+,故負極電極反應為:CH3OH-6e-+H2O=CO2+6H+;
②結(jié)合題中給出的方程式分析即可。
I、(1)根據(jù)蓋斯定律,將兩個熱化學方程式加起來得:CH4(g)+2H2O(g)=CO2(g)+4H2(g) H=+165.2kJ·mol-1;
(2)①兩個反應都是放熱反應,合成反應器出口樣品的溫度更高一些,故選a;
②兩個反應都是氣體體積減小的反應,從平衡的角度來看,增大壓力,能使該反應速率增大、原料轉(zhuǎn)化率升高,但是壓強高,意味著設備要好,這就需要加大成本的投入,因此需要適當加壓;
③CO和H2生成二甲醚的化學方程式為:2CO+4H2![]() CH3OCH3+H2O;
CH3OCH3+H2O;
④題中給出了幾個物質(zhì)的沸點,甲醇的沸點較高,且和其他物質(zhì)的沸點相差較大,可以通過降溫冷凝的方法得到甲醇粗品,再經(jīng)過蒸餾提純;
II、(3)①燃料電池的構(gòu)造中有質(zhì)子交換膜,則說明反應中產(chǎn)生H+,故負極電極反應為:CH3OH-6e-+H2O=CO2+6H+;
②結(jié)合題中給出的化學方程式,可以推出另外兩種單體分別為: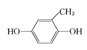 、
、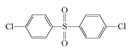 或
或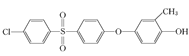 。
。


 特高級教師點撥系列答案
特高級教師點撥系列答案科目:高中化學 來源: 題型:
【題目】有下列幾組物質(zhì),請將序號填入下列空格內(nèi):
A、CH2=CH﹣COOH和油酸(C17H33COOH)
B、12C60和石墨
C、![]() 和
和![]()
D、35Cl和37Cl
E、乙醇和乙二醇
(1)互為同位素的是 ;
(2)互為同系物的是 ;
(3)互為同素異形體的是 ;
(4)互為同分異構(gòu)體的是 ;
(5)既不是同系物,又不是同分異體,也不是同素異形體,但可看成是同一類物質(zhì)的是 .
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將a g二氧化錳粉末加入b mol/L的濃鹽酸c L中加熱完全溶解,反應中轉(zhuǎn)移電子d個,設NA為阿伏加德羅常數(shù)的值,下列敘述正確的是
A.可以收集到氯氣![]() L
L
B.NA可表示為:![]()
C.反應后溶液中的Cl―數(shù)目為:![]()
D.反應后溶液中的H+數(shù)目為:![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對于下列化學平衡在一定條件下發(fā)生移動的描述,不正確的是
A.Cl2+H2O![]() HCl+HClO,氯水中加入碳酸鈣,漂白性增強
HCl+HClO,氯水中加入碳酸鈣,漂白性增強
B.ZnS + Cu2+![]() CuS + Zn2+,閃鋅礦(ZnS)遇CuSO4溶液轉(zhuǎn)化為銅藍(CuS)
CuS + Zn2+,閃鋅礦(ZnS)遇CuSO4溶液轉(zhuǎn)化為銅藍(CuS)
C.2NO2![]() N2O4 ΔH<0,將裝有NO2的玻璃球浸入熱水中,紅棕色變淺
N2O4 ΔH<0,將裝有NO2的玻璃球浸入熱水中,紅棕色變淺
D.Cr2O72-(橙色)+H2O![]() 2CrO42-(黃色) +2H+,K2Cr2O7溶液中滴加幾滴濃硫酸,橙色加深
2CrO42-(黃色) +2H+,K2Cr2O7溶液中滴加幾滴濃硫酸,橙色加深
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用下圖裝置探究1-溴丁烷在氫氧化鈉溶液中發(fā)生的反應,觀察到高錳酸鉀酸性溶液褪色。下列分析不正確的是
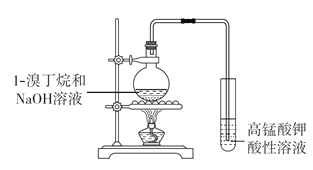
A.推斷燒瓶中可能生成了1-丁醇或1-丁烯
B.用紅外光譜可檢驗在該條件下反應生成有機物中的官能團
C.將試管中溶液改為溴水,若溴水褪色,則燒瓶中一定有消去反應發(fā)生
D.通過檢驗反應后燒瓶內(nèi)溶液中的溴離子,可確定燒瓶內(nèi)發(fā)生的反應類型
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】I、為了研究化學反應A+B=C+D的能量變化情況,某同學設計了如圖所示裝置。當向盛有A的試管中滴加試劑B時,看到U形管中甲處液面下降乙處液面上升。試回答下列問題:
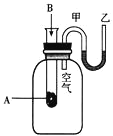
(1)該反應為________反應(填“放熱”或“吸熱”)。
(2)A和B的總能量比C和D的總能量_________(填“高”或“低”)。
(3)該反應的物質(zhì)中的化學能通過化學反應轉(zhuǎn)化成________釋放出來。
(4)該反應的反應物化學鍵斷裂吸收的能量________(填“高”或“低”)于生成物化學鍵形成放出的能量。
(5)Ⅱ、同素異形體相互轉(zhuǎn)化的反應熱相當小,而且轉(zhuǎn)化速率較慢,有時還很不完全,測定反應熱很困難。現(xiàn)在可根據(jù)蓋斯提出的“不管化學過程是一步完成還是分幾步完成,這個總過程的熱效應是相同的”觀點來計算反應熱。
已知:
①P4(白磷,s)+5O2(g)= P4O10(s) ΔH=-2983.2 kJ·mol1
②P(紅磷,s)+5/4O2(g)=1/4P4O10(s) ΔH=-738.5 kJ·mol1
則白磷轉(zhuǎn)化為紅磷的熱化學方程式為__________。相同狀況下,能量狀態(tài)較低的是________;白磷的穩(wěn)定性比紅磷_________(填“高”或“低”)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】以CH4和H2O為原料,通過下列反應來制備甲醇。
I:CH4(g) + H2O(g) ![]() CO(g) + 3H2(g) △H=+206.0kJ·mol-1
CO(g) + 3H2(g) △H=+206.0kJ·mol-1
II:CO(g) + 2H2(g) ![]() CH3OH(g) △H=-129.0kJ·mol-1
CH3OH(g) △H=-129.0kJ·mol-1
(1)一定溫度下,在容積2L且固定的兩個密閉容器中,按如下方式加入反應物發(fā)生反應I,一段時間后達到平衡。
容 器 | 甲 | 乙 |
反應物投入量 | 1molCH4、1molH2O | a molCH4、a molH2O、b molCO、c molH2 |
經(jīng)測定甲容器經(jīng)過5min達到平衡,平衡后甲中氣體的壓強為開始的1.2倍,若要使平衡后乙與甲中相同組分的體積分數(shù)相等,且起始時維持化學反應向逆反應方向進行,則b的取值范圍為__________。
(2)將1.0molCH4和2.0molH2O(g)通入容積為10L的反應室,在一定條件下發(fā)生反應I,測得在一定的壓強下CH4的轉(zhuǎn)化率與溫度的關系如圖。
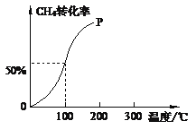
①假設100 ℃時達到平衡所需的時間為5min,則用H2表示該反應的反應速率為______。
②100℃時反應I的平衡常數(shù)為____________。
(3)若在恒溫恒壓容器內(nèi)進行反應II,下列能說明該反應達到平衡狀態(tài)的有________(填序號)。
A.有2個H—H鍵生成的同時有 3個C—H鍵斷裂
B.CO百分含量保持不變
C.容器中混合氣體的壓強保持不變
D.容器中混合氣體的密度保持不變
(4)在壓強為0.1MPa、溫度為300℃條件下,將amol CO與3amol H2的混合氣體在催化劑作用下發(fā)生反應II生成甲醇,平衡后將容器的容積壓縮到原來的l/2,其他條件不變,對平衡體系產(chǎn)生的影響是__________(填序號)。
A.c(H2) 減少 B.正反應速率加快,逆反應速率減慢
C.n(CH3OH) 增加 D.![]() 減小 E.平衡常數(shù)K增大
減小 E.平衡常數(shù)K增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化學用語是學好化學知識的重要基礎,下列有關化學用語表示正確的有( )
①用電子式表示HCl的形成過程:![]()
②MgCl2的電子式:![]()
③質(zhì)量數(shù)為133、中子數(shù)為78的銫原子:![]() Cs
Cs
④S2﹣的結(jié)構(gòu)示意圖:![]()
⑤次氯酸分子的結(jié)構(gòu)式:H-O-Cl
⑥ CO2的分子比例模型示意圖:![]()
A.2個B.3個C.4個D.5個
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用水鈷礦(主要成分為Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)可以制取多種化工試劑,以下為草酸鈷晶體和氯化鈷晶體的制備流程,回答下列問題:
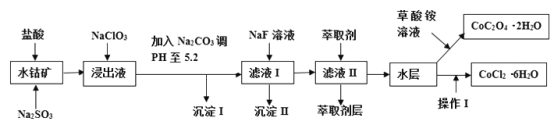
已知:①浸出液中含有的陽離子主要有H+、Co2+、Fe2+、Mn2+、Al3+、Mg2+、Ca2+等;②沉淀I中只含有兩種沉淀;③流程中部分陽離子以氫氧化物形式沉淀時溶液的pH見下表:
沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
開始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)浸出過程中Co2O3發(fā)生反應的離子反應方程式為_________________。
(2)NaClO3在浸出液中發(fā)生的離子反應方程式為______________。
(3)加入Na2CO3調(diào)PH至5.2,目的是________;萃取劑層含錳元素,則沉淀II的主要成分為_____。
(4)操作I包括:將水層加入濃鹽酸調(diào)整PH為2-3,______、_____、過濾、洗滌、減壓烘干等過程。
(5)為測定粗產(chǎn)品中CoCl2·6H2O含量,稱取一定質(zhì)量的粗產(chǎn)品溶于水,加入足量硝酸酸化的硝酸銀溶液,過濾、洗滌、干燥,測沉淀質(zhì)量。通過計算發(fā)現(xiàn)粗產(chǎn)品中CoCl2·6H2O質(zhì)量分數(shù)大于100%,其原因可能是_____(回答一條原因即可)。
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com