
| 陽離子 | K+ Na+ Fe2+ Ba2+ NH4+ |
| 陰離子 | OHˉ NO3ˉ Iˉ HCO3ˉ AlO2ˉ HSO4ˉ |
| ||
| ||


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
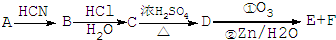
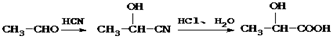
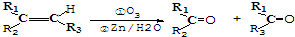
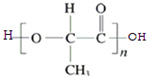 )的合成路線流程圖(無機試劑任選用).
)的合成路線流程圖(無機試劑任選用).
查看答案和解析>>
科目:高中化學 來源: 題型:
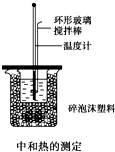 50mL 0.50mol/L鹽酸與50mL 0.55mol/L NaOH溶液在如圖所示的裝置中進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:
50mL 0.50mol/L鹽酸與50mL 0.55mol/L NaOH溶液在如圖所示的裝置中進行中和反應,通過測定反應過程中所放出的熱量可計算中和熱,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 實驗序號 | 實 驗 | 實驗現象 | 結 論 |
| 實驗Ⅱ | 將實驗I中收集到的氣體點燃 | 安靜燃燒, 火焰呈淡藍色 | 氣體成分為 |
| 實驗Ⅲ | 將實驗I中的白色不溶物濾出、洗滌,取少量加入足量 | 白色不溶物中含有MgCO3 | |
| 實驗Ⅳ | 取實驗Ⅲ中的濾液,向其中加入適 量 | 產生白色沉淀,溶液紅色變淺 | 溶液中存在CO32- 離子 |

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com