
【題目】某課外小組分別用如圖所示裝置對原電池和電解原理進行實驗探究。

請回答:
Ⅰ.用圖 1 所示裝置進行第一組實驗。
(1)在保證電極反應不變的情況下,不能替代 Cu 作電極的是__(填字母序號)。
A 鋁 B 石墨 C 銀 D 鉑
(2)N 極發生反應的電極反應式為__。
Ⅱ.用圖 2 所示裝置進行第二組實驗。實驗過程中,觀察到與第一組實驗不同的現象:兩極均有氣體產生,Y極區溶液逐漸變成紫紅色;停止實驗,鐵電極明顯變細,電解液仍然澄清。 查閱資料得知,高鐵酸根離子(FeO42-)在溶液中呈紫紅色。
(3)電解過程中,X 極區溶液的 pH__(填“增大”“減小”或“不變”)。
(4)電解過程中,Y 極發生的電極反應之一為 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 極收集到672 mL 氣體,在 Y 極收集到 168 mL 氣體(均已折算為標準狀況時氣體體積),則 Y 電極(鐵電極)質量減少____g。
(5)在堿性鋅電池中,用高鐵酸鉀作為正極材料,電池反應為 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,該電池正極發生的反應的電極反應式為__。
【答案】A 2H++2e-=H2↑(或2H2O+2e﹣=H2↑+2OH﹣) 增大 0.28 FeO42-+6e﹣+5H2O=Fe2O3+10OH﹣
【解析】
Ⅰ圖1中,左邊裝置是原電池,較活潑的金屬鋅作負極,較不活潑的金屬銅作正極,如果要找電極材料代替銅,所找材料必須是不如鋅活潑的金屬或導電的非金屬,M是陽極,N是陰極,電解池中陰極上陽離子得電子發生還原反應,原電池放電時,陰離子向負極移動;
Ⅱ該電解池中,陽極材料是活潑金屬,則電解池工作時,陽極上鐵失電子發生氧化反應,同時氫氧根離子失電子生成氧氣,陰極上氫離子得電子發生還原反應,根據陰陽極上轉移電子數相等計算鐵反應的質量,在堿性鋅電池中,正極上得電子發生還原反應。
(1)在保證電極反應不變的情況下,仍然是鋅作負極,則正極材料必須是不如鋅活潑的金屬或導電的非金屬,鋁是比鋅活潑的金屬,所以不能代替銅,故選A;
(2)N電極連接原電池負極,所以是電解池陰極,陰極上氫離子得電子發生還原反應,電極反應式為:2H++2e-=H2↑(或2H2O+2e﹣=H2↑+2OH﹣);
(3)電解過程中,陰極上氫離子放電生成氫氣,則陰極附近氫氧根離子濃度大于氫離子溶液,溶液呈堿性,溶液的pH增大,故答案為增大;
(4)X電極上析出的是氫氣,Y電極上析出的是氧氣,且Y電極失電子進入溶液,設鐵質量減少為xg,根據轉移電子數相等得![]() ,x=0.28,即鐵質量減少0.28g;
,x=0.28,即鐵質量減少0.28g;
(5)正極上高鐵酸根離子得電子發生還原反應,反應方程式為FeO42-+6e﹣+5H2O=Fe2O3+10OH﹣。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:
【題目】現有 A、B、C、D、E、F 六種短周期主族元素,其相關性質信息如下:
元素 | 相關信息 |
A | 地殼中含量最多的金屬元素 |
B | 原子核外電子數和周期序數相等 |
C | 最外層電子數是次外層電子數的 3 倍 |
D | 最高正價與最低負價代數和為 4,常溫下單質為固體 |
E | 在短周期元素中,原子半徑最大 |
F | M 層比L 層少 1 個電子 |
請根據上述信息,完成下列問題:
(1)請給出元素 D 在元素周期表中的位置:________。
(2)請將 A、D、E、F 四種元素的簡單離子按照離子半徑由大到小排序(用離子符號表示):__________。
(3)請給出化合物 BFC 的電子式:______。
(4)用電子式表示 E 與 F 形成化合物 EF 的過程:______。
(5)請將 A、D、F 三種元素的最高價氧化物對應的水化物按照酸性由強到弱排序(用化學式表示):__________。
(6)元素 A 的單質常用于野外焊接鋼軌,請寫出該反應的化學方程式:________。
(7)單質 A 能溶于 E 的最高價氧化物對應水化物的水溶液,請給出該反應的離子方程式:_____________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列離子方程式書寫正確的是
A.向鐵粉中加入足量稀鹽酸:Fe+2H+=Fe3++H2↑
B.向FeCl3溶液中加入少量銅粉:Fe3++Cu=Fe2++Cu2+
C.Cu與稀硝酸反應:3Cu+8H++2![]() =3Cu2++2NO↑+4H2O
=3Cu2++2NO↑+4H2O
D.向AlCl3溶液中滴加濃氨水至過量:Al3++4OH-=![]() +2H2O
+2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鈉、鎂、鋁的單質及其化合物是中學階段重點研宄的物成.
(1)按性質分類,Na2O2____________(填“屬于”或“不屬于”)堿性氧化物。
(2)用離子方程式說明Al(OH)3是兩性氫氧化物: ____________________。
(3)某同學用如圖所示裝置進行實驗探究有關鈉、鎂、鋁的化合物的性質(夾持儀器省略)。將液體A遂滿加入到固體B中,回答下列問題:
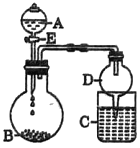
①若A為70%硫酸溶液,B為Na2SO3,C盛有氫硫酸(H2S)飽和溶液,旋開E后,C中發生反應的化學方程式為________________________。
②若A為水,B為Mg3N2,C中盛有AlC13溶液,旋開E,足夠長的時間后,C中發生反應的離子方程式為__________________________。
③若A為濃鹽酸,B為NaClO3,C中盛有KI-淀粉溶液,旋開E后,C中的現象是________________,繼續通氣體于C中,足夠長的時間后,發現C中溶液的顏色消失,這是因為在溶液中I2能被Cl2氧化為HIO3,寫出該反應的化學方程式: _______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】硫化堿法是工業上制備Na2S2O3的方法之一,反應原理:2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2(該反應ΔH>0),某研究小組在實驗室用硫化堿法制備Na2S2O3·5H2O流程如下:

(1)吸硫裝置如圖所示:

①裝置B的作用是檢驗裝置A中SO2的吸收效率,B中試劑是____________,表明SO2吸收效率低的實驗現象是B中_________。
②為了使SO2盡可能吸收完全,在不改變A中溶液濃度、體積的條件下,除了及時攪拌反應物外,還可采取的合理措施是________、________。(寫出兩條)
(2)Na2S2O3溶液是定量實驗中的常用試劑,測定其濃度的過程如下:準確稱取ag KIO3(化學式量:214)固體配成溶液,加入過量KI固體和H2SO4溶液,滴加指示劑,用Na2S2O3溶液滴定至終點,消耗Na2S2O3溶液的體積為VmL。則c(Na2S2O3)=_________ mol·L-1。(只列出算式,不作運算)已知:![]() +I2=
+I2=![]() +2I-
+2I-
(3)某同學第一步和第二步的操作都很規范,第三步滴速太慢,這樣測得的Na2S2O3濃度可能 ____(填“無影響”、“偏低”或“偏高”),原因是_________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】吡唑類化合物是重要的醫用中間體,如圖是吡唑類物質L的合成路線。
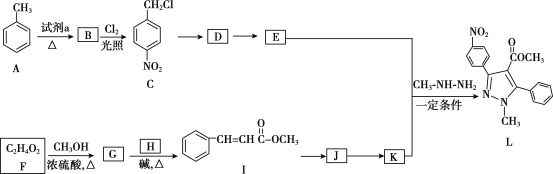
已知:R1—CHO+R2CH2—COOR3![]()
R1—CHO+R2NH2![]() R1—CH=N—R2
R1—CH=N—R2
(1)試劑a是__。
(2)C生成D的反應類型是__。
(3)D生成E的化學方程式是___。
(4)生成G的化學方程式是__。
(5)H的結構簡式是__。
(6)寫出符合下列條件的I的同分異構體的結構簡式__。
a.是反式結構
b.能發生銀鏡反應
c.苯環上的一氯代物有2種
d.1mol該有機物能與2mol氫氧化鈉反應
(7)K的分子式是C10H8O2,K的結構簡式是__。
(8)以2-甲基丙烯和乙酸為原料,選用必要的無機試劑,合成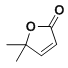 ,寫出合成路線__(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)
,寫出合成路線__(用結構簡式表示有機物,用箭頭表示轉化關系,箭頭上注明試劑和反應條件)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】元素周期表與元素周期律在學習、研究中有很重要的作用。下表是元素周期表中6種元素的相關信息,其中Q、W、X位于同一周期。
元素 | 信息 |
Q | 單質是穩定的半導體材料,用于制造芯片 |
W | 最高化合價為+7價 |
X | 最高價氧化物對應的水化物在本周期中堿性最強 |
Y | 焰色反應為紫色(透過藍色鈷玻璃片) |
Z | 地殼中含量最高的金屬元素,其合金可用于制造飛機外殼 |
M | 原子結構示意圖為 |
(1)Q元素所在周期表的位置為_____。
(2)W單質的電子式為_____。
(3)Z的單質與X的最高價氧化物對應的水化物反應的離子方程式為_____。
(4)Y的金屬性強于X,請結合原子結構解釋其原因_____。
(5)下列對于M及其化合物的推斷中,正確的是_____(填序號)。
①M的最低負化合價與W的最低負化合價相同
②M的氫化物的穩定性弱于W的氫化物的穩定性
③M的單質可與X和W形成的化合物的水溶液發生置換反應
(6)與M位于同一主族,電子層數比M多一層的元素在生活中的用途是_____(寫出一條即可)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NA代表阿伏加德羅常數的值,下列說法正確的是( )
A. 100 mL 1 mol·L-1FeCl3溶液中所含Fe3+的數目為0.1NA
B. 常溫常壓下,11.2 L甲烷和乙烯混合物中含氫原子數目為2NA
C. 密閉容器中,2 mol SO2和1 mol O2催化反應后分子總數為2NA
D. 標準狀況下,124 g P4中所含P—P鍵數目為6NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某實驗小組用下列裝置制備溴苯,下列說法錯誤的是
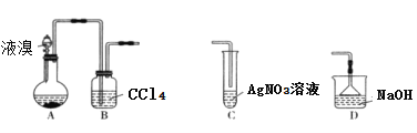
A. 裝置A中長玻璃導管僅起冷凝回流作用,裝置B中的實驗現象是CCl4由無色變橙色
B. 若裝置B后連接裝置C,裝置C中生成淡黃色沉淀,可證明裝置A中發生取代反應
C. 若裝置B后連接裝置D,則裝置D的作用是吸收尾氣
D. 向反應后的裝置A中加入NaOH溶液,振蕩靜置,下層為無色油狀液體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com