
【題目】2019年諾貝爾化學獎頒給了三位為鋰離子電池發展作出重要貢獻的科學家。用太陽能電池給磷酸鐵鋰鋰離子電池充電示意圖如圖所示,陽極反應式為:LiFePO4-xe-=xLi++Li1-xFePO4。下列敘述錯誤的是

A.晶體硅能將太陽能轉化為電能,但硅太陽能電池不屬于原電池
B.該鋰電池放電時負極反應為:LixC6-xe-=xLi++Li1-xC6
C.該鋰電池放電時,電子通過外電路由鋁箔流向鋼箔
D.磷酸鐵鋰鋰離子電池充放電過程通過Li+遷移實現,Fe、C、P元素化合價均不發生變化
【答案】D
【解析】
由磷酸鐵鋰鋰離子電池圖解可知,鋰離子從右向左移動,鋼箔為陽極,鋁箔為陰極,據此回答問題。
A.晶體硅能將太陽能轉化為電能,但硅太陽能電池不屬于原電池,A正確;
B.該鋰電池放電時負極為鋁箔,發生氧化反應,陽極反應式為LiFePO4-xe-=xLi++Li1-xFePO4,即放電時正極為xLi++Li1-xFePO4+xe-= LiFePO4,即負極反應為:LiC6-xe-=xLi++Li1-xC6,B正確;
C.放電時Li+右移,鋁箔是負極,鋼箔是正極,電子由鋁箔沿導線流向鋼箔,C正確;
D.磷酸鐵鋰鋰離子電池充放電過程通過Li+遷移實現,Li、Fe元素化合價發生變化,D錯誤;
答案為D。


科目:高中化學 來源: 題型:
【題目】對溴苯乙烯與丙烯的共聚物是一種高分子阻燃劑,具有低毒、熱穩定性好等優點。完成下列填空:
(1)寫出該共聚物的結構簡式____________。
(2)實驗室由乙苯制取對溴苯乙烯,需先經兩步反應制得中間體![]() ,寫出該兩步反應所需的試劑及條件____________。
,寫出該兩步反應所需的試劑及條件____________。
(3)將![]() 與足量氫氧化鈉溶液共熱得到A,A在酸性條件下遇FeCl3溶液不顯色。A的結構簡式為____________。由上述反應可推知____________。由A生成對溴苯乙烯的反應條件為____________。
與足量氫氧化鈉溶液共熱得到A,A在酸性條件下遇FeCl3溶液不顯色。A的結構簡式為____________。由上述反應可推知____________。由A生成對溴苯乙烯的反應條件為____________。
(4)丙烯催化二聚得到2,3-二甲基-1-丁烯,B與2,3-二甲基-1-丁烯互為同分異構體,且所有碳原子處于同一平面。
寫出B的結構簡式____________。
設計一條由2,3-二甲基-1-丁烯制備B的合成路線____________。(合成路線常用的表示方式為:![]() )
)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】有人設計了如圖所示實驗裝置,目的是做鈉與水反應實驗,并驗證①鈉的物理性質;②鈉與水反應的產物是什么。

(1)當進行適當操作時還需要的儀器有________。
(2)如何進行操作?__________。
(3)實驗現象是_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某化學小組用如圖所示裝置驗證鹵素單質氧化性的相對強弱。下列說法不正確的是( )
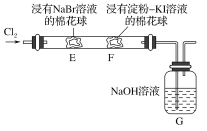
A.E處棉花球變成黃色,說明Cl2的氧化性比Br2強
B.F處棉花球變成藍色,說明Br2的氧化性比I2強
C.E處發生反應的離子方程式為:Cl2+2Br-===2Cl-+Br2
D.G裝置中NaOH溶液與Cl2反應的離子方程式為:2OH-+Cl2===ClO-+Cl-+H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氧化亞鐵的制備:在一支試管中加入少量的硫酸亞鐵溶液,然后滴入氫氧化鈉溶液。
(1)觀察到的實驗現象是_________。
(2)用化學方程式表示產生上述現象的原因:_______________、________________
(3)在制取氫氧化亞鐵時,可將吸有氫氧化鈉溶液的長膠頭滴管伸入到硫酸亞鐵液面下,再擠出氫氧化鈉溶液的目的是_________。
(4)下列各圖所示的實驗中能較長時間看到Fe(OH) 2 白色沉淀的是_______。
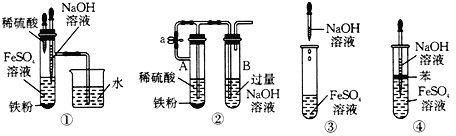
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在一個固定容積的密閉容器中,可逆反應m A(g)+n B(g)![]() p C(g)+q D(g),當 m、 n、 p、q 為任意整數時,下列說法一定能說明反應已達到平衡的是( )
p C(g)+q D(g),當 m、 n、 p、q 為任意整數時,下列說法一定能說明反應已達到平衡的是( )
①體系的壓強不再改變 ②體系的密度不再改變 ③各組分的濃度不再改變 ④各組分的質量分數不再改變 ⑤反應速率 v(A)∶v(B)∶v(C)∶v(D)=m∶n∶p∶q ⑥單位時間內 m mol A 發生斷鍵反應,同時 p mol C 也發生斷鍵反應
A. ③④⑤⑥ B. ③④⑥ C. ①③④ D. ②③⑥
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,0.1 mol·L-1的HA溶液中c(OH-)/c(H+)=1×10-8,下列敘述中正確的是( )
A. 0.01 mol·L-1HA的溶液中c(H+)=1×10-4mol·L-1
B. pH=3的HA溶液與pH=11的NaOH溶液等體積混合后所得溶液中c(Na+)>c(A-)>c(OH-)>c(H+)
C. 濃度均為0.1 mol·L-1的HA溶液和NaA溶液等體積混合后所得溶液顯酸性,則c(OH-)-c(H+)<c(HA)-c(A-)
D. pH=3的HA溶液與pH=11的NaOH溶液按體積比1:10混合后所得溶液中c(OH-)+c(A-)=c(H+)+c(Na+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究性學習小組進行CH4的制備及性質探究實驗。根據反應:CH3COONa(固體)+NaOH(固體)→ Na2CO3+CH4↑制備氣體。
(1)用CH4氣體分別進行下列實驗:
①通入酸性KMnO4溶液,現象是______________________________。
②在無色玻璃集氣瓶中與C12混合后光照,現象是___________________________。
(2)為了驗證CH4是否具有還原性,某小組設計了如下實驗:

①當玻璃管中的氧化銅由黑色變為紅色時,說明CH4具有還原性。你認為這一結論是否正確?__________(填“正確”或“不正確”),理由是______________________________。
②實驗過程中還觀察到無水CuSO4逐漸變藍,澄清石灰水出現渾濁現象,則CH4與CuO反應的化學方程式為______________________________。
(3)研究小組將CH4通入溴水時,發現溴水逐漸褪色,你認為原因可能是______________。請設計一個實驗方案證明你的結論(用文字表示,不必畫實驗裝置圖)_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】等物質的量的X(g)與Y(g)在密閉容器中進行可逆反應:X(g)+Y(g) ![]() 2Z(g)+W(s) ΔH<0,下列敘述正確的是 ( )
2Z(g)+W(s) ΔH<0,下列敘述正確的是 ( )
A. 平衡常數K值越大,X的轉化率越大
B. 達到平衡時,反應速率v正(X)=2v逆(Z)
C. 達到平衡后降低溫度,正向反應速率減小的倍數大于逆向反應速率減小的倍數
D. 達到平衡后,升高溫度或增大壓強都有利于該反應平衡向逆反應方向移動
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com