
【題目】2017年11月16日新聞報道“阿斯利康哮喘”新藥獲批上市,哮喘率降低近51%,有機物Z可用于治療哮喘、系統性紅斑狼瘡等。其合成路線如下圖所示
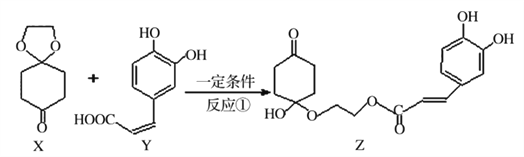
(1)化合物X的有_______種化學環境不同的氫原子。
(2)下列說法正確的是_______.
A.X是芳香化合物 B.Ni催化下Y能與5molH2加成
C.Z能發生加成、取代及消去反應 D. lmolZ最多可與5molNaOH反應
(3)Y與過量的溴水反應的化學方程式為_________。
(4)X可以由_______(寫名稱)和M(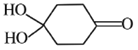 ) 分子間脫水而得;一定條件下,M發生1個—OH的消去反應得到穩定化合物N (分子式為C6H8O2),則N的結構簡式為_____(己知烯醇式不穩定,會發生分子重排,例如:
) 分子間脫水而得;一定條件下,M發生1個—OH的消去反應得到穩定化合物N (分子式為C6H8O2),則N的結構簡式為_____(己知烯醇式不穩定,會發生分子重排,例如: 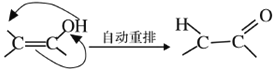 )。
)。
(5)Y也可以與環氟丙烷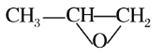 )發生類似反應①的反應,其生成物的結構簡式為_________(寫一種);Y的同分異構體很多種,其中有苯環、苯環上有二個取代基(且酚羥基的位置和數目都不變)、屬于酯的同分異構體有_____種。
)發生類似反應①的反應,其生成物的結構簡式為_________(寫一種);Y的同分異構體很多種,其中有苯環、苯環上有二個取代基(且酚羥基的位置和數目都不變)、屬于酯的同分異構體有_____種。
(6)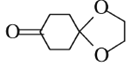 可由
可由 和有機物H分子間脫去一分子水而得,則H的名稱為________;通常采用
和有機物H分子間脫去一分子水而得,則H的名稱為________;通常采用![]() 為原料合成
為原料合成 ,請參照題目路線圖設計該合成路線(無機試劑任選) _______。(合成路線常用的表示方式為:
,請參照題目路線圖設計該合成路線(無機試劑任選) _______。(合成路線常用的表示方式為:  )
)
【答案】 3 C  乙二醇
乙二醇 
 或
或 8 乙二醇
8 乙二醇 
【解析】(1)根據化合物X的結構簡式得出有3種不同化學環境的氫原子。
(2)C項,Z中含有碳碳雙鍵和苯環,可以發生加成反應,含有酚羥基,能發生取代反應,醇羥基連接的碳原子的鄰位碳上有氫原子,能發生消去反應,故C項正確;A項,X中沒有苯環,不是芳香化合物,故A項錯誤;
B項,Y中苯環消耗3molH2,碳碳雙鍵消耗1molH2,所以Y可與4molH2發生加成反應,故B項錯誤;D項,Z中含有酚羥基和酯基,最多可與3molNaOH反應,故D項錯誤。
綜上所述,本題正確答案為C。
(3)酚羥基激活苯環鄰位和對位上的氫與溴發生取代反應,碳碳雙鍵與溴發生加成反應,所以Y與過量的溴水反應的化學方程式為 。
。
(4)根據X的結構簡式推出M與乙二醇分子間脫水制備得到X,M中醇羥基連接的碳原子的鄰位碳上有氫原子,能發生消去反應,發生1個-OH的消去反應得到烯醇式結構,根據材料知烯醇式不穩定發生重排,生成穩定化合物N,則N的結構簡式為![]() 。
。
(5)根據反應①,Y與環氧丙烷(![]() )發生反應,其生成物的結構簡式為
)發生反應,其生成物的結構簡式為 或
或  ;苯環、苯環上有三個取代基(且酚羥基的位置和數目都不變)、屬于酯的取代基有4種:
;苯環、苯環上有三個取代基(且酚羥基的位置和數目都不變)、屬于酯的取代基有4種:![]() 、
、![]() 、
、![]() 、
、![]() (或
(或 ),苯環上取代基的位置有2種可能
),苯環上取代基的位置有2種可能 ,所以Y的同分異構體8種。
,所以Y的同分異構體8種。
(6)![]() 可由
可由![]() 和有機物H分子間脫去一分子水而得,根據原子守恒和碳架結構不變,可知H的結構簡式為HOCH2CH2OH,名稱為乙二醇;采用
和有機物H分子間脫去一分子水而得,根據原子守恒和碳架結構不變,可知H的結構簡式為HOCH2CH2OH,名稱為乙二醇;采用![]() 為原料合成
為原料合成![]() 的流程為
的流程為 。
。


科目:高中化學 來源: 題型:
【題目】將a克Fe2O3、Al2O3樣品溶解在過量的400mL 0.1molL﹣1的硫酸溶液中,然后向其中加入NaOH 溶液使Fe3+、Al3+剛好完全沉淀,用去NaOH 溶液100mL,則NaOH 溶液的濃度為( )
A. 0.1 molL﹣1 B. 0.2 molL﹣1 C. 0.4 molL﹣1 D. 0.8 molL﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】碳是自然界中形成化合物種類最多的元素,CO和CO2是碳的最常見氧化物。
(1)研究和解決二氧化碳捕集和轉化問題是當前科學研究的前沿領域。在太陽能的作用下,缺鐵氧化物[Fe0.9O]能分解CO2,其過程如圖1所示。過程①的化學方程式是______。在過程②中每產生0.1molO2,轉移電子______mol。

(2)在催化劑作用下,將二氧化碳和氫氣混合反應生成甲烷,是目前科學家們正在探索的處理空氣中的二氧化碳的方法之一。
①已知:
共價鍵 | C=O | H—H | C—H | O—H |
鍵能/(kJmol-1) | 745 | 436 | 413 | 463 |
則CO2(g)+4H2(g)![]() CH4(g)+2H2O(g) △H=______kJmol-1。
CH4(g)+2H2O(g) △H=______kJmol-1。
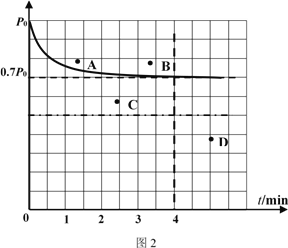
②向1L固定容積的密閉容器中加入4.0 mol H2(g)、1.0mol CO2,控制條件(催化劑:銠—鎂合金、高溫T1)使之反應,若測得容器內氣體的壓強隨著時間的變化如圖2所示。則4 min時容器內氣體的密度為______;溫度T1 下,該反應的化學平衡常為______。若采用2 L固定容積的密閉容器,投料量、催化劑和反應溫度均保持不變,則反應重新達到平衡時對應體系內的壓強的點是______(填字母)。
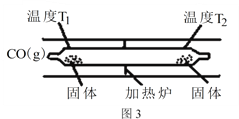
(3)工業合成原料氣CO會與設備、管道及催化劑表面的金屬鐵、鎳反應,生成羰基化合物。四羰基鎳是熱分解法制備高純鎳的原料,也是有機合成中供給一氧化碳的原料,還可做催化劑。Ni(s)+4CO(g)![]() Ni(CO)4(g) △H<0 Ni(CO)4(g)
Ni(CO)4(g) △H<0 Ni(CO)4(g)![]() Ni(s)+4CO(g)。如圖3所示,在石英真空管的溫度為T1一端,放入少量粗鎳和CO(g),一段時間后,在溫度為T2的一端可得到純凈的鎳。則溫度T1______T2(填“>”“<”或“=”),上述反應體系中循環使用的物質為______(填化學式)。
Ni(s)+4CO(g)。如圖3所示,在石英真空管的溫度為T1一端,放入少量粗鎳和CO(g),一段時間后,在溫度為T2的一端可得到純凈的鎳。則溫度T1______T2(填“>”“<”或“=”),上述反應體系中循環使用的物質為______(填化學式)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋰離子電池已經成為應用最廣泛的可充電電池,某種鋰離子電池的結構示意圖如下,它在放電時有關離子轉化關系如圖所示,下列說法正確的是

A. Li+透過膜除允許Li+通過外,還允許H2O分子通過
B. 充電時,電池內部發生的總反應為Li++Fe2+![]() Li+Fe3+
Li+Fe3+
C. 充電時,鈦電極與外電源的負極相連
D. 放電時,進入貯罐的液體發生的離子反應方程式為:S2O82-+Fe2+=Fe3++2SO42-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】銅及其化合物在生產生活中有廣泛應用
(1)工業上以黃銅礦(CuFeS2)為原料,采用火法熔煉工藝生產銅的中間過程會發生反應:2Cu2O+Cu2S![]() 6Cu+SO2↑該反應的氧化劑是________,驗證反應產生的氣體是SO2的方法是___________。
6Cu+SO2↑該反應的氧化劑是________,驗證反應產生的氣體是SO2的方法是___________。
(2)將少量銅絲放入適量的稀硫酸中,溫度控制在50℃,加入H2O2,反應一段時間后,升溫到60℃,再反應一段時間后可制得硫酸銅,溫度控制在50℃~60℃的兩個原因除了加快反應速率外,還有___________。在CuSO4溶液中加入一定量的Na2SO3和NaCl溶液加熱,生成CuC1沉淀,寫出生成CuCl的離子方程式______________。
(3)堿式碳酸銅在有機催化劑、煙火制造和顏料、農藥生產中有廣泛的應用。某工廠以輝銅礦(主要成分為Cu2S,含少量Fe2O3、SiO2等雜質)為原料制備堿式碳酸銅的流程如下:
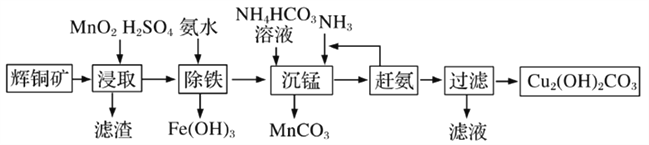
①輝銅礦在浸取前要富集與粉碎,粉碎的好處是___________。
②浸取過程中得到一種單質,寫出浸取時主要反應的化學方程式___________。
③寫出“沉錳”反應時離子方程式___________。
④“除鐵”這一步反應在25℃進行,加入氨水調節溶液pH為4后,溶液中銅離子最大濃度不超過_________mol/L。(已知Ksp[Cu(OH)2]=2.2×10-20)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為探究鐵和鐵的化合物的一些化學性質,某學生實驗小組設計了以下實驗。

(1)往A溶液中分別滴入幾滴KSCN溶液,溶液的顏色__________,
(2)根據上述過程寫出有關反應的離子方程式:Fe3O4→A _________________,A→B ___________。
(3)向B溶液中加入NaOH溶液,可看到的現象是_______________________________________,此過程中發生的氧化還原反應化學方程式為__________________________________。
(4)將A的飽和溶液滴入沸水中并不斷加熱,可制得_______________膠體;當光束通過該膠體時,可看到一條光亮的“通路”,這種現象稱為___________效應。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,用0.1mol/LNaOH溶液分別滴定體積均為20.00mL、濃度均為0.1mol/L的HX、HY溶液,pH隨NaOH溶液體積變化如圖。下列結論正確的是
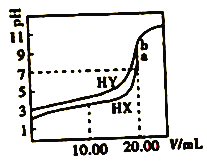
A. 水解常數:X->Y-
B. a、b兩點溶液混合后:c(HX)+c(HY)+c(H+)=c(OH-)
C. pH=7時,c(Y-)>c(X-)
D. 10.00mlL時,有c(Na+)>c(HX)>c(X-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向銅屑、稀鹽酸和鐵鹽的混合溶液中持續通入空氣可制備氯化銅。其反應過程如圖所示。

下列說法不正確的是
A. Fe3+對該反應有催化作用
B. 該過程中的Fe3+可由Fe(NO3)3提供
C. 可用K3[Fe(CN)6]溶液區分Fe3+與Fe2+
D. 制備CuCl2的總反應為2Cu + O2 + 4HCl = 2CuCl2 + 2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】(I)將35.2銅與140mL一定濃度的硝酸反應,銅完全溶解產生的NO和NO2混合氣體在標準狀況下的體積為11.2L。請回答:
(1)NO的體積為_____L,NO2的體積為______L。
(2)參加反應的硝酸的物質的量是_______mol。
(3)待產生的氣體全部釋放后,向溶液加入VmL a mol/L的NaOH溶液,恰好使溶液中的Cu2+全部轉化成沉淀,則原硝酸溶液的濃度為___________mol/L。(結果不需化簡)
(II)在標準狀況下,由CO和CO2組成的混合氣體為6.72 L,質量為10 g,求
(1)此混合物中CO和CO2物質的量之比_____。
(2)CO的質量分數_____
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com