

| A. | ①加CCl4 ②加苯 ③加酒精 | |
| B. | ①加酒精 ②加CCl4 ③加苯 | |
| C. | ①加苯 ②加CCl4 ③加酒精 | |
| D. | ①加苯 ②加酒精 ③加CCl4 |
 舉一反三同步巧講精練系列答案
舉一反三同步巧講精練系列答案 口算與應用題卡系列答案
口算與應用題卡系列答案 名師點睛字詞句段篇系列答案
名師點睛字詞句段篇系列答案科目:高中化學 來源: 題型:選擇題
| A. | 2AlCl3(熔融) $\frac{\underline{\;電解\;}}{冰晶}$ 4Al+3Cl2↑ | |
| B. | Fe2O3+3CO $\frac{\underline{\;高溫\;}}{\;}$ 2Fe+3CO2 | |
| C. | Fe+CuSO4═FeSO4+Cu | |
| D. | 2KCl(熔融)$\frac{\underline{\;電解\;}}{\;}$2K+Cl2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
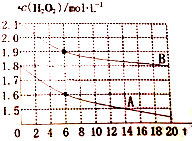 現有如下溶液:①1.0mL0.10mol•L-1雙氧水 ②1.0mL0.20mol•L-1雙氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有實驗均需加入1.0mL稀硫酸(足量),依據褪色時間長短判定反應速率快慢:
現有如下溶液:①1.0mL0.10mol•L-1雙氧水 ②1.0mL0.20mol•L-1雙氧水 ③3.0mL0.10mol•L-1KMnO4溶液 ④3.0mL0.010mol•L-1KMnO4溶液.所有實驗均需加入1.0mL稀硫酸(足量),依據褪色時間長短判定反應速率快慢:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若向2mL 1mol/LNaOH溶液中先加入2滴1mol/L MgCl2溶液,再加入2滴1mol/L的FeCl3溶液,可以證明Mg(OH)2沉淀轉化為Fe(OH)3沉淀 | |
| B. | 常溫下,某溶液中由水電離出來的c(OH-)=1.0×10-12mol•L-1,則該溶液可能為鹽酸,也可能為NaOH溶液 | |
| C. | 處理鍋爐水垢中的CaSO4時,依次加入飽和NaCO3溶液和鹽酸,水垢溶解,說明溶解度:S(CaCO3)<S(CaSO4) | |
| D. | 常溫下的醋酸銨溶液呈中性,則溶液中c(H+)=c(OH-)=1.0×10-7mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 降低溫度可以縮短反應達到平衡的時間 | |
| B. | 恒容時通入氬氣,壓強增大,平衡向右移動 | |
| C. | 恒容時通入X2,平衡向正反應方向移動,平衡常數不變 | |
| D. | 恒溫恒壓下,若混合氣體密度不變,說明反應已達平衡 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
| 實驗步驟 | 實驗現象 |
| ①將鎂條用砂紙打磨后,放入試管中,加入少量水后,加熱至水沸騰;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四處游動,發出“嘶嘶”聲,隨之消失,溶液變成紅色 |
| ②向新制得的Na2S溶液中滿加新制的氯水 | B.有氣體產生,溶液變成淺紅色 |
| ③將一小塊金屬鈉放入滴有酚酞溶液的冷水中 | C.劇烈反應,迅速產生大量無色氣體 |
| ④將鎂條投入稀鹽酸中 | D.反應不十分劇烈;產生無色氣體 |
| ⑤將鋁條投入稀鹽酸中 | E.生成白色膠狀沉淀,繼而沉淀消失 |
| ⑥向AlCl3溶液中滴加NaOH溶液至過量 | F.生成淡黃色沉淀 |
| 實驗內容 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 實驗現象(填A~F) | F | E |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com